Резюме
Актуальність. Ефективність та універсальність регіонарних методів знеболювання в поєднанні з мультимодальним підходом до періопераційної аналгезії дозволяють використовувати їх для дедалі більшої кількості пацієнтів, зокрема при проведенні операцій в гінекології. Мета: оцінити анальгетичну ефективність TAP-блоку як компонента мультимодальної аналгезії порівняно з відсутністю застосування регіонарних методів аналгезії при проведенні абдомінальних тотальних гістеректомій. Матеріали та методи. Нами проведено ретроспективне одноцентрове дослідження у відділеннях анестезіології, інтенсивної терапії та гінекології КП «Рівненська обласна клінічна лікарня імені Юрія Семенюка». У дослідження було включено пацієнтів із симптомними фіброміомами, ускладненими кровотечами зі статевих шляхів, які потребували проведення тотальної абдомінальної гістеректомії (надпіхвової ампутації матки з придатками), віком 40–65 років. Критеріями виключення з дослідження були: відмова пацієнта від участі у дослідженні на будь-якому з його етапів, клас за ASA > IV, індекс маси тіла > 40 кг/м2, застосування агоністів/агоністів-антагоністів опіатних рецепторів до операції, неконтрольована артеріальна гіпертензія, порушення ритму серця. До аналізу даних включені 43 пацієнти. Результати. Встановлено, що рівень болю за візуальною аналоговою шкалою у І групі досягав максимальних значень на етапах дослідження h12 та h24 і становив 4,8 [3,3; 5,8] бала та 5,3 [3,9; 6,4] бала, тоді як у пацієнтів ІІ групи на аналогічних етапах дослідження біль було оцінено в 2,7 [2,3; 3,5] бала та 2,1 [1,6; 4,1] бала відповідно (p < 0,05). Виявлено вірогідні відмінності рівня частоти серцевих скорочень між І та ІІ групами пацієнтів на етапі дослідження h24 (93 [87; 98] уд/хв у І групі порівняно з 72 [63; 79] уд/хв у ІІ групі, p = 0,05). Не встановлено вірогідних відмінностей середнього артеріального тиску між І та ІІ групами пацієнтів на всіх етапах дослідження, проте була тенденція до зниження цього показника впродовж усього дослідження в І групі пацієнтів. Середня добова потреба в налбуфіні на етапі дослідження h24 мала тенденцію (p = 0,07) до нижчих показників серед пацієнтів ІІ групи (40,9 ± 1,1 мг/добу) порівняно з показниками пацієнтів І групи (51,4 ± 2,9 мг/добу). На етапі дослідження h72 потреба в налбуфіні була вірогідно нижчою (p < 0,05) в ІІ групі та становила 5,8 ± 0,8 мг/добу порівняно з 22,5 ± 4,1 мг/добу в І групі. Середня тривалість госпіталізації серед пацієнтів І групи становила 6,8 ± 0,5 дня, серед пацієнтів ІІ групи — 4,2 ± 0,2 дня (p < 0,05). Висновки. Застосування двостороннього TAP-блоку із 0,25% бупівакаїном та ад’ювантом дексаметазоном продемонструвало тенденцію до зниження потреби в налбуфіні в першу післяопераційну добу на 25,7 %, на третю післяопераційну добу — в 3,9 раза (p < 0,05). Тривалість госпіталізації у пацієнтів ІІ групи зменшувалася на 2,6 дня (p < 0,05).
Background. The effectiveness and widespread use of regional anesthesia in combination with a multimodal approach to perioperative analgesia allow them to be used for an increasing number of patients, including those undergoing surgery in gynecology. The purpose of the study was to determine the effectiveness of transversus abdominis plane block as a component of multimodal analgesia compared to no regional methods of analgesia for a total abdominal hysterectomy. Materials and methods. We conducted a retrospective single-center study at the Department of Anaesthesiology and Intensive Care and the Department of Gynecology of Yuriy Semenyuk Rivne Regional Clinical Hospital (Ukraine). The study included patients aged 40–65 years with symptomatic fibroids complicated by vaginal bleedings, who required a total abdominal hysterectomy (supravaginal amputation of the uterus with ovaries). Exclusion criteria were: patient’s refusal to participate in the study at any of its stages, ASA class > IV, body mass index > 40 kg/m2, use of opioid receptor agonists/agonists-antagonists before surgery, uncontrolled arterial hypertension, heart rhythm disorders. Forty-three patients were included in data analysis. Results. It was found that the level of pain on visual analogue scale in the first group reached its maximum values at h12 and h24 stages of the study and was 4.8 [3.3; 5.8] and 5.3 [3.9; 6.4] points, respectively, while in patients of the second group at same stages of the study pain seve-rity was 2.7 [2.3; 3.5] and 2.1 [1.6; 4.1] points (p < 0.05). Significant differences were found in heart rate between the first and the second groups at h24 stage of the study (93 [87; 98] bpm in the first group and 72 [63; 79] bpm in the second, p = 0.05). There were no significant differences in mean blood pressure at all stages of the study; however, there was a tendency towards a decrease in these data throughout the study in the first group of patients. The ave-rage daily dose of nalbuphine at h24 stage has a tendency (p = 0.07) towards a decrease in the second group (40.9 ± 1.1 mg/day) compared with the first group (51.4 ± 2.9 mg/day). At h72 stage, the need in nalbuphine was significantly lower (p < 0.05) in the second group (5.8 ± 0.8 mg/day) compared to the first group (22.5 ± 4.1 mg/day). The average length of hospital stay in the first group was 6.8 ± 0.5 days, in the second one — 4.2 ± 0.2 days (p < 0.05). Conclusions. The use of bilateral transversus abdominis plane block with 0.25% bupivacaine and dexamethasone showed a tendency towards a reduction in the need for nalbuphine in the first postoperative day by 25.7 %, on the third postoperative day — by 3.9 times (p < 0.05). The length of hospital stay in the second group was decreased by 2.6 days compared to the first group (p < 0.05).
Вступ
Протоколи покращення відновлення після операцій (Enhanced Recovery After Surgery, ERAS) та техніки регіонарної анестезії продовжують розвиватися для різних напрямків хірургічних втручань [1, 10]. Одними з компонентів ERAS є протоколи анестезії та мультимодальної післяопераційної аналгезії. Рекомендації ERAS (2019) при операціях у гінекології [2] включають та підтверджують однакову ефективність спінальної анестезії з ад’ювантом морфіном, блокади поперечних м’язів живота (Transversus Abdominis Plane Block, TAP-блок) та блокади квадратного м’яза попереку. Варто відзначити, що впродовж останніх років регіонарна анестезія здійснюється під контролем ультразвуку (УЗ), що сприяло вдосконаленню її традиційних технік, підвищенню рівня безпеки та впровадженню низки нових підходів, які доповнюють стратегії ERAS.
Також відомо, що інтраопераційна мультимодальна аналгезія з використанням кетаміну, пропофолу, лідокаїну (внутрішньовенно) та уникненням застосування інгаляційних анестетиків зменшує частоту хронізації болю, тоді як опіати (різної тривалості дії) можуть індукувати виникнення гіпералгезії та хронізацію болю [3]. Неадекватна післяопераційна аналгезія має наслідком біль, який у пацієнтів після гінекологічних втручань асоціюється з вищою частотою ускладнень, тривалим часом госпіталізації та більшими витратами на лікування [4]. Тому застосування неопіоїдних анальгетиків з різними, проте синергічними, механізмами дії є основою післяопераційного знеболювання в рамках концепції ERAS [2].
Отже, ефективність та універсальність регіонарних методів знеболювання в поєднанні з мультимодальным підходом до періопераційної аналгезії дозволяють використовувати їх для дедалі більшої кількості пацієнтів. Це дозволяє покращити клінічні результати лікування та знизити фінансове навантаження на систему охорони здоров’я.
Метою нашого дослідження було встановлення аналгетичної ефективності TAP-блоку як компонента післяопераційного знеболювання у пацієнтів, яким проводили тотальну абдомінальну гістеректомію. Робочою була гіпотеза, що використання TAP-блоку як додаткового компонента періопераційної мультимодальної аналгезії під час тотальної абдомінальної гістеректомії зменшує потребу в післяопераційному введенні опіоїдів, зменшує тривалість госпіталізації.
Матеріали та методи
Нами проведено ретроспективне одноцентрове дослідження у відділеннях анестезіології, інтенсивної терапії та гінекології Комунального підприємства «Рівненська обласна клінічна лікарня імені Юрія Семенюка». У дослідження було включено пацієнтів із симптомними фіброміомами, ускладненими кровотечами зі статевих шляхів, які потребували проведення тотальної абдомінальної гістеректомії (надпіхвової ампутації матки з яєчниками), віком 40–65 років. Критеріями виключення з дослідження були: відмова пацієнта від участі у дослідженні на будь-якому з його етапів, клас за Американським товариством анестезіологів (American Society of Anesthesiologists, ASA) > IV, індекс маси тіла (ІМТ) > 40 кг/м2, застосування агоністів/агоністів-антагоністів опіатних рецепторів до операції, неконтрольована артеріальна гіпертензія, порушення ритму серця.
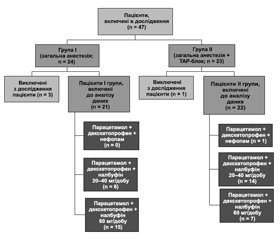
У дослідження було включено 47 пацієнтів, яких ретроспективно було розподілено на І та ІІ групи. До І групи увійшли пацієнти, в яких інтраопераційно застосовували загальну анестезію з міорелаксацією та штучною вентиляцією легень, до ІІ групи — пацієнти, в яких на додачу до загальної анестезії з міорелаксацією та штучною вентиляцією легень застосовували УЗ-асистований TAP-блок двосторонньо з латерального доступу. Для TAP-блок використовували 20 мл 0,25% розчину бупівакаїну в поєднанні з 4 мг дексаметазону з кожного боку. В ранньому післяопераційному періоді пацієнти обох груп отримували мультимодальну аналгезію парентерально: декскетопрофен (100–150 мг/добу) та парацетамол (3000 мг/добу). Крім того, пацієнти І групи впродовж 1-ї години після завершення операції отримували 20 мг налбуфіну внутрішньом’язово та в подальшому, при вираженості больового синдрому понад 5–6 балів за візуальною аналоговою шкалою (ВАШ), — по 20 мг налбуфіну що 8 годин упродовж перших 2–3 діб після операції; пацієнти ІІ групи при вираженості больового синдрому понад 5–6 балів за ВАШ отримували 20 мг налбуфіну парентерально. До аналізу даних включені 43 пацієнти (рис. 1).
/63.jpg)
Етапи дослідження: 6 годин (h6), 12 годин (h12), 24 години (h24), 48 годин (h48), 72 години (h72) після операції. В обох групах пацієнтів вивчали: рівень болю за ВАШ, частоту серцевих скорочень (ЧСС), середній артеріальний тиск (САТ), добову потребу в налбуфіні (в мг/добу), тривалість госпіталізації.
Статистичну обробку результатів дослідження проводили з допомогою MS Exсel 2017 з розрахунком частоти (%), медіани [IQR — interquartile range], середнього значення з урахуванням стандартного квадратичного відхилення (M ± σ), рівня значущості p.
Результати та обговорення
Клінічна характеристика пацієнтів, включених до аналізу даних, наведена в табл. 1. Медіана віку серед пацієнтів І групи становила 45,2 [41,3; 54,8] року, серед пацієнтів ІІ групи — 48,1 [44,2; 57,4] року. Показник медіани ІМТ серед пацієнтів І групи становив 29,3 [25,5; 36,7] кг/м2, серед пацієнтів ІІ групи — 30,5 [24,9; 38,1] кг/м2. Вірогідних відмінностей щодо віку та індексу маси тіла між І та ІІ групами пацієнтів не виявлено.
Провівши ретроспективний аналіз особливостей післяопераційного знеболювання у пацієнтів після проведення тотальної гістеректомії, ми встановили, що в І групі не було пацієнтів, які б отримували мультимодальну аналгезію за допомогою комбінації таких препаратів, як парацетамол + декскетопрофен + нефопам, тоді як у ІІ групі пацієнтів був лише 1 такий пацієнт (4,6 %). Поєднання парацетамолу, декскетопрофену та налбуфіну в дозі 20–40 мг/добу в І групі пацієнтів отримували 6 осіб, що становить 28,6 %, тоді як у ІІ групі пацієнтів — 14 осіб, що становить 63,6 % (p < 0,05). Мультимодальна післяопераційна аналгезія за допомогою парацетамолу + декскетопрофену + налбуфіну 60 мг/добу була необхідною для задовільного контролю больового синдрому в 15 пацієнтів І групи (71,4 %) та в 7 пацієнтів ІІ групи (31,8 %), p < 0,05.
/64.jpg)
При проведенні аналізу показників, що об’єктиві-зують аналгетичний компонент лікування в післяопераційному періоді, нами було встановлено, що рівень болю за ВАШ серед пацієнтів І групи досягав максимальних значень на етапах дослідження h12 та h24 та становив 4,8 [3,3; 5,8] бала та 5,3 [3,9; 6,4] бала відповідно. Ці показники мали вірогідні (p < 0,05) відмінності від рівня болю за ВАШ серед пацієнтів ІІ групи, де біль було оцінено в 2,7 [2,3; 3,5] бала та 2,1 [1,6; 4,1] бала відповідно.
Встановлено наявність вірогідних відмінностей у рівні ЧСС між І та ІІ групами пацієнтів лише на етапі дослідження h24, коли медіана цього показника для І групи становила 93 [87; 98] уд/хв порівняно з 72 [63; 79] уд/хв у ІІ групі пацієнтів (p = 0,05). Не встановлено вірогідних відмінностей середнього артеріального тиску між І та ІІ групами пацієнтів на всіх етапах дослідження, проте необхідно відзначити наявність тенденції до зниження цього показника впродовж усього дослідження серед пацієнтів І групи.
Проаналізувавши середню добову потребу в налбуфіні серед пацієнтів І та ІІ груп (табл. 3), ми виявили, що на етапі дослідження h24 була тенденція (p = 0,07) до зниження потреби в ньому серед пацієнтів ІІ групи (40,9 ± 1,1 мг/добу) порівняно з потребою серед пацієнтів І групи (51,4 ± 2,9 мг/добу).
На етапі дослідження h72 потреба в налбуфіні була вірогідно нижчою (p < 0,05) в ІІ групі порівняно з І групою та становила 5,8 ± 0,8 мг/добу порівняно з 22,5 ± 4,1 мг/добу.
Середня тривалість госпіталізації серед пацієнтів І групи становила 6,8 ± 0,5 дня, серед пацієнтів ІІ групи — 4,2 ± 0,2 дня (p < 0,05).
Опіоїд-обмежувальна мультимодальна післяопераційна аналгезія відіграє важливу роль у зниженні частоти виникнення післяопераційних ускладнень, зменшує тривалість госпіталізації, знижує частоту повторних звернень за медичною допомогою та витрати на лікування пацієнтів [2, 9]. Застосування винятково опіатів для знеболювання після гінекологічних операцій підвищує частоту виникнення нудоти та блювання, може призводити до седативного ефекту, підвищує ризик виникнення опіоїдної залежності [5, 6]. Тому уникання застосування опіоїдів, а також максимальне зниження їх дозування у межах мультимодального післяопераційного знеболювання, з більшим акцентом на неопіоїдні ліки, покращують досвід пацієнта щодо післяопераційного періоду та функціональне відновлення після операції [7].
Неопіоїдні медикаменти для знеболювання включають парацетамол (потрібно віддавати перевагу пероральним формам парацетамолу, відколи можливий даний шлях їх застосування), нестероїдні протизапальні препарати, габапентин та дексаметазон. Неопіоїдні анальгетики повинні бути препаратами першої лінії про що необхідно наголошувати пацієнтам ще на передопераційному етапі [2]. Важливим компонентом мультимодальної стратегії знеболювання є інфільтрація місця хірургічного доступу місцевим анестетиком, що дозволить знизити потребу в післяопераційному знеболюванні. Серед регіонарних методів знеболювання на сьогодні широко обговорюються епідуральна аналгезія на грудному рівні та TAP-блок. Проте ще не достатньо літературних даних, які б чітко вказували на переваги епідуральної аналгезії на грудному рівні, TAP-блоку чи інфільтрації ділянки хірургічного доступу місцевим анестетиком. Водночас УЗ-контроль, відсутність артеріальної гіпотензії та можливість ранньої мобілізації пацієнта після операції при виконанні TAP-блоку порівняно з епідуральною аналгезією роблять цю технологію безпечною та з деякими перевагами для пацієнтів. Але потреба виконувати TAP-блок білатерально однозначно підвищує дозу місцевого анестетика та ризик виникнення системної токсичності [8]. У рандомізованому дослідженні, де порівнювали епідуральну аналгезію та TAP-блок при проведенні гістеректомій, було продемонстровано зменшення тривалості госпіталізації серед пацієнтів, яким виконували TAP-блок, на 0,5 дня. Тоді як у нашому дослідженні при порівнянні загальної анестезії та післяопераційної мультимодальної аналгезії без регіонарного компонента та при виконанні TAP-блоку продемонстровано зниження тривалості госпіталізації на 2,6 дня (p < 0,05). Проте слід відзначити, що рекомендації ERAS (2019) [2] вказують на перевагу застосування інфільтрації ділянки хірургічного доступу місцевим анестетиком над TAP-блоком та епідуральною аналгезією на грудному рівні.
На додачу до регіонарного компонента аналгезії важливе значення у запобіганні виникненню болю відіграють різні групи неопіоїдних анальгетиків. За рекомендаціями ERAS (2019) [2], застосування комбінації парацетамолу та нестероїдних протизапальних препаратів має високий рівень доказовості. В нашому дослідженні було продемонстровано, що пацієнти І та ІІ груп отримували цю комбінацію. Проте значна частка пацієнтів І групи (71,4 %) потребувала призначення налбуфіну у максимальній добовій дозі, тоді як серед пацієнтів, яким виконали TAP-блок, ця частка пацієнтів була практично вдвічі меншою (31,8 %). Налбуфін є антагоністом µ-опіатних рецепторів та агоністом k-опіатних рецепторів, що дозволяє зменшити прояви або взагалі уникнути певних несприятливих ефектів агоністів µ-опіоїдних рецепторів. Застосування нефопаму як препарату, що за механізмом дії інгібує зворотне захоплення катехоламінів і серотоніну на рівні синапсів, не чинить протизапального ефекту та має антиноцицептивні властивості, було лише в 4,6 % пацієнтів ІІ групи. Цей препарат не включений у рекомендації ERAS (2019). Високий рівень доказовості згідно з ERAS (2019) [2], має інфільтрація рани місцевим анестетиком, середній рівень доказовості — епідуральна аналгезія на грудному рівні, низький рівень доказовості — TAP-блок. Однак необхідно зважати на переваги та ризики кожного з методів регіонарної анестезії в даному випадку та керуватися пацієнт-орієнтованою індивідуалізованою тактикою при виборі методу. Додавання дексаметазону як ад’юванта при виконанні регіонарної анестезії при гістеректомії дозволяє зменшувати частоту післяопераційних ускладнень (нудоти та блювання), а також, очевидно, має певний аналгетичний ефект. У дослідженні Ritva M. Jokela зі співавт. [9] продемонстровано, що додавання 15 мг дексаметазону внутрішньовенно перед індукцією в анестезію порівняно з плацебо зменшує потребу в оксикодоні в перші 24 год після виконання лапароскопічної гістеректомії. В нашому дослідженні не було виокремлено внесок кожного з компонентів аналгезії в забезпечення її ефективності, проте можна очікувати, що дексаметазон може впливати на зниження потреби в налбуфіні в післяопераційному періоді.
Висновки
Двосторонній TAP-блок 0,25% бупівакаїном та ад’ювантом дексаметазоном у пацієнтів, яким виконували тотальну гістеректомію, продемонстрував тенденцію до зниження потреби в налбуфіні в першу післяопераційну добу на 25,7 %, на третю післяопераційну добу вірогідно знизив потребу в налбуфіні в 3,9 раза (p < 0,05). Тривалість госпіталізації у пацієнтів, яким застосовували двосторонній TAP-блок, зменшувалася на 2,6 дня (p < 0,05).
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 26.09.2021
Рецензовано/Revised 12.10.2021
Прийнято до друку/Accepted 22.10.2021

/63.jpg)
/64.jpg)