Вступ
Атопічний дерматит (АД) — це багатофакторне захворювання, при якому мікробні продукти бактерій і дріжджів відіграють різноманітну роль у запуску захворювання. Дріжджові гриби Malassezia spp. є частиною нормальної мікробіоти шкіри, але було висловлено припущення, що у хворих на АД вони діють як алергени, а не як інфекційні агенти [1]. Дві низки доказів підтверджують роль Malassezia spp. у розвитку запалення й загострення АД. По-перше, як місцеві, так і системні протигрибкові засоби зменшують вираженість шкірних симптомів у сенсибілізованих до дріжджів хворих на АД [2], і, по-друге, пацієнти з AД частіше реагують на екстракт Malassezia і рекомбінантні антигени Malassezia, ніж здорові особи [3].
Дріжджі Malassezia пов’язані з лупою і себорейним дерматитом [4]. Піритіон цинку (ПЦ) є похідним піритіону (1-гідрокси-2-піридинтіону), який синтезується з протимікробного метаболіту аспергілової кислоти Aspergillus flavus. У дослідженнях продемонстровано, що ПЦ ефективний проти росту Malassezia in vitro і при випробуванні на шкірі як шампунь [5]. Вважається, що взаємодія між Malassezia та імунною системою шкіри при АД сприяє запаленню шкіри. Ці висновки стали корисними для дослідження ролі Malassezia у мікробіомі шкіри, ураженої АД, і ролі ПЦ у лікуванні АД.
ПЦ має кілька механізмів дії. По-перше, оскільки піритіон є відомим іонофором цинку, ПЦ викликає підвищення внутрішньоклітинних рівнів цинку в дріжджових клітинах [6] до такої міри, що це призводить до неправильного метилювання й клітинного стресу [7]. По-друге, ендогенні рівні міді, які можуть вивільнятися під час оновлення шкіри або постачатися імунною системою, також беруть участь у пригніченні росту [8]. Вважається, що протигрибкові ефекти виникають через реакцію позаклітинної трансхелації, яка перетворює ПЦ у піритіон міді, що призводить до внутрішньоклітинного припливу міді [8, 9]. Цей надлишок внутрішньоклітинної міді може потім інактивувати аконітазу, яка є ферментом, що бере участь у виробництві енергії грибами в мітохондріях [10]. Дослідження також показали, що ПЦ пригнічує мембранний транспорт поживних речовин, необхідних для росту дріжджів, викликаючи деполяризацію мембрани [11]. Нарешті, відносно недавні дані продемонстрували, що ПЦ у M.restricta може знижувати експресію ліпази, критичну для розпаду ліпідів, а також знижувати експресію генів для компонентів циклу Кребса (наприклад, сукцинатдегідрогенази й цитратсинтази) і ланцюга транспорту електронів (наприклад, субодиниця АТФ-синтази) [6]. Разом ці дослідження показують, що ПЦ погіршує здатність грибкових клітин асимілювати й метаболізувати поживні речовини для росту, що призводить до пригнічення росту. Відносний внесок кожного з цих механізмів у загальну активність не відомий, однак той факт, що ПЦ діє кількома шляхами, імовірно, пояснює, чому не повідомлялося про стійкість грибів до цього агента.
Метою даного дослідження було оцінити ефективність ПЦ у лікуванні АД у дітей шляхом проведення рандомізованого клінічного дослідження із застосуванням ПЦ у вигляді крему як додаткової терапії.
Матеріали та методи
Дане рандомізоване дослідження проводилося з квітня 2021 року по січень 2022 року в МЦ «Алерголог», м. Київ. У дослідження включені 62 хворих на АД віком 2–18 років. Хворі мали ступінь тяжкості за шкалою SCORAD (SCORing for Atopic Dermatitis — шкала для оцінки атопічного дерматиту) від 10 до 70 балів. Критеріями включення були такі: тривалість АД понад 2 роки; ступінь тяжкості за шкалою SCORAD 10–70 балів. Критерії виключення були такими: лікування системними кортикостероїдами протягом останніх 4 тижнів, лікування місцевими або системними протигрибковими препаратами будь-якого іншого дерматологічного захворювання протягом останніх 4 тижнів, тяжкі системні захворювання або злоякісні пухлини. Зібрані демографічні, клінічні й серологічні дані, що включали вік пацієнта, стать, локалізацію АД на голові й шиї, загальні рівні IgE в сироватці, рівні IgE для Malassezia (табл. 1).
/9.jpg)
Пацієнтів випадковим чином було розподілено на дві групи: групу, що отримувала крем з ПЦ, і контрольну групу. Пацієнти основної групи отримували лікування кремом 0,2% ПЦ (1 г крему містить 2 мг ПЦ) на уражені ділянки шкіри 2 рази на день і необхідними симптоматичними засобами. Діти контрольної групи отримували лише симптоматичну терапію. Термін лікування становив 3 тижні. До і після лікування реєстрували показник SCORAD, протягом дослідження реєструвались побічні ефекти.
Проведене дослідження відповідало етичним стандартам Гельсінської декларації 1975 року і було схвалене етичною комісією НМУ імені О.О. Богомольця. Усі учасники/батьки дітей, включених до дослідження, дали інформовану згоду.
Специфічний IgE до суміші Malassezia (m227) (Malassezia sympodialis, Malassezia globosa і Malassezia restricta) аналізували в 31 хворого основної групи. Зразки сироватки пацієнтів відбирали під час відвідувань і зберігали при –20 °C перед аналізом. Усі зразки разом аналізували на рівень загального IgE і специфічного IgE до Malassezia spp. (m227) за допомогою імунохемілюмінесцентного методу на ImmunoCAP 100 (Thermo Fisher Scientific Inc., Фадія, Швеція). Клас 1 або вище був визначений як позитивний.
Залежно від ступеня тяжкості АД хворі основної групи отримували симптоматичну терапію — левоцетиризину гідрохлорид і топічно крем бетаметазон дипропіонат, як у контрольній групі. Діти контрольної групи отримували лише левоцетиризину гідрохлорид і місцеве застосування емолієнту й крему бетаметазону дипропіонату (1 г крему містить 0,64 мг бетаметазону дипропіонату) на уражені ділянки шкіри на 7–14 днів.
Статистичну обробку отриманих даних проводили за допомогою статистичного пакета IBM SPSS Statistics Base (версія 22) і програмного забезпечення EZR, версія 1.32 (графічний інтерфейс середовища R, версія 2.13.0). Базу даних дослідження було систематизовано в редакторі Microsoft Excel. Відмінність в ефективності терапії між двома підгрупами визначалась за допомогою Т-критерію Вілкоксона в кожній підгрупі до і після лікування, а вплив наявності сенсибілізації до Malassezia на ефективність терапії — за допомогою W-критерію Вілкоксона, відмінність вважалася статистично значущою на рівні p < 0,05.
Результати
62 хворі віком від 2 до 18 років (середній вік 7,7 ± 4,8 року) були включені в дослідження й рандомним шляхом розподілені на дві групи: 31 хворий отримував лікування кремом ПЦ (основна група) і 31 — отримував традиційну терапію (контрольна група). Не було значущих відмінностей між двома групами за віком, співвідношенням статей, тривалістю й тяжкістю захворювання (p > 0,05; табл. 1). Дві групи відрізнялися між собою за рівнем загального IgE — вищі показники були в основній (W = 753,5; p = 0,002). Усі хворі основної і контрольної груп завершили дослідження. Серед пацієнтів основної групи повідомлялося про наступні побічні ефекти: 4 хворі відмічали підвищену сухість шкіри, імовірно, пов’язану з лікуванням. Симптоми легко піддавались лікуванню емолієнтами.
31 дитині основної групи було визначено специфічний IgE до суміші Malassezia (m227), серед них 12 дітей (38,7 %) мали позитивний результат: троє дітей мали 1-й клас сенсибілізації, 1 дитина — 2-й клас, 4 хворих — 3-й клас, 4 дитини — 5-й клас сенсибілізації. 19 (61,3 %) дітей мали негативний показник специфічного IgE до Malassezia.
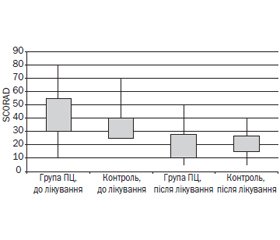
У групі дітей, що отримували додатково до традиційної терапії ПЦ, покращення показника SCORAD становило 45 % (T-W = 496,0; p < 0,001). У групі контролю також спостерігалось покращення показника SCORAD — 35,2 % (T-W = 496,0; p < 0,001). Але при порівнянні ефективності лікування у двох групах було виявлено, що діти, хворі на АД, які приймали ПЦ місцево, мали статистично вірогідно кращу динаміку показника SCORAD, ніж діти контрольної групи: середнє значення ΔSCORAD в основній групі становило 17,9, у контрольній — 12,6 (W = 782,5; p = 0,006) (рис. 1).
Ми вирішили дослідити, чи впливала наявність сенсибілізації до Malassezia на ефективність терапії. За допомогою W-критерію Вілкоксона ми порівняли різницю показника SCORAD до і після лікування (ΔSCORAD) у групі дітей із сенсибілізацією і без неї (рис. 2). Вірогідної різниці залежно від наявності сенсибілізації до Malassezia не було (W = 179,0; p = 0,597).
Жоден пацієнт не потребував госпіталізації або не виключився з дослідження через несприятливі події від лікування, не повідомляв про серйозні системні побічні ефекти.
Обговорення
Шкіра є найбільш значимим зовнішнім бар’єром і колонізується великою кількістю мікроорганізмів. У хворих на АД можє розвиватися сенсибілізація до дріжджів Malassezia. Окрім того, існує багато інших механізмів, завдяки яким Malassezia погіршує стан при АД. Протигрибкове лікування призводить до покращення шкірних симптомів, що може бути наслідком вимирання грибкових алергенів.
У даному дослідженні було вивчено ефективність застосування ПЦ як додаткової терапії в дітей, хворих на АД. У групі дітей, які отримували ПЦ, покращення показника SCORAD становило 45 % (T-W = 496,0; p < 0,001), у контрольній групі — 35,2 % (T-W = 496,0; p < 0,001). Але хворі на АД, які приймали ПЦ місцево, мали статистично вірогідно кращу динаміку показника SCORAD, ніж діти контрольної групи: середнє значення ΔSCORAD в основній групі становило 17,9, у контрольній — 12,6 (W = 782,5, p = 0,006).
У групі дітей, що отримували ПЦ, ми дослідили специфічний IgE до Malassezia: 12 дітей (38,7 %) мали позитивний результат, 19 (61,3 %) дітей мали негативний показник специфічного IgE до Malassezia. Ми не виявили впливу наявності сенсибілізації до Malassezia на ефективність терапії ПЦ (W = 179,0; p = 0,597). Це може бути пов’язано з тим, що вплив Malassezia на тяжкість АД не обмежується лише сенсибілізацією, дріжджові гриби справляють пошкоджуючий вплив на кератиноцити, і протигрибкова терапія, направлена на зменшення грибкового навантаження, приводить до покращення стану шкіри.
Результати попередніх досліджень підтверджують протигрибкову ефективність ПЦ як засобу від лупи. Malassezia restricta і Malassezia globosa — це ліпідозалежні коменсальні дріжджі, пов’язані з лупою. М. Park et al. у своєму дослідженні спробували зрозуміти механізм дії ПЦ проти M.restricta, використовуючи біохімічний і транскриптомний аналіз, і виявили, що ПЦ в основному викликає токсичність цинку і мітохондріальну дисфункцію [6]. Крім того, дані дозволяють припустити, що ПЦ зменшує експресію ліпаз, що може відігравати важливу роль у виживанні M.restricta на шкірі голови хворих на лупу [6]. Цей транскрипційний аналіз показав, що ПЦ інгібує синтез кластерів Fe-S у M.restricta, — результат, подібний до отриманого для клітин, оброблених ПЦ S.cerevisiae [8, 12]. Синтез кластера Fe-S є одним з основних метаболічних процесів заліза, що відбувається в мітохондріях, а підвищення рівня клітинного цинку у відповідь на лікування ПЦ може бути основною причиною гальмування синтезу кластера Fe-S у M.restricta.
У недавньому дослідженні C. Leong і співавт. оцінювали ефективність протигрибкових засобів лікування проти Malassezia на шкірі голови за допомогою комбінації культурологічних і геномних методів виявлення. ПЦ пригнічував ріст Malassezia при низьких мінімальних інгібуючих концентраціях. У поздовжньому пілотному дослідженні кількісний аналіз ПЛР показав зменшення M.restricta на шкірі голови після лікування ПЦ [5].
Незважаючи на значну кількість досліджень щодо вивчення ефективності ПЦ у вигляді шампуню для лікування себорейного дерматиту й лупи [13–15], даних щодо ефективності лікування АД препаратами ПЦ у вигляді крему бракує. Більш рандомізовані плацебо-контрольовані дослідження для великих груп пацієнтів потрібні для надійної оцінки переваг протигрибкової терапії при АД. Також не було достатньо вивчено ефективність різних схем протигрибкової терапії в дітей з АД, зокрема без застосування топічних протизапальних препаратів. Використання сучасних схем терапії АД у дітей не забезпечує тривалої ремісії, а застосування протизапальних препаратів пов’язане з низкою тяжких і небезпечних побічних ефектів, і залишається необхідність персоналізованого підходу до терапії з урахуванням обтяжуючих факторів і тригерів АД.
Як підсумок: протигрибкова терапія демонструє позитивний ефект у деяких пацієнтів. Однак патогенетичний механізм і взаємодія між Malassezia spp. і AД досі частково залишаються незрозумілими і потребують подальшого дослідження.
Висновки
Дане дослідження продемонструвало ефективність застосування ПЦ у лікуванні АД як додаткової терапії: хворі на АД, які приймали ПЦ місцево, мали статистично вірогідно кращу динаміку показника SCORAD, ніж діти, які отримували тільки традиційну терапію. Значення дріжджів Malassezia при АД зараз широко вивчається, і потрібні ще дослідження, щоб зрозуміти точну роль цих організмів у перебігу захворювання і роль протигрибкових препаратів у лікуванні АД.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 05.07.2022
Рецензовано/Revised 15.07.2022
Прийнято до друку/Accepted 23.07.2022
Список литературы
1. Волосовець О.П., Кривопустов С.П., Мозирська О.В. Роль мікробіому шкіри в розвитку атопічного дерматиту в дітей. Здоров’я дитини. 2021. Т. 16. № 3. doi: https://doi.org/10.22141/2224-0551.16.3.2021.233911.
2. Navarro-Triviño F.J., Ayén-Rodríguez Á. Study of Hypersensitivity to Malassezia furfur in Patients with Atopic Dermatitis with Head and Neck Pattern: Is It Useful as a Biomarker and Therapeutic Indicator in These Patients? Life (Basel). 2022 Feb 16. 12(2). 299. doi: 10.3390/life12020299. PMID: 35207586; PMCID: PMC8876740.
3. Sonesson A., Bartosik J., Christiansen J., Roscher I., Nilsson F., Schmidtchen A., Bäck O. Sensitization to skin-associated microorganisms in adult patients with atopic dermatitis is of importance for disease severity. Acta Derm. Venereol. 2013 May. 93(3). 340-5. doi: 10.2340/00015555-1465. PMID: 23073977.
4. Prohic A., Jovovic Sadikovic T., Krupalija-Fazlic M., Kuskunovic-Vlahovljak S. Malassezia species in healthy skin and in dermatological conditions. Int. J. Dermatol. 2016 May. 55(5). 494-504. doi: 10.1111/ijd.13116. Epub 2015 Dec 29. PMID: 26710919.
5. Leong C., Wang J., Toi M.J., Lam Y.I., Goh J.P., Lee S.M., Dawson T.L. Effect of zinc pyrithione shampoo treatment on skin commensal Malassezia. Medical mycology. 2021. 59(2), 210-213. https://doi.org/10.1093/mmy/myaa068.
6. Park M., Cho Y.J., Lee Y.W., Jung W.H. Understanding the Mechanism of Action of the Anti-Dandruff Agent Zinc Pyrithione against Malassezia restricta. Sci Rep. 2018 Aug 14. 8(1). 12086. doi: 10.1038/s41598-018-30588-2. PMID: 30108245; PMCID: PMC6092343.
7. Pierrel F., Cobine P.A., Winge D.R. Metal Ion availability in mitochondria. Biometals. 2007. 20. 675-682. doi: 10.1007/s10534-006-9052-9.
8. Reeder N.L., Kaplan J., Xu J., Youngquist R.S., Wallace J., Hu P. et al. Zinc pyrithione inhibits yeast growth through copper influx and inactivation of iron-sulfur proteins. Antimicrob. Agents Chemother. 2011 Dec. 55(12). 5753-60. doi: 10.1128/AAC.00724-11. Epub 2011 Sep 26. PMID: 21947398; PMCID: PMC3232817.
9. Reeder N., Xu J., Youngquist R., Schwartz J., Rust R., Saunders C. The antifungal mechanism of action of zinc pyrithione. Br. J. Dermatol. 2011. 165. 9-12. doi: 10.1111/j.1365-2133.2011.10571.x.
10. Gelling C., Dawes I.W., Richhardt N., Lill R., Mühlenhoff U. Mitochondrial Iba57p Is Required for Fe/S Cluster Formation on Aconitase and Activation of Radical SAM Enzymes. Mol. Cell. Biol. 2008. 28. 1851-1861. doi: 10.1128/MCB.01963-07.
11. Mangion S.E., Holmes A.M., Roberts M.S. Targeted Delivery of Zinc Pyrithione to Skin Epithelia. Int. J. Mol. Sci. 2021 Sep 8. 22(18). 9730. doi: 10.3390/ijms22189730. PMID: 34575891; PMCID: PMC8465279.
12. Yasokawa D., Murata S.M., Iwahashi Y., Kitagawa E., Kishi K., Okumura Y., Iwahashi H. DNA microarray analysis suggests that zinc pyrithione causes iron starvation to the yeast Saccharomyces cerevisiae. Journal of Bioscience and Bioengineering. 2010. 109. 5. 479-86 .
13. Piérard-Franchimont C., Goffin V., Decroix J., Piérard G.E. A multicenter randomized trial of ketoconazole 2% and zinc pyrithione 1% shampoos in severe dandruff and seborrheic dermatitis. Skin Pharmacol. Appl. Skin Physiol. 2002 Nov-Dec. 15(6). 434-41. doi: 10.1159/000066452. PMID: 12476017.
14. Schwartz J.R., Bacon R.A., Shah R., Mizoguchi H., Tosti A. Therapeutic efficacy of anti-dandruff shampoos: a randomized clinical trial comparing products based on potentiated zinc pyrithione and zinc pyrithione/climbazole. Int. J. Cosmet. Sci. 2013 Aug. 35(4). 381-7. doi: 10.1111/ics.12055. Epub 2013 May 24. PMID: 23614401.
15. Schwartz J.R. Zinc Pyrithione: A Topical Antimicrobial With Complex Pharmaceutics. J. Drugs Dermatol. 2016 Feb. 15(2). 140-4. PMID: 26885780.

/9.jpg)
/10.jpg)