Журнал «Почки» Том 11, №4, 2022
Вернуться к номеру
Використання препарату Пембіна Блю в лікуванні й профілактиці рецидивуючих інфекцій нижніх сечовивідних шляхів у жінок
Авторы: Возіанов О.С. (1), Іванов Д.Д. (2)
(1) — ДУ «Інститут урології імені академіка О.Ф. Возіанова НАМН України», м. Київ, Україна
(2) — Національний університет охорони здоров’я України ім. П.Л. Шупика, м. Київ, Україна
Рубрики: Нефрология
Разделы: Клинические исследования
Версия для печати
Мета дослідження: проаналізувати ефективність, безпечність і переносимість використання препарату Пембіна Блю з метою лікування й профілактики загострень рецидивуючих інфекцій нижніх сечовивідних шляхів у жінок. Матеріали та методи. Було проведено відкрите моноцентрове порівняльне дослідження, у якому взяли участь 50 жінок віком від 20 до 75 років з рецидивуючими інфекціями нижніх сечовивідних шляхів. З метою лікування хворим було призначено препарат Пембіна Блю по 1 капсулі 2 рази на добу протягом 10 днів як монотерапія. При дослідженні бралися до уваги об’єктивні зміни показників загального аналізу сечі (фізико-хімічні властивості сечі й мікроскопічне дослідження), а також суб’єктивні зміни клінічних проявів захворювання й переносимості ліків (згідно з розробленими анкетами-опитувальниками). Дані для аналізу були отримані на 1-шу й 7-му добу проведеного лікування. Результати. Проведене дослідження продемонструвало, що застосування препарату Пембіна Блю курсом від 7 днів дає значний антибактеріальний, спазмолітичний і знеболюючий ефект. Препарат може використовуватись як монозасіб або в комплексному лікуванні з метою підкислення сечі й показує кращі результати у хворих із початковим показником рН сечі ≥ 7. Пембіна Блю не має побічної дії, добре переноситься хворими, що дозволяє рекомендувати його для широкого застосування в лікуванні й профілактиці рецидивуючих інфекцій нижніх сечовивідних шляхів у жінок. Висновки. Проведене дослідження продемонструвало, що застосування препарату Пембіна Блю як монозасобу має високу ефективність при низькому рівні побічної дії, що дозволяє рекомендувати його для застосування у хворих на рецидивуючі інфекції нижніх сечовивідних шляхів.
The purpose of the study: to analyze the effectiveness, safety and tolerability of Pembina Blue for the treatment and prevention of exacerbations of recurrent lower urinary tract infections in women. Materials and methods. An open-label, single-center, comparative study was conducted in 50 women aged 20 to 75 years with recurrent lower urinary tract infections. For the purpose of treatment, the patients were prescribed Pembina Blue 1 capsule 2 times a day for 10 days as monotherapy. The study took into account objective changes in general urinalysis indicators (physicochemical properties of urine and microscopic examination), as well as subjective changes in clinical manifestations of the disease and drug tolerance (according to developed questionnaires). Data for analysis were obtained on days 1 and 7 of the treatment. Results. The conducted study demonstrated that the use of Pembina Blue for a course of 7 days provides a significant antibacterial, antispasmodic and pain-relieving effect. The drug can be used as a monotherapy or in combination treatment to acidify urine and shows better results in patients with initial urine pH ≥ 7. Pembina Blue has no side effects, is well tolerated by patients, which allows us to recommend it for a wide use in the treatment and prevention of recurrent lower urinary tract infections in women. Conclusions. The conducted study demonstrated that the use of Pembina Blue as a monotherapy has high efficiency with a low level of side effects, which allows recommending it for use in patients with recurrent lower urinary tract infections.
рецидивуючі інфекції нижніх сечовивідних шляхів; Пембіна Блю; лікування; профілактика
recurrent lower urinary tract infections; Pembina Blue; treatment; prevention
Вступ
Матеріали та методи
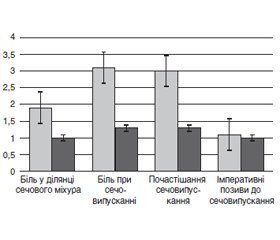
Результати та обговорення
/28.jpg)
Висновки
- Horan T.C. et al. CDC/NHSN surveillance definition of health care-associated infection and criteria for specific types of infections in the acute care setting. Am. J. Infect. Control. 2008. 36. 309. https://pubmed.ncbi.nlm.nih.gov/18538699.
- Johansen T.E. et al. Critical review of current definitions of urinary tract infections and proposal of an EAU/ESIU classification system. Int. J. Antimicrob. Agents. 2011. 38. Suppl. 64. https://pubmed.ncbi.nlm.nih.gov/22018988.
- Пасечников С.П., Мітченко М.В. Неспецифічний цистит: сучасні принципи діагностики та лікування. Здоров’я України 21 сторіччя. 2017. № 8(405). С. 50-51.
- Bonkat G., Pickard R., Bartoletti R. et al. Guidelines EAU: Guidelines on urological infections. 2017. 106 p.
- Wagenlehner F.M. et al. Uncomplicated urinary tract infections. Dtsch Arztebl. Int. 2011. 108. 415. https://pubmed.ncbi.nlm.nih.gov/21776311.
- Stamm W.E. et al. Management of urinary tract infections in adults. N. Engl. J. Med. 1993. 329. 1328. https://pubmed.ncbi.nlm.nih.gov/8413414.
- Bradbury S.M. Collection of urine specimens in general practice: to clean or not to clean? J. R. Coll. Gen. Pract. 1988. 38. 363. https://pubmed.ncbi.nlm.nih.gov/3256648.
- Lifshitz E. et al. Outpatient urine culture: does collection technique matter? Arch. Intern. Med. 2000. 160. 2537. https://pubmed.ncbi.nlm.nih.gov/10979067.
- Fihn S.D. Clinical practice. Acute uncomplicated urinary tract infection in women. N. Engl. J. Med. 2003. 349. 259. https://pubmed.ncbi.nlm.nih.gov/12867610.
- Foxman B. et al. Epidemiology of urinary tract infections: transmission and risk factors, incidence, and costs. Infect. Dis. Clin. North Am. 2003. 17. 227. https://pubmed.ncbi.nlm.nih.gov/12848468.
- Hooton T.M. Recurrent urinary tract infection in women. Int. J. Antimicrob. Agents. 2001. 17. 259. https://pubmed.ncbi.nlm.nih.gov/11295405.
- Hooton T.M. et al. Effect of Increased Daily Water Intake in Premenopausal Women with Recurrent Urinary Tract Infections: A Randomized Clinical Trial. JAMA Intern. Med. 2018. 178. 1509. https://pubmed.ncbi.nlm.nih.gov/30285042.
- Chen Y.Y. et al. Estrogen for the prevention of recurrent urinary tract infections in postmenopausal women: a meta-analysis of randomized controlled trials. Int. Urogynecol. J. 2021. 32. 17. https://pubmed.ncbi.nlm.nih.gov/32564121.
- Duenas-Garcia O.F. et al. Pharmacological agents to decrease new episodes of recurrent lower urinary tract infections in postmenopausal women. A systematic review. Female Pelvic Med. Reconstruct. Surg. 2016. 22. 63. https://pubmed.ncbi.nlm.nih.gov/26825411.
- Beerepoot M.A.J. et al. Nonantibiotic prophylaxis for recurrent urinary tract infections: A systematic review and meta-analysis of randomized controlled trials. J. Urol. 2013. 190. 1981. https://pubmed.ncbi.nlm.nih.gov/23867306.
- Naber K.G. et al. Immunoactive prophylaxis of recurrent urinary tract infections: a meta-analysis. Int. J. Antimicrob. Agents. 2009. 33. 111. https://pubmed.ncbi.nlm.nih.gov/18963856.
- Canales J. et al. Are probiotics effective in preventing urinary tract infection? Medwave. 2018. 18. e7186. https://pubmed.ncbi.nlm.nih.gov/29624569.
- Grin P.M. et al. Lactobacillus for preventing recurrent urinary tract infections in women: meta-analysis. Can. J. Urol. 2013. 20. 6607. https://pubmed.ncbi.nlm.nih.gov/23433130.
- Lenger S.M. et al. D-mannose vs other agents for recurrent urinary tract infection prevention in adult women: a systematic review and meta-analysis. Am. J. Obstet. Gynecol. 2020. 223. 265. https://pubmed.ncbi.nlm.nih.gov/32497610.
- Fu Z. et al. Cranberry Reduces the Risk of Urinary Tract Infection Recurrence in Otherwise Healthy Women: A Systematic Review and Meta-Analysis. J. Nutr. 2017. 147. 2282. https://pubmed.ncbi.nlm.nih.gov/29046404.
- Wang C.H. et al. Cranberry-containing products for prevention of urinary tract infections in susceptible populations: a systematic review and meta-analysis of randomized controlled trials. Arch. Intern. Med. 2012. 172. 988. https://pubmed.ncbi.nlm.nih.gov/22777630.
- Ansari M.A., Fatima Z., Hameed S. Antifungal action of methylene blue involves mitochondrial dysfunction and disruption of redox and membrane homeostasis in C.аlbicans. The Open Microbio–logy Journal. 2016. Vol. 10. Р. 12-22. https://pubmed.ncbi.nlm.nih.gov/27006725.
- Nalliah S. et al. The use of chemotherapeutic agents as prophylaxis for recurrent urinary tract infection in healthy nonpregnant women: A network meta-Analysis. Indian J. Urol. 2019. 35. 147. https://pubmed.ncbi.nlm.nih.gov/31000921.
- Ahmed H. et al. Long-term antibiotics for prevention of recurrent urinary tract infection in older adults: Systematic review and meta-analysis of randomised trials. BMJ Open. 2017. 7. e015233. https://pubmed.ncbi.nlm.nih.gov/28554926.
- Rudenko N. et al. Prevention of recurrent lower urinary tract infections by long-term administration of fosfomycin trometamol: Double blind, randomized, parallel group, placebo controlled study. Arzneimittel-Forschung/Drug Research. 2005. 55. 420. https://pubmed.ncbi.nlm.nih.gov/16080282.