Журнал «Медицина неотложных состояний» Том 19, №4, 2023
Вернуться к номеру
Антибіотикотерапія при вогнепальній бойовій травмі: вісім років по тому (ретроспективне обсерваційне дослідження)
Авторы: Кріштафор Д.А. (1), Кріштафор А.А. (1), Галущак А.Я. (2), Минка В.Ю. (2), Селезньова У.В. (2), Грабова Г.Ю. (3)
(1) — Дніпровський державний медичний університет, м. Дніпро, Україна
(2) — Дніпропетровська обласна клінічна лікарня ім. І.І. Мечникова, м. Дніпро, Україна
(3) — Інститут мікробіології і вірусології ім. Д.К. Заболотного НАН України, м. Київ, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
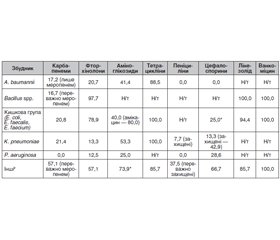
Актуальність. Для вогнепальних бойових поранень характерні масивна деструкція тканин і значне забруднення. Інфекційні ускладнення є причиною смерті 80 % поранених, які померли у пізні терміни після бойової травми. Тому боротьба з рановою інфекцією є одним із пріоритетних завдань у лікуванні бойової травми. Мета дослідження: визначити зміни у складі бактеріальної мікрофлори вогнепальних бойових поранень та її чутливості до антибактеріальних препаратів між 2014 та 2022 роками. Матеріали та методи. Нами обстежено 167 поранених із вогнепальною бойовою травмою, з них 29 надійшли 2014 року, а 138 — 2022 року. За результатами бактеріологічних досліджень ран, виконаних при надходженні поранених до стаціонару ІІІ рівня, ми вивчали частоту колонізації ран, характер колонізації (контамінація/інфікування), характер виявленої мікрофлори та її чутливість до антибактеріальних препаратів. Результати. Із виконаних бактеріологічних досліджень 2014 року не виявлено росту у 27,6 %, 2022 року — 41,3 % (p = 0,168). Серед позитивних результатів у 2014 році відповідали критеріям інфікування (≥104 колонієутворюючих одиниць, КУО) 30,8 % збудників, у 2022 році — 63,8 % (p < 0,001). 2014 року серед збудників переважали A. baumannii (21,4 %), S. haemolyticus (19,0 %), бактерії кишкової групи (19,0 %) та P. aeruginosa (11,9 %). 2022 року найчастіше виявлялися Bacillus spp. (28,4 %), A. baumannii (19,6 %), бактерії кишкової групи (14,2 %) та K. pneumoniae (10,1 %). При цьому у 71,1 % випадків виділення Bacillus spp. кількість бактерій відповідала критеріям інфікування. Загальна чутливість у 2014 та 2022 роках склала відповідно: до карбапенемів — 33,3–35,7 та 6,4–23,2 % (p < 0,05); до цефалоспоринів — 18,8–61,5 та 8,3–46,7 %; до фторхінолонів — 15,4–44,4 та 31,3–87,1 % (p < 0,05); до пеніцилінів — 0,0–12,5 та 5,3–66,7 % (p < 0,05); до аміноглікозидів — 22,2–50,0 та 33,3–46,3 %; до ванкоміцину та доксицикліну — 64,7 та 100,0 %; до кліндаміцину — 27,3 та 94,3 % (p < 0,05); до тайгецикліну — 90,0 та 94,4 %; до лінезоліду — 91,7 та 97,1 %. Чутливість Bacillus spp. до фторхінолонів, лінезоліду та ванкоміцину складала 97,7–100,0 %, до карбапенемів — 16,7 %. Висновки. Порівняно з 2014 роком у 2022-му частота контамінації ран зменшилася, а серед ранової мікрофлори почали домінувати Bacillus spp. Це може пояснюватися широким застосуванням для обробки ран пробіотичних спреїв. Утім, зважаючи на велику кількість КУО Bacillus spp. та розвинення ними стійкості до деяких груп препаратів (як-от карбапенеми), ефективність застосування цих спреїв потребує подальшого вивчення. Загальна чутливість збудників до карбапенемів та цефалоспоринів знизилася, до фторхінолонів та аміноглікозидів — підвищилася; високою залишається чутливість до препаратів резерву (тайгециклін, доксициклін, ванкоміцин, лінезолід), дуже низькою — до пеніцилінів. Це ще раз підкреслює необхідність диференційованого підходу до антибактеріальної терапії та подальших досліджень у цьому напрямку.
Background. Combat gunshot wounds are characterized by massive tissue destruction and significant contamination. Infectious complications are the cause of death of 80 % victims who died late after a combat injury. Therefore, the fight against wound infection is one of the priority tasks in the treatment of combat trauma. The purpose of our study was to determine the changes in the composition of the bacterial microflora of combat gunshot wounds and its sensitivity to antibacterial drugs between 2014 and 2022. Materials and methods. We examined 167 patients with gunshot combat injuries, of which 29 were admitted in 2014, and 138 in 2022. Based on the results of bacteriological examinations of wounds performed upon admission to a third-level hospital, we studied the frequency of wounds colonization, its nature (contamination/infection), the nature of the identified microflora and its sensitivity to antibacterial drugs. Results. Of the bacteriological studies performed in 2014, no growth was found in 27.6 % of cases, in 2022 — in 41.3 % (p = 0.168). Among the positive results in 2014, 30.8 % of pathogens met the criteria for infection (≥ 104 colony-forming units; in 2022, 63.8 % (p < 0.001). In 2014, A.baumannii (21.4 %), S.haemolyticus (19.0 %), gut bacteria (19.0 %) and P.aeruginosa (11.9 %) prevailed among pathogens. In 2022, the Bacillus spp. (28.4 %), A.baumannii (19.6 %), gut bacteria (14.2 %) and K.pneumoniae (10.1 %) were detected most frequently. At the same time, in 71.1 % of cases, the number of Bacillus spp. bacteria met the criteria for infection. The overall sensitivity in 2014 and 2022, respectively, was: to carbapenems — 33.3–35.7 and 6.4–23.2 % (p < 0.05); to cephalosporins — 18.8–61.5 and 8.3–46.7 %; to fluoroquinolones — 15.4–44.4 and 31.3–87.1 % (p < 0.05); to penicillins — 0.0–12.5 and 5.3–66.7 % (p < 0.05); to aminoglycosides — 22.2–50.0 and 33.3–46.3 %; to vancomycin and doxycycline — 64.7 and 100.0 %, to clindamycin — 27.3 and 94.3 % (p < 0.05), to tigecycline — 90.0 and 94.4 %, to linezolid — 91.7 and 97.1 %. Bacillus spp. was sensible to fluoroquinolones, linezolid and vancomycin in 97.7–100.0 % cases, to carbapenems — in 16.7 %. Conclusions. Compared to 2014, the frequency of wound contamination in 2022 decreased, and Bacillus spp. began to dominate among the wound microflora. This is probably due to the widespread use of probiotic sprays for the treatment of wounds. However, given the large number of Bacillus spp. colony-forming units and development of their resistance to some groups of drugs (such as carbapenems), the effectiveness of these sprays requires further study. The general sensitivity of pathogens to carbapenems and cephalosporins decreased, to fluoroquinolones and aminoglycosides — increased; sensitivity to reserve drugs (tigecycline, doxycycline, vancomycin, linezolid) remains high, to penicillins — very low. This once again emphasizes the need for a differentiated approach to antibacterial therapy and further research in this direction.
вогнепальні бойові поранення; антибактеріальні препарати; антибіотики; чутливість
gunshot combat wounds; antibacterial drugs; antibio-tics; sensitivity
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Office of the United Nations High Commissioner for Human Rights. Report on the human rights situation in Ukraine: 1 August 2021 to 31 January 2022. URL: https://www.ohchr.org/en/documents/country-reports/report-human-rights-situation-ukraine-1-august-2021-31-january-2022.
- Патрульна поліція України. Статистика ДТП в Україні за період з 01.01.2021 по 31.12.2021. URL: https://patrolpolice.gov.ua/statystyka/.
- Office of the United Nations High Commissioner for Human Rights. Ukraine: civilian casualty update 22 May 2023. URL: https://www.ohchr.org/en/news/2023/05/ukraine-civilian-casualty-update-22-may-2023.
- Bhandari P.S., Maurya S., Mukherjee M.K. Reconstructive challenges in war wounds. Indian J. Plast. Surg. 2012. Vol. 45(2). P. 332-339. doi: 10.4103/0970-0358.101316.
- Йовенко І.О., Кобеляцький Ю.Ю., Царьов О.В. та ін. Практика інфузійно-трансфузійної терапії кровотеч при тяжкій вогнепальній травмі: питання вибору препаратів та цільових кінцевих точок. Медицина невідкладних станів. 2015. № 2(65). С. 164-170. doi: 10.22141/2224-0586.2.65.2015.79500.
- Gray R. War wounds: basic surgical management. Geneva, Switzerland, 1994. 48 p.
- Weintrob A.C., Murray C.K., Xu J. et al. Early Infections Complicating the Care of Combat Casualties from Iraq and Afghanistan. Surg. Infect. (Larchmt). 2018. Vol. 19(3). P. 286-297. doi: 10.1089/sur.2017.240.
- Yun H.C., Blyth D.M., Murray C.K. Infectious Complications After Battlefield Injuries: Epidemiology, Prevention, and Treatment. Curr. Trauma Rep. 2017. Vol. 3. P. 315-323. doi: 10.1007/s40719-017-0102-2.
- Клінічний протокол надання медичної допомоги хворим із відкритими пошкодженнями хребта та спинного мозку. Затверджений Наказом МОЗ № 317 від 13.06.2008 «Про затвердження клінічних протоколів надання медичної допомоги за спеціальністю «Нейрохірургія». Київ, 2008. URL: https://zakon.rada.gov.ua/rada/show/v0317282-08#Text.
- Протокол надання медичної допомоги хворим із збройними непроникаючими пораненнями голови мирного часу. Наказ МОЗ № 245 від 25.04.2006 «Про затвердження протоколів надання медичної допомоги за спеціальністю «Нейрохірургія». Київ, 2006. URL: https://zakononline.com.ua/documents/show/87829___679328.
- Emergency War Surgery. Fourth United States Revision. Еd. by M.A. Cubano. San-Antonio, 2013. 589 p.
- Йовенко І.О., Кріштафор Д.А., Кобеляцький Ю.Ю. та ін. Бактеріальний контроль при тяжкій вогнепальній травмі. Медицина невідкладних станів. 2015. № 2. С. 171-175. doi: 10.22141/2224-0586.2.65.2015.79515.
- Emergency War Surgery. Fifth United States Revision. Еd. by M.A. Cubano. San-Antonio, 2018. 605 p.
- Кріштафор Д.А., Йовенко І.О., Кріштафор А.А., Минка В.Ю. Антибіотикотерапія при вогнепальній бойовій травмі: ретроспективне обсерваційне дослідження. Гострі та невідкладні стани у практиці лікаря. 2015. № 2. С. 47-50.
- Peacock J.L., Peacock P.L. Oxford Hadbook of Medical Statistics (2nd ed.) Oxford University Press, UK, 2020. 640 p. doi: 10.1093/med/9780198743583.001.0001.
- Almasaudi S.B. Acinetobacter spp. as nosocomial pathogens: Epidemiology and resistance features. Saudi J. Biol. Sci. 2018. Vol. 25(3). P. 586-596. doi: 10.1016/j.sjbs.2016.02.009.
- Haque M.A., Wang F., Chen Y. et al. Bacillus spp. Contamination: A Novel Risk Originated from Animal Feed to Human Food Chains in South-Eastern Bangladesh. Front. Microbiol. 2022. Vol. 12. Article No. 783103. doi: 10.3389/fmicb.2021.783103.
- Turnbull P.C.B. Bacillus. In: Baron S., editor. Medical Microbiology. 4th edition. Galveston (TX): University of Texas Medical Branch at Galveston, 1996. Chapter 15. URL: https://www.ncbi.nlm.nih.gov/books/NBK7699/.
- Alou M.T., Rathored J., Khelaifia S. et al. Bacillus rubiinfantis sp. nov. strain mt2T, a new bacterial species isolated from human gut. New Microbes New Infect. 2015. Vol. 8. P. 51-60. 10.1016/j.nmni.2015.09.008.
- Kotb E. Purification and partial characterization of serine fibrinolytic enzyme from Bacillus megaterium KSK-07 isolated from kishk, a traditional Egyptian fermented food. Appl. Biochem. Microbiol. 2015. Vol. 51. P. 34-43. doi: 10.1134/S000368381501007X.
- Gonzalez D.J., Haste N.M., Hollands A. et al. Microbial competition between Bacillus subtilis and Staphylococcus aureus monitored by imaging mass spectrometry. Microbiology. 2011. 157. 2485. 10.1099/mic.0.048736-0.
- Ben David N., Mafi M., Nyska A. et al. Bacillus subtilis in PVA Microparticles for Treating Open Wounds. ACS Omega. 2021. Vol. 6(21). P. 13647-13653. doi: 10.1021/acsomega.1c00790.
- Elshaghabee F.M.F., Rokana N., Gulhane R.D., Sharma C., Panwar H. Bacillus as potential probiotics: status, concerns, and future perspectives. Front. Microbiol. 2017. Vol. 8. P. 1490. 10.3389/fmicb.2017.01490.
- Cui Y., Märtlbauer E., Dietrich R., Luo H., Ding S., Zhu K. Multifaceted toxin profile, an approach toward a better understanding of probiotic Bacillus cereus. Crit. Rev. Toxicol. 2019. Vol. 49. P. 342-356. 10.1080/10408444.2019.1609410.
- Gupta R.C., Srivastava A., Lall R. Nutraceuticals in Veterinary Medicine. Cham: Springer Nature Switzerland AG. 2019. P. 271-285. 10.1007/978-3-030-04624-8.
- Haque M.A., Quan H., Zuo Z., Khan A., Siddique N., He C. Pathogenicity of feed-borne Bacillus cereus and its implication on food safety. Agrobiol. Rec. 2021. Vol. 3. P. 1-16. 10.47278/journal.abr/2020.015.
- Сафронова Л.А. Біологічна активність пробіотичних штамів бацил, основи препарату ендоспорину. Збірник доповідей НАН України. 2015. № 6. С. 138-146.
- Марушко Р.В. Спороутворюючі пробіотики та їх застосування у дітей. Сучасна педіатрія. 2015. 4(68). 77-84. doi: 10.15574/SP.2015.68.77.
- Легеза К.Н., Чаплинський В.Я., Сорокулова І.Б., Якимова С.В., Грицаєнко А.М. Застосування біоспорину при лікуванні кишкових інфекцій. Сучасна педіатрія. 2013. № 5. С. 172-174.
- Algburi A., Al-Hasani H.M., Ismael T.K. et al. Antimicrobial Activity of Bacillus subtilis KATMIRA1933 and Bacillus amyloliquefaciens B-1895 Against Staphylococcus aureus Biofilms Isolated from Wound Infection. Probiotics Antimicrob. Proteins. 2021. Vol. 13(1). P. 125-134. doi: 10.1007/s12602-020-09673-4.
- Бойко В.В., Кравцов О.В., Лихман В.М., Кравцова О.О. Місцеве лікування опікових ран із застосуванням пробіотиків. Харківська хірургічна школа. 2022. № 4–5 (115–116). C. 6-10. Doi: 10.37699/2308-7005.4-5.2022.01.
- Chen G., Wang F., Zhang X., Shang Y., Zhao Y. Living microecological hydrogels for wound healing. Sci. Adv. 2023. Vol. 9(21). P. eadg3478. doi: 10.1126/sciadv.adg3478.
- Sliman R., Rehm S., Shlaes D.M. Serious infections caused by Bacillus species. Medicine (Baltimore). 1987. Vol. 66(3). P. 218-223. doi: 10.1097/00005792-198705000-00005.
- Redgrave L.S., Sutton S.B., Webber M.A., Piddock L.J.V. Fluoroquinolone resistance: mechanisms, impact on bacteria, and role in evolutionary success. Trends in Microbiology. 2014. Vol. 22. № 8. P. 438-445. doi: 10.1016/j.tim.2014.04.007.
- Бур’янов О.А., Ярмолюк Ю.О., Лось Д.В., Вакулич М.В. Сучасні хірургічні методи лікування постраждалих з вогнепальними пораненнями кінцівок. Травма. 2017. Т. 18. № 2. С. 30-35. doi: 10.22141/1608-1706.2.18.2017.102555.