Журнал "Гастроэнтерология" Том 57, №4, 2023
Вернуться к номеру
Диференційований підхід до вибору панкреатоєюноанастомозу під час панкреатодуоденектомії
Авторы: Велигоцький М.М., Арутюнов С.Е., Велігоцький О.М.
Харківський національний медичний університет, м. Харків, Україна
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
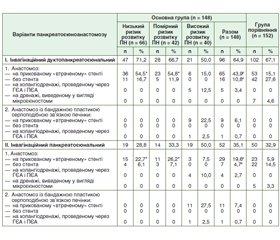
Актуальність. У разі новоутворень панкреатодуоденальної зони радикальним оперативним втручанням є панкреатодуоденектомія (ПДЕ), яка супроводжується частими післяопераційними ускладненнями. Відповідальним моментом реконструктивного етапу панкреатодуоденектомії є виконання панкреатоєюноанастомозу (ПЄА), що обумовлює важливість вдосконалення методик його пластики та дренування, а також розробку диференційованого підходу до вибору ПЄА. Мета дослідження: оцінка ефективності диференційованого підходу до вибору методики ПЄА при виконанні панкреатодуоденектомії. Матеріали та методи. У дослідження включено 302 пацієнти, яким виконано панкреатодуоденектомію з приводу новоутворень підшлункової залози (ПЗ). Вік хворих варіював від 31 до 77 років, чоловіків — 178 (58,9 %), жінок — 124 (41,1 %). У групі порівняння (154 пацієнти) виконували стандартний діагностично-лікувальний алгоритм із вибором методики ПЄА з урахуванням інтраопераційної оцінки ступеня щільності паренхіми підшлункової залози та оцінкою протокової системи (досвід та інтуїція хірурга). В основній групі (148 хворих) застосовували вдосконалений діагностично-лікувальний алгоритм, що включав застосування неінвазивних передопераційних методик візуалізації змін паренхіми ПЗ, анатомічних особливостей її перешийка та протокової системи, а також використання розроблених методик пластики та дренування ПЄА. Результати. В основній групі застосований диференційований підхід до вибору ПЄА полягав у тому, що на доопераційному етапі було проведено прогнозування ступеня ризику розвитку панкреатичної нориці (ПН): у 66 (44,6 %) пацієнтів виявлено низький ризик, у 42 (28,4 %) — помірний ризик, у 40 (27,0 %) хворих — високий ризик розвитку ПН. Виділення хворих із високим ризиком розвитку ПН дало змогу не тільки на операційному, але й на доопераційному етапі виконати необхідні лікувальні заходи, що вплинуло на зменшення частоти розвитку тяжких форм ПН. А саме, у групі порівняння тип В відзначено в 2,5 раза (χ2 = 3,94; р = 0,047) та тип С — в 6,4 раза (р = 0,034 за точним критерієм Фішера) частіше, ніж в основній групі. Це стало підґрунтям для розробки методик ПЄА з пластичним укриттям зони анастомозу та удосконалення методик дренування ПЄА з одночасним дренуванням біліодигестивного анастомозу. Розроблений диференційований підхід до вибору методики ПЄА на основі оцінки в доопераційному періоді ступеня ризику розвитку ПН дав змогу знизити частоту її розвитку, особливо тяжких форм (типи В і С), з 16,2 % випадків у групі порівняння до 5,4 % — в основній групі (χ2 = 8,01; р = 0,005). Летальність з приводу панкреатичної фістули в основній групі становила 0,7 %, у групі порівняння — 4,8 % (р = 0,034, точний критерій Фішера). Висновки. Проведення доопераційної неінвазивної оцінки ступеня змін паренхіми підшлункової залози і стану вірсунгової протоки із застосуванням фіброеластографії, комп’ютерної томографії дало змогу розробити диференційований підхід до вибору методики ПЄА з урахуванням прогнозування ризику розвитку ПН у післяопераційному періоді (чутливість — 90,5 %, специфічність — 81,8 %, діагностична точність — 86,1 %). Використання розроблених методик із застосуванням бандажної пластики серпоподібною зв’язкою печінки та холангіодренажу для дренування ПЄА за м’якої підшлункової залози дало змогу знизити частоту розвитку ПН у 2 рази (р < 0,05), що призвело до зменшення летальності майже в 7 разів (р < 0,05).
Background. Pancreatoduodenectomy is a radical surgical intervention in case of neoplasms of the pancreatoduodenal zone, which is accompanied by frequent postoperative complications. The critical point of the reconstructive stage of pancreatoduodenectomy is pancreaticojejunostomy (PES), which dictates the importance of improving the techniques of its repair and drainage, as well as the development of a differentiated approach to the choice of PES. The aim of the study: to evaluate the effectiveness of a differentiated approach to the choice of PES technique when performing pancreatoduodenectomy. Materials and methods. The study included 302 patients who underwent pancreatoduodenectomy for pancreatic neoplasms. The age of patients varied from 31 to 77 years, there were 178 (58.9 %) men, and 124 (41.1 %) women. In the comparison group (154 patients), a standard diagnostic and treatment algorithm was used with the choice of PES technique taking into account the intraoperative evaluation of the degree of the pancreatic parenchyma density and the assessment of the ductal system (surgeon’s experience and intuition). In the main group (148 patients), an improved diagnostic and treatment algorithm was used, which included non-invasive preoperative methods of visualization of changes in the pancreatic parenchyma, anatomical features of its isthmus and ductal system, as well as the use of developed methods for repair and drainage of the PES. Results. In the main group, the applied differentiated approach to the selection of PES consisted in the fact that at the preoperative stage, the degree of risk of developing pancreatic fistula (PF) was predicted: in 66 (44.6 %) patients, a low risk was detected, in 42 (28.4 %) — a moderate risk, 40 (27.0 %) people had a high risk. Identification of patients with a high risk of developing PF made it possible to carry out the necessary medical measures not only in the operating room, but also in the pre-operative stage, which affected a decrease in the frequency of severe forms of PF. Specifically, in the comparison group, type B was noted 2.5 times (χ2 = 3.94; p = 0.047) and type C — 6.4 times (p = 0.034 according to Fisher’s exact test) more often than in the main group. This became the basis for the development of PES techniques with plastic covering of the anastomotic zone and improvement of PES drainage techniques with simultaneous drainage of the biliodigestive anastomosis. The developed differentiated approach to the choice of PES method based on the preoperative assessment of the risk of PF made it possible to reduce the frequency of its development, especially severe forms (types B and C) from 16.2 % of cases in the comparison group to 5.4 % in main group (χ2 = 8.01; p = 0.005). Mortality due to pancreatic fistula in the main group was 0.7 %, in the comparison group — 4.8 % (p = 0.034, Fisher’s exact test). Conclusions. Carrying out a preoperative non-invasive assessment of the degree of changes in the pancreatic parenchyma and the state of the duct of Wirsung by means of fibroelastography and computer tomography made it possible to develop a differentiated approach to the choice of PES technique, taking into account the prediction of the risk of PF in the postoperative period (sensitivity — 90.5 %, specificity — 81, 8 %, diagnostic accuracy — 86.1 %). The use of the developed methods with a falciform ligament wrap and cholangiodrainage to drain PES in soft pancreas made it possible to reduce in half the frequency of PF development (p < 0.05), which led to a decrease in mortality by almost 7 times (p < 0.05).
панкреатодуоденектомія; панкреатоєюноанастомоз; зміни паренхіми підшлункової залози
pancreatoduodenectomy; pancreaticojejunostomy; changes in the pancreatic parenchyma
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- A score model based on pancreatic steatosis and fibrosis and pancreatic duc diameter to predict postoperative pancreatic fistula after pancreatoduodenectomy / G. Xingjun et al. BMC Surgery. 2019. Vol. 19(1). P. 75-83. doi: https://doi.org/10.1186/s12893-019-0534-4.
- Велигоцкий Н.Н., Велигоцкий А.Н., Арутюнов С.Э., Клименко М.В. Выбор панкреатоеюноанастомоза на основании опыта 200 панкреатодуоденальных резекций. Клінічна хірургія. 2014. № 6. С. 5-7. URL: https://hirurgiya.com.ua/index.php/journal/issue/view/77/6-2014.
- Методи профілактики виникнення панкреатичної нориці після панкреатодуоденектомії / В.М. Копчак та ін. Клінічна хірургія. 2022. Т. 89. № 3–4. С. 18-24. doi: https://doi.org/10.26779/2522-1396.2022.3-4.18.
- Pancreatic CT density is an optimal imaging biomarker for earlier detection of malignancy in the pancreas with intraductal papillary mucinous neoplasm / D. Yamada et al. Pancreatology. 2022. Vol. 22(4). P. 488-496. doi: https://doi.org/10.1016/j.pan.2022.03.016.
- Еластографія зсувної хвилі в оцінці морфологічних змін підшлункової залози при хронічному панкреатиті / О.М. Бабій та ін. Клінічна хірургія. 2019. Т. 86. № 1. С. 10-12. doi: https://doi.org/10.26779/2522-1396.2019.01.10.
- Role of ultrasound shear wave elastography in preoperative prediction of pancreatic fistula after pancreaticoduodenectomy / N. Sushma et al. Pancreatology. 2020. Vol. 20(8). P. 1764-1769. doi: https://doi.org/10.1016/j.pan.2020.10.047.
- Pancreatic ultrasound elastography is not useful to predict the risk of pancreatic fistulas after pancreatic resection / G. Marasco et al. Updates Surg. 2020. Vol. 72(4). P. 1081-1087. doi: https://doi.org/10.1007/s13304-020-00748-z.
- Multifactorial mitigation strategy to reduce clinically relevant pancreatic fistula in high-risk pancreatojejunostomy following pancreaticoduodenectomy / F. Ausania et al. Pancreatology. 2021. Vol. 21(2). P. 466-472. doi: https://doi.org/10.1016/j.pan.2020.12.019.
- A simple preoperative stratification tool predicting the risk of postoperative pancreatic fistula after pancreatoduodenectomy / H. Lapshyn et al. Pancreatology. 2020. Vol. 21(5). P. 957-964. doi: https://doi.org/10.1016/j.pan.2021.03.009.
- Novel risk scoring system for prediction of pancreatic fistula after pancreaticoduodenectomy / Y. Li et al. World Journal of Gastroenterology. 2019. Vol. 25(21). P. 2650-2664. doi: https://doi.org/10.3748/wjg.v25.i21.2650.
- Pre-operative prediction of pancreatic fistula: Is it possible? / K. Roberts et al. Pancreatology. 2013. Vol. 13(4). P. 423-428. doi: https://doi.org/10.1016/j.pan.2013.04.322.
- Pros and pitfalls of externalized trans-anastomotic stent as a mitigation strategy of POPF: a prospective risk-stratified observational series / S. Andrianello et al. HPB (Oxford). 2021. Vol. 23 (7). P. 1046-1053. doi: https://doi.org/10.1016/j.hpb.2020.10.025.
- Surgical techniques and postoperative management to prevent postoperative pancreatic fistula after pancreatic surgery / H. Kawaida et al. World Journal of Gastroenterology. 2019. Vol. 25(28). P. 3722-3737. doi: https://doi.org/10.3748/wjg.v25.i28.3722.
- Risk stratification for postoperative pancreatic fistula using the pancreatic surgery registry StuDoQjPancreas of the German Society for General and Visceral Surgery / E. Petrova et al. Pancreatology. 2019. Vol. 19(1). P. 17-25. doi: https://doi.org/10.1016/j.pan.2018.11.008.
- Perioperative acinar cell count method works well in the prediction of postoperative pancreatic fistula and other postoperative complications after pancreaticoduodenectomy / V. Teranen et al. Pancreatology. 2021. Vol. 21(2). P. 487-493. doi: https://doi.org/10.1016/j.pan.2021.01.005.
- Pancreatic parenchymal changes seen on endoscopic ultrasound are dynamic in the setting of fatty pancreas: A short-term follow-up study / A. Muftah et al. Pancreatology. 2022. Vol. 22(6). P. 1187-1194. doi: https://doi.org/10.1016/j.pan.2022.10.006.
- Beger H.G. Benign tumors of the pancreas-radical surgery versus parenchyma-sparing local resection — the challenge facing surgeons. J. Gastrointest. Surg. 2018. Vol. 22(3). P. 562-566. doi: https://doi.org/10.1007/s11605-017-3644-2.
- Endoscopic ultrasound elastography for small solid pancreatic lesions with or without main pancreatic duct dilatation / K. Kataoka et al. Pancreatology. 2021. Vol. 21(2). P. 451-458. doi: https://doi.org/10.1016/j.pan.2020.12.012.
- Serum lipase on postoperative day one is a strong predictor of clinically relevant pancreatic fistula after pancreaticoduodenectomy: A retrospective cohort / H. Chen et al. Pancreatology. 2022. Vol. 22(8). P. 810-816. doi: https://doi.org/10.1016/j.pan.2022.06.001.