Международный неврологический журнал 4 (66) 2014
Вернуться к номеру
Клінічний перебіг гострого больового синдрому, обумовленого дискогенною попереково-крижовою радикулопатією, на фоні лікування нестероїдними протизапальними препаратами
Авторы: Литвиненко Н.В., Ковтун І.І. - ВДНЗУ «Українська медична стоматологічна академія», м. Полтава
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
Проведено комплексне дослідження 51 пацієнта віком від 29 до 55 років із гострим больовим синдромом (ГБС), обумовленим дискогенною попереково-крижовою радикулопатією (ПКР), на фоні лікування диклофенаком та лорноксикамом (Ксефокамом). Проводили кількісну та якісну оцінку ГБС та особистісних особливостей пацієнтів за уніфікованими шкалами, визначали в сироватці крові маркери ноцицептивної системи (субстанцію Р). Аналіз результатів дослідження виявив, що застосування лорноксикаму (Ксефокаму) у комплексній терапії ГБС, обумовленого ПКР, показало більшу ефективність щодо покращення статико-локомоторних функцій хребта, зменшення інтенсивності больового синдрому за візуальною аналоговою шкалою (з вираженої до легкої) та якісних характеристик больового синдрому за рахунок сенсорної та афективної складових за опитувальником Мак-Гілла, зменшення рівня депресії, значного зниження концентрації субстанції Р у сироватці крові хворих.
Проведено комплексное обследование 51 пациента в возрасте от 29 до 55 лет с острым болевым синдромом (ОБС), обусловленным дискогенной пояснично-крестцовой радикулопатией (ПКР), на фоне лечения диклофенаком и лорноксикамом (Ксефокамом). Проводили количественную и качественную оценку ОБС и личностных особенностей пациентов по унифицированным шкалам, определяли в сыворотке крови маркеры ноцицептивной системы (субстанцию Р). Анализ результатов исследования выявил, что использование лорноксикама (Ксефокама) в комплексной терапии ОБС, обусловленного ПКР, показало большую эффективность в отношении улучшения статико-локомоторных функций позвоночника, уменьшения интенсивности болевого синдрома по визуальной аналоговой шкале (с выраженной до легкой) и качественных характеристик болевого синдрома за счет сенсорной и аффективной составляющих по опроснику Мак-Гилла, уменьшения уровня депрессии, значительного снижения концентрации субстанции Р в сыворотке крови больных, улучшения уровня жизнедеятельности пациентов.
Comprehensive examination has been carried out in 51 patients aged 29 to 55 years with acute pain syndrome (APS), caused by discogenic lumbosacral radiculopathy (DLR) on the background of treatment with diclofenac and lornoxicam (Xefocam). We have carried out a quantitative and qualitative assessment of APS and personality characteristics of patients on standardized scales, determined markers of nociceptive system (substance P) in the blood serum. Analysis of the findings revealed that the use of lornoxicam (Xefocam) in complex therapy for APS caused by DLR showed greater efficacy in terms of improving static-locomotor functions of the spine, reducing pain syndrome severity by VAS (form severe to mild) and qualitative characteristics of pain syndrome due to sensory and affective components by McGill questionnaire, reduced level of depression, a significant reduction of substance P concentration in the blood serum of patients, improving the level of patients’ vital activity.
больовий синдром, нестероїдні протизапальні препарати, радикулопатія.
болевой синдром, нестероидные противовоспалительные препараты, радикулопатия.
pain syndrome, non-steroidal antiinflammatory drugs, radiculopathy.
Статья опубликована на с. 91-95
Біль у спині займає друге місце за частотою серед усіх випадків тимчасової непрацездатності та п’яте місце серед випадків госпіталізації в Україні [1]. Лікування гострого больового синдрому (ГБС) повинно починатися в максимально ранні строки з метою повернення пацієнта до активного способу життя, запобігання повторним загостренням та хронізації больового синдрому [2–4]. Згідно з літературними даними, у 10–20 % хворих працездатного віку гостра дорсалгія трансформується у хронічну [5]. Хронізація провокується перебудовою периферичної та центральної нервової систем, що перевантажуються больовими імпульсами від запальних м’язів, зв’язок, фасеткових суглобів та інших структур. Найтяжчим варіантом вертеброгенних больових синдромів є попереково-крижова радикулопатія. У більшості випадків біль у спині минає через декілька днів або 2–4 тижні, при радикулопатії біль триває тижні або місяці та в частині випадків хронізується і триває роки [3, 6]. Хронічному перебігу болю в спині сприяє неадекватне лікування гострого болю та інші причини (тривалий ліжковий режим, надмірне обмеження фізичних навантажень, «больовий» тип особистості, понижений фон настрою, у частині випадків зацікавленість пацієнта в тривалій непрацездатності, агравація симптомів та рентне ставлення до хвороби) [7]. Золотим стандартом для лікування гострого болю у спині є нестероїдні протизапальні препарати (НПЗП). Механізм дії НПЗП полягає в інгібуванні циклооксигенази — ключового ферменту в каскаді метаболізму арахідонової кислоти, що є попередником простагландинів, простациклінів та тромбоксанів. Внаслідок зменшення синтезу простагландинів знижується продукція медіаторів набряку та запалення, зменшується чутливість нервових структур до брадикініну, гістаміну, оксиду азоту, що утворюються в тканинах при запаленні [8, 9]. НПЗП поділяють на 4 групи залежно від аналгезуючої активності та періоду напіввиведення. До групи з високою аналгезуючою активністю та коротким періодом напіввиведення зараховують диклофенак, індометацин, лорноксикам (Ксефокам) та кетопрофен [10]. Препарати саме цієї групи використовують для лікування гострого больового синдрому.
Мета — комплексне порівняння клінічного перебігу ГБС, обумовленого дискогенною радикулопатією L5, S1, на фоні лікування різними групами НПЗП — натрієвою сіллю диклофенаку та лорноксикамом.
Матеріали та методи
Проведено обстеження 51 пацієнта (27 чоловіків, 24 жінки) віком від 29 до 55 років (у середньому 43,10 ± 0,80 року) із ГБС, обумовленим попереково-крижовою радикулопатією (ПКР). До групи здорових увійшли 20 практично здорових осіб (8 жінок, 12 чоловіків), середній вік яких становив 43,0 ± 1,8 року. Обстеження пацієнтів проводилось за спеціально розробленою нами картою пацієнта з болем у нижній частині спини, що включала дані анамнезу та скарг, неврологічного статусу, параклінічних методів обстеження, зокрема магнітно-резонансної томографії попереково-крижового відділу хребта. У всіх хворих був діагностований ГБС, пов’язаний із компресією L5 (17 хворих — 33,33 %) або S1 (34 хворі — 66,67 %) корінців на фоні протрузій та гриж міжхребцевих дисків. Пацієнти були оглянуті нейрохірургом і на момент лікування не потребували нейрохірургічної допомоги. Для об’єктивізації больового синдрому, оцінки обсягу активних рухів у поперековому відділі хребта, наявності депресії, рівня тривожності хворого, порушення його життєдіяльності та контролю за ефективністю застосовуваної терапії було використано уніфіковані шкали: візуальну аналогову шкалу болю (ВАШ), опитувальник болю Мак–Гілла, тести Томайера та Шобера, шкала депресії Бека, тест Спілбергера — Ханіна, опитувальник Роланда — Морріса.
ВАШ являє собою відрізок довжиною 10 см. Хворий відмічав знаком цифру (бал), що відповідала інтенсивності болю на відрізку, початок якого (0 балів) відповідав відсутності больового відчуття, 1–3 бали — болю слабкої інтенсивності, 4–6 балів — середньої інтенсивності болю, 7–9 балів — сильному болю, а кінець (10 балів) — дуже сильному (нестерпному) болю. Опитувальник болю Мак-Гілла дає якісну характеристику вимірювання болю. Сімдесят вісім слів, що характеризували біль, були розподілені на двадцять класів (субшкал) і утворили 3 головні класи (шкали). Перший клас (з 1-ї по 13-ту субшкалу) давав характеристику болю на сенсорному рівні, другий клас (з 14-ї по 18-ту субшкалу) — на емоційному рівні, третій клас (з 19-го по 20-й) допомагав визначити інтенсивність болю. Хворий вибирав ті чи інші дескриптори з будь-яких 20 субшкал, але лише один дескриптор у відповідній шкалі. Вираховувався ранговий індекс болю (РІБ) — сума порядкових номерів дескрипторів у всіх субшкалах та індекс числа вибраних дескрипторів (ІЧВД). Шкала Мак-Гілла дозволяє виміряти сенсорну, емоційну та кількісну (евалюативну) складові больового відчуття. Оцінка ступеня депресивних розладів проводилась за допомогою тесту Бека. Результат 10–15 балів вказував на наявність м’якої депресії, 16–19 балів — на помірно виражену депресію, понад 19 балів — на значний ступінь депресивних розладів. Рівень тривожності проводився за допомогою тесту Спілбергера — Ханіна (визначення особистісної та реактивної тривожності). Результат до 30 балів відбивав низький рівень тривожності, 31–45 балів — середній, 46 балів і більше — високий рівень тривожності. Обмеження рухової активності оцінювали за опитувальником Роланда — Морріса, що включав 18 питань, які визначали життєдіяльність у зв’язку з болем у спині. Порушення життєдіяльності констатували в тому разі, якщо пацієнт відмічав 7 пунктів. Порушення вважали вираженими (8–12 пунктів) або значно вираженими (13–18 пунктів).
Пацієнтам, а також групі здорових осіб визначали в сироватці крові рівень субстанції Р. Пацієнти були розподілені на дві групи. Контрольну групу становили 26 пацієнтів, які отримували лікування: НПЗП (натрієва сіль диклофенаку в дозі 75 мг внутрішньом’язово щоденно 7 днів), міорелаксант (толперизон 100 мг внутрішньом’язово щоденно 14 днів), вітамінні препарати (тіаміну гідрохлорид 100 мг, піридоксину гідрохлорид 100 мг, ціанокобаламін 1 мг внутрішньом’язово через день 5 ін’єкцій). Основну групу становили 25 пацієнтів, яким була призначена терапія за вищенаведеною схемою, при цьому натрієву сіль диклофенаку було замінено на Ксефокам 16 мг внутрішньом’язово щодня 7 днів. Курс лікування тривав 14 днів, всім пацієнтам проведено комплексне обстеження на 1-й та 14-й день спостереження.
Результати та їх обговорення
Основними клінічними симптомами у пацієнтів обох груп були біль у попереково-крижовому відділі хребта з іррадіацією в нижню кінцівку (100 %), протибольовий сколіоз (39 хворих — 76,47 %), напруження м’язів спини (100 %), зниження або зникнення ахіллового рефлексу (67 %); гіпестезія (38 хворих — 74,5 %), гіперестезія (13 хворих — 25,5 %), гіпотонія м’язів (7 хворих — 13,7 %) у ділянці ураженого корінця. Вираженими були симптом натягу Ласега (у середньому становив 32,2 ± 1,6 градуса), функціональні порушення стану хребта (за тестами Шобера та Томайера відповідно 2,60 ± 0,16 см та 34,40 ± 1,48 см). Згідно з проведеним обстеженням, за ВАШ у групі хворих до лікування біль оцінювався як помірний у 18 пацієнтів (35,3 %), як сильний — у 27 пацієнтів (52,9 %), як дуже сильний — у 6 пацієнтів (11,88 %) і в середньому становив 7,60 ± 0,27 бала (відповідав сильному). Загалом за віком, статтю, інтенсивністю больового синдрому та об’єктивною неврологічною симптоматикою обидві групи були однорідними.
Після проведеної терапії в обох групах хворих відмічено зменшення вираженості клінічної симптоматики ГБС (табл. 1).
Згідно з даними, наведеними в табл. 1, терапія НПЗП приводила до значного зменшення клінічних проявів ГБС, обумовленого дискогенною ПКР, в обох групах. В основній групі пацієнтів із застосуванням лорноксикаму в комплексній терапії була виявлена більш виражена позитивна динаміка таких параметрів, як анталгічний сколіоз, напруження м’язів спини, інтенсивність больового синдрому. Поряд із зменшенням проявів больового синдрому в пацієнтів обох груп після лікування виявлено покращення статико-локомоторних функцій, пов’язаних з алгічним та м’язово-тонічним компонентом. Так, у контрольній та основній групах спостерігали зростання кута розгинання випрямленої нижньої кінцівки в кульшовому суглобі при перевірці симптому Ласега (в основній групі 32,40 ± 1,39° до лікування, 73,00 ± 1,29° після лікування, p < 0,05; у контрольній групі 32,10 ± 1,82°до лікування, 61,00 ± 1,54° після лікування, p < 0,05); зростання відстані від L5 хребця при максимальному нахилі вперед за пробою Шобера (в основній групі 2,70 ± 0,15 см до лікування, 4,40 ± 0,08 см після лікування, p < 0,05; у контрольній групі 2,70 ± 0,17 см до лікування, 4,10 ± 0,11 см після лікування, p < 0,05); зменшення відстані від III пальця витягнутих рук до підлоги при максимальному нахилі вперед при перевірці проби Томайера (в основній групі 36,00 ± 1,31 см до лікування, 14,90 ± 0,77 см після лікування, p < 0,05; у контрольній групі 35,90 ± 1,64 см до лікування, 19,20 ± 0,99 см після лікування, p < 0,05).
Невід’ємною складовою клінічної картини ГБС, обумовленого дискогенною ПКР, у 100 % пацієнтів були тривожні та депресивні прояви, виявлені за допомогою тесту Спілбергера — Ханіна та шкали Бека. Динаміка рівнів тривожності та депресії у пацієнтів контрольної та основної груп наведена в табл. 2.
За даними, наведеними у табл. 2, після лікування лорноксикамом та диклофенаком у пацієнтів вірогідно зменшився рівень реактивної тривожності (з високого до помірного). Потрібно підкреслити, що тільки в основній групі (лікування лорноксикамом) зменшився рівень депресії (з легкого рівня до повної відсутності депресії).
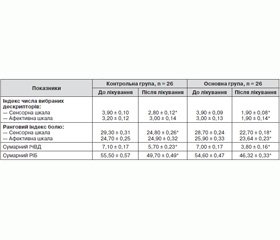
Якісну характеристику больового синдрому до та після лікування оцінювали за опитувальником Мак-Гілла (табл. 3).
Як видно з даних, наведених у табл. 3, на фоні лікування в обох групах хворих вірогідно зменшувалося сумарне число виділених слів (індекс числа виділених дескрипторів, якими пацієнт описував свої больові відчуття, а також значимість цих слів-дескрипторів (ранговий індекс болю)). Після лікування диклофенаком сумарний РІБ та сумарний ІЧВД зменшилися виключно за рахунок сенсорної шкали. Зменшення сумарних ІЧВД та РІБ на фоні лікування лорноксикамом відбувалося за рахунок сенсорної та афективної шкал, що говорить про можливість впливу даної терапії на сенсорну та афективну (емоційну) складові больового відчуття.
Рівень концентрації субстанції Р (маркера ноцицептивної системи) у сироватці крові хворих обох груп до лікування підвищився порівняно з групою здорових осіб у 370 разів у контрольній групі та у 390 разів в основній групі. Під впливом лікування у контрольній та основній групах позитивна динаміка клінічних параметрів була об’єктивізована змінами концентрації субстанції Р в сироватці крові. Так, у контрольній групі концентрація субстанції Р до та після лікування становила 18,80 ± 2,96 мг/мл та 12,92 ± 3,14 мг/мл відповідно, р < 0,05; в основній групі — відповідно 19,70 ± 1,80 мг/мл та 9,10 ± 1,58 мг/мл, р < 0,05. При цьому різниця значень субстанції Р до та після лікування в контрольній групі становила 5,90 ± 0,28 мг/мл, в основній — 10,60 ± 0,64 мг/мл, р < 0,05.
ГБС до лікування у групах супроводжувався значним порушенням життєдіяльності пацієнтів, про що свідчила наявність обмежень, пов’язаних із болем за даними опитувальника Роланда — Морріса: у контрольній групі — 11,70 ± 0,54 бала, в основній — 11,90 ± 0,45 бала. Після лікування спостерігали підвищення життєдіяльності пацієнтів у контрольній групі на 33,3 % (7,80 ± 0,40 бала, р < 0,05), в основній групі — 60,5 % (4,70 ± 0,26 бала, р < 0,05).
Висновки
Застосування НПЗП у комплексному лікуванні ГБС, обумовленого попереково-крижовою радикулопатією, призводило до зменшення вираженості клінічних проявів больового синдрому, рівня реактивної тривожності, інтенсивності больового відчуття та його якісних характеристик, зниження рівня концентрації субстанції Р у сироватці крові хворих та покращення рівня життєдіяльності пацієнтів.
Застосування лорноксикаму (Ксефокаму) у комплексній терапії ГБС, обумовленого ПКР, показало більшу ефективність щодо покращення статико-локомоторних функцій хребта, зменшення інтенсивності больового синдрому за ВАШ (із вираженої до легкої), якісних характеристик больового синдрому за рахунок сенсорної та афективної складових за опитувальником Мак-Гілла, зменшення рівня депресії, значного зниження рівня концентрації субстанції Р у сироватці крові хворих, покращення рівня життєдіяльності пацієнтів.
1. Морозова О.Г. Острая боль в спине: подходы к терапии // Здоров’я України. — 2007. — № 6/1. — С. 22–23.
2. Иванова М.Ф., Евтушенко С.К. Дорсалгия, обусловленная дегенеративно-дистрофической патологией позвоночника // Новости медицины и фармации. — 2010. — № 15(33). — С. 16–17.
3. Van Tulder M., Becker A., Bekkering T. [et al.] European guidelines for the management of acute nonspecific low back pain in primary care // Eur. Spine J. — 2006. — 15(Suppl. 2). — Р. 169–191.
4. Литвиненко Н.В. Динаміка маркерів ноцицептивної системи та больового синдрому в процесі лікування болю у нижній частині спини, обумовленого дискогенною радикулопатією / Н.В. Литвиненко, І.І. Ковтун // Актуальні проблеми сучасної медицини: Вісник Української медичної стоматологічної академії. — 2013. — Т. 13, № 3(43). — С. 151–153.
5. Боль (практическое руководство для врачей) / Под ред. Н.Н. Яхно, М.Л. Кукушкина. — М.: Издательств РАМН, 2011. — 512 с.
6. Товажнянская Е.Л. Болевые синдромы в области спины: современные направления рациональной фармакотерапии // Международный неврологический журнал. — 2013. — № 2(56). — С. 149–154.
7. Glombiewski J.A., Hartwich-Tersek J. [et al.]. Attrition in Cognitive-behavioral Treatment of Chronic Back Pain // The Clinical Journal of Pain. — 2010. — 26 (7). — P. 137–144.
8. Wilkes J.M., Clark L.E., Herrera J.L. Acetaminophen overdose in pregnancy // South Med. J. — 2005. — 98(11). — Р. 1118–1122.
9. Насонов Е.Л., Лазебник Л.Б., Беленков Ю.Н. [и др.]. Применение нестероидных противовоспалительных препаратов / Клинические рекомендации. — Москва: Алмаз, 2006. — 88 с.
10. Курушина О.В., Барулин А.Е. Современные аспекты лечения болей в спине // Международный неврологический журнал. — 2012. — № 4(50). — С. 105–110.

/93/93.jpg)
/94/94.jpg)