Журнал «Медицина неотложных состояний» 5 (60) 2014
Вернуться к номеру
Оцінка стану кровопостачання нижніх кінцівок у хворих на діабетичну периферичну поліневропатію без уражень магістральних артерій
Авторы: Горобейко М.Б. - Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Обстежено 178 хворих на цукровий діабет 2-го типу з явищами вираженої периферичної поліневропатії. Черезшкірний парціальний тиск кисню (PtcO2) в тканинах стоп був знижений порівняно з нормою у 139 (78 %) пацієнтів. Отримана пряма статистично вірогідна залежність ступеня тканинної ішемії нижніх кінцівок від тривалості цукрового діабету, із найгіршими показниками PtcO2 у хворих із діабетичним стажем понад 12 років. Рівень тканинної ішемії не залежав від статі пацієнтів, статусу тютюнопаління та ступеня компенсації цукрового діабету за показниками глікованого гемоглобіну. У зв’язку з інструментально підтвердженою відсутністю оклюзій артерій гомілок великого та середнього калібру зроблено висновок, що причинами прихованої ішемії стоп є мікроангіопатія та поліневропатія.
Обследовано 178 больных сахарным диабетом 2-го типа с явлениями выраженной диабетической периферической полиневропатии. Чрескожное парциальное давление кислорода (PtcO2) в тканях стоп было снижено по сравнению с нормой у 139 (78 %) пациентов. Получена прямая статистически достоверная зависимость степени тканевой ишемии нижних конечностей от длительности сахарного диабета, с наихудшими показателями PtcO2 у больных с диабетическим стажем более 12 лет. Уровень тканевой ишемии не зависел от пола пациентов, статуса табакокурения и степени компенсации сахарного диабета по показателям гликированного гемоглобина. В связи с инструментально подтвержденным отсутствием окклюзий артерий голени крупного и среднего калибра сделан вывод, что причинами скрытой ишемии стоп являются микроангиопатия и полиневропатия.
The study involved 178 patients with diabetes mellitus type 2 and symptoms of severe diabetic peripheral polyneuropathy. Transcutaneous partial oxygen pressure (PtcO2) in tissues of the feet was reduced compared with the norm in 139 (78 %) patients. We have obtained a direct statistically significant dependence of the degree of tissue ischemia of the lower extremities on the duration of diabetes mellitus, with the worst PtcO2 parameters in patients with diabetes duration more than 12 years. The level of tissue ischemia was independent of sex of the patients, smoking status and degree of diabetes mellitus compensation in terms of glycated hemoglobin. Due to the lack of instrumentally confirmed occlusion of the leg arteries of large and medium caliber we have concluded that the causes of hidden ischemia of the feet are microangiopathy and polyneuropathy.
цукровий діабет, невропатія, мікроангіопатія, діагностика.
сахарный диабет, невропатия, микроангиопатия, диагностика.
diabetes mellitus, neuropathy, microangiopathy, diagnosis.
Статья опубликована на с. 58-60
Вступ
Діабетична невропатія вважається найбільш поширеним хронічним ускладненням цукрового діабету (ЦД). За даними Davies та співавторів, її можна виявити у кожного десятого хворого вже під час первинної діагностики ЦД 2-го типу, а за тривалості захворювання 10 років і більше ознаки ураження периферичної або центральної нервової системи наявні у кожного другого пацієнта [1]. Найчастіше у клінічній практиці зустрічається периферична сенсомоторна поліневропатія нижніх кінцівок. У масштабних багатоцентрових контрольованих дослідженнях DCCT та UKPDS частота її діагностування сягала 20 % у хворих з уперше виявленим ЦД 2-го типу. Поліневропатія може перебігати у больовій формі або тривалий час не турбувати хворого. Безбольова форма вважається найбільш небезпечною, оскільки зниження усіх видів шкірної чутливості сприяє травматизації стоп і є одним із чинників розвитку синдрому діабетичної стопи (СДС).
Згiдно з сучасними уявленнями про патогенез пізніх ускладнень ЦД, зокрема СДС, констатується тісний взаємозв’язок метаболічних і судинних факторів [2–4]. Діабетична поліневропатія та діабетична мікроангіопатія вважаються наслідками одного стану — хронічної гіперглікемії. На практиці важливо враховувати взаємообумовленість цих патологічних процесів. Відомо, що не тiльки зміни vasa nervorum можуть призводити до порушення функції периферичних нервів згідно з судинною теорією розвитку невропатії, але й порушення іннервації мікросудинного русла можуть погіршувати мікроциркуляцію, зокрема шляхом розвитку феномена артеріоло-венулярного шунтування, викликаючи ішемію тканин нижніх кінцівок [5].
Водночас зумовлені ЦД зміни в ендотелії судин, гіперкоагуляція та мікротромбози артеріол та венул також сприяють розвитку ішемії, навіть за збереженої прохідності магістральних судин. У таких випадках говорять про так звані невропатичну або невропатично-ішемічну форми СДС згідно з класифікацією ВООЗ 1991 року. На відміну від ішемічної форми СДС, яка зумовлена здебільшого симптомною ішемією внаслідок порушення прохідності магістральних артерій нижніх кінцівок, за невропатичної або невропатично-ішемічної форм СДС провідну роль відіграють поліневропатія та приховані порушення мікроциркуляції. Таку приховану ішемію можливо встановити шляхом вимірювання черезшкірного парціального тиску кисню (PtcO2) в тканинах стопи [6]. Деякі автори взагалі окремо не виділяють ішемічну форму СДС, відносячи її до нейроішемічної. Пояснюють це тим, що у всіх хворих на ЦД наявні тією чи іншою мірою виражені ураження периферичної нервової системи [7–9].
Разом з тим взаємозв’язки між периферичною невропатією, ішемією тканин нижніх кінцівок та іншими характеристиками перебігу ЦД недостатньо вивчені. Клінічне значення цих взаємозв’язків полягає у можливості більш точної стратифікації ризиків СДС, зокрема у хворих з ознаками невропатії, але без видимих порушень кровопостачання нижніх кінцівок.
Метою нашого дослідження було вивчення поширеності ішемії тканин нижніх кінцівок серед хворих на діабетичну невропатію при збереженій прохідності магістральних артерій та встановлення її зв’язку із тривалістю захворювання, рівнем компенсації ЦД, тютюнопалінням.
Матеріал і методи
У дослідження включали хворих на ЦД 2-го типу з явищами вираженої периферичної поліневропатії та без ознак порушення кровотоку по магістральних артеріях нижніх кінцівок. Ступінь компенсації ЦД визначали за показниками глікованого гемоглобіну, глікемії та глюкозурії у день обстеження. Також визначали діабетичний стаж хворих, тобто час від моменту встановлення діагнозу ЦД, та статус тютюнопаління.
Наявність діабетичної периферичної поліневропатії визначали з урахуванням клінічних настанов Національного інституту здоров’я і клінічного удосконалення Великої Британії (NICE) [10] шляхом вимірювання вібраційної чутливості нижніх кінцівок за допомогою камертона С 128 Гц, дискримінаційної чутливості — тактильного циркулярного дискримінатора, температурної чутливості — тестера «Тіптерм», больової чутливості — набору «Нейропен», тактильної чутливості — монофіламентів, а також висоти рефлексів з ахіллова сухожилка за допомогою неврологічного молоточка та рефлексометрії.
Критерієм діагнозу периферичної невропатії вважали зниження двох або більше видів чутливості. Виключалися інші можливі причини невропатії: метаболічні порушення крім цукрового діабету, екзогенні інтоксикації, інші неврологічні, інфекційні, алергічні захворювання, системні захворювання сполучної тканини.
Для виключення наявності оклюзій магістральних артерій нижніх кінцівок після збору анамнезу, фізикальних та лабораторний тестів досліджували прохідність артерій гомілок методом ультразвукової допплерографії з обчисленням кісточково-плечового індексу.
Усім хворим вимірювали парціальний тиск кисню (PtcO2) на тилі правої стопи за допомогою газоаналізатора компанії Rаdiometer із візуалізуючою приставкою для обробки даних.
Результати та обговорення
Обстежено 178 хворих (82 чоловіки і 96 жінок) віком від 39 до 62 років. Середній вік чоловіків становив 48,56 ± 9,23 року, жінок — 51,58 ± 8,35 року.
Середній рівень глікованого гемоглобіну в чоловіків — 8,97 ± 2,53 г/л, у жінок — 8,39 ± 1,87 г/л.
Тривалість перебігу ЦД становила до 7 років у 28 чоловіків та 34 жінок, 7–12 років — у 36 чоловіків та 44 жінок, більше 12 років — у 18 чоловіків та 18 жінок.
Курцями на момент обстеження були 33 чоловіки та 13 жінок. Двоє чоловіків та 3 жінки кинули палити протягом двох останніх років, проте палили більше ніж 10 років до цього, тому також були зараховані до групи курців.
/60/60_2.jpg)
Парціальний тиск кисню в тканинах стопи був знижений порівняно з нормою у 139 пацієнтів (78 %). В інших 39 осiб цей показник знаходився в межах 55–63 мм рт.ст. Слід зазначити, що рівень PtcO2 визначався у перші 1–2 дні з моменту госпіталізації, коли практично всі хворі мали декомпенсацію ЦД того чи іншого ступеня. Статистичної залежності рівня PtcO2 від глікованого гемоглобіну не було виявлено, окрім того факту, що у всіх шести пацієнтів з рівнем глікованого гемоглобіну > 10,0 г/л рівень PtcO2 не перевищував 30 мм рт.ст., що вказує на критичну ішемію нижніх кінцівок.
Унаслідок малої вибірки не було отримано вірогідних відмінностей між групами курців і некурців. Також не виявлено вірогідних відмінностей між чоловіками та жінками як в цілому, так і в межах груп дослідження.
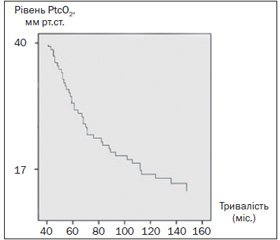
Натомість досить наглядною виявилася різниця показників PtcO2 залежно від стажу діабету, з вірогідною тенденцією до зниження киснезабезпечення нижніх кінцівок прямо пропорційно тривалості захворювання (табл. 1).
Як видно з табл. 1, найгірші показники PtcO2, що відповідають критичній ішемії, були в підгрупі чоловіків з діабетичним стажем понад 12 років.
При цьому порушення прохідності магістральних артерій ніг були відсутніми за даними допплерографії у всіх пацієнтів. Кісточково-плечовий індекс варіював у межах 1–1,2. Стенозів та оклюзій артеріальних судин нижніх кінцівок не було знайдено у жодному випадку.
У кожного з пацієнтів було порушено понад два види чутливості нижніх кінцівок і спостерігалася гіпорефлексія з ахіллових сухожилків, що підтверджувало діагноз діабетичної периферичної поліневропатії, оскільки інших причин ураження периферичних нервів під час ретельного збору анамнезу та обстеження хворих знайдено не було. Отже, саме приховані порушення мікроциркуляції нижніх кінцівок і невропатія, які ми вважаємо взаємозумовленими, становили патологічний субстрат зниження киснезабезпечення тканин нижніх кінцівок у більшості хворих (78 % обстежених).
Висновки
1. Навіть за збереженої прохідності магістральних судин нижніх кінцівок у хворих на діабетичну периферичну поліневропатію парціальний тиск кисню у тканинах стопи може бути значно зниженим.
2. За отриманими даними рівень тканинної ішемії не залежить від статі пацієнтів, статусу тютюнопаління та ступеня компенсації цукрового діабету за показниками глікованого гемоглобіну.
3. Відмічається пряма статистично вірогідна залежність ступеня тканинної ішемії нижніх кінцівок від діабетичного стажу пацієнта. Особливу увагу слід звертати на хворих з тривалим (10–12 і більше років) перебігом ЦД, оскільки навіть за відсутності оклюзійних уражень магістральних артерій гомілок у них можна виявити приховану ішемію стоп критичного рівня. Такі хворі становлять групу високого ризику за розвитком СДС.
4. Таким чином, необхідно внести до стандартної схеми лікування хворих на діабетичну периферичну невропатію, крім стандартних цуркознижувальних препаратів та АЛК, ще й засоби для покращення мікроциркуляції, насамперед низькомолекулярні гепарини другого покоління (беміпарин) як фонове лікування протягом 16–20 днів у дозі 2500 Од на добу.
1. Davies M., Brophy S., Williams R., Taylor A. The Prevalence, Severity, and Impact of Painful Diabetic Peripheral Neuropathy in Type 2 Diabetes // Diabetes Care. — 2006. — Vol. 29. — P. 1518-1522.
2. Boulton A.J.M., Connor H., Cavanagh P.R. The foot in diabetes. — Chichester: J. Willey & Sons, 1994. — 256 p.
3. Brownlee M. Negative consequences of glycation // Metabolism. — 2000. — Vol. 49, Suppl. 2. — P. 9-13.
4. Cameron N.E., Cotter M.A. The relationship of vascular changes to metabolic factors in diabetes mellitus and their role in development of peripheral nerve complications // Diab. Metab. Rev. — 1994. — Vol. 10, № 3. — P. 189-224.
5. Gershater M.A., Löndahl M., Nyberg P. et al. Complexity of factors related to outcome of neuropathic and neuroischaemic/ischaemic diabetic foot ulcers: a cohort study // Diabetologia. — 2009. — Vol. 52, № 3. — P. 398-407.
6. Таран Є.В., Бабіна Г.В., Горобейко М.Б., Гирявенко О.Я., Болгарська С.В. Парціальний тиск кисню у шкірі стоп хворих на цукровий діабет, ускладений периферичною нейропатією та мікроангіопатією // Клінічна ендокринологія та ендокринна хірургія. — 2007. — № 1(18). — C. 49-50.
7. Гурьева И.В. Профилактика, лечение, медико-социальная реабилитация и организация междисциплинарной помощи больным с синдромом диабетической стопы: Дис... д-ра мед. наук. — М., 2001.
8. Светухин А.М., Земляной А.Б. Гнойно-некротические формы синдрома диабетической стопы // Consilium medicum. — 2002. — Т. 4, № 10.
9. Бегма А.Н., Бегма И.В., Демин Д.И., Поташов Д.А., Гурьева И.В., Земляной А.Б. Оптимизация лечения нейроишемической формы синдрома диабетической стопы // Здравоохранение Урала. — 2003. — № 9.
10. Diabetic Foot Problems: Inpatient Management of Diabetic Foot Problems // NICE Clinical Guidelines, No. 119. — March, 2011. — 574 p. — online access http://www.ncbi.nlm.nih.gov/books/NBK82350/pdf/TOC.pdf.

/60/60.jpg)