Журнал «Медицина неотложных состояний» 6 (61) 2014
Вернуться к номеру
Коррекция гиповолемии у хирургических больных с использованием комбинированного раствора Гекотон® в комплексе инфузионной терапии
Авторы: Гриценко С.Н., Корогод С.Н. - ГУ «Запорожская медицинская академия последипломного образования МЗ Украины», кафедра анестезиологии и интенсивной терапии; Пуха И.П. - Запорожская областная клиническая больница
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
В статье рассматривается вопрос оптимизации инфузионной терапии с включением комбинированного, полиэлектролитного, коллоидно-гиперосмолярного раствора нового поколения (Гекотон®) для коррекции гиповолемии при обезвоживании у хирургических больных. Проведенное исследование показало, что использование раствора Гекотон® в дозе 400 мл в течение 3 суток в комбинации с кристаллоидами у хирургических больных со 2-й степенью дегидратации позволило корригировать гиповолемию, стабилизировать гемодинамические показатели и устранить признаки обезвоживания на вторые сутки.
У статті розглядається питання оптимізації інфузійної терапії з включенням комбінованого, поліелектролітного, колоїдно-гіперосмолярного розчину нового покоління (Гекотон®) для корекції гіповолемії при зневодненні в хірургічних хворих. Проведене дослідження показало, що використання розчину Гекотон® в дозі 400 мл упродовж 3 діб у комбінації з кристалоїдами в хірургічних хворих з 2-м ступенем дегідратації дозволило коригувати гіповолемію, стабілізувати гемодинамічні показники й усунути ознаки зневоднення на другу добу.
The paper deals with a problem of optimizing of infusion therapy included combined multiple electrolyte, colloid osmotic solution of a new generation (Geсoton®) for hypovolemia treatment the dehydrated patients after surgery. The study demonstrated that Gecoton® used 400 ml during 3 days combined with crystalloid solutions in surgical patients with 2 grade dehydration allowed treat hypovolemia, normalize hemodynamic parameters and reduce dehydration symptoms on the 2nd day.
гиповолемия, обезвоживание, инфузионная терапия, Гекотон®.
гіповолемія, зневоднення, інфузійна терапія, Гекотон®.
hypovolemia, dehydration, infusion therapy, Gecoton.
Статья опубликована на с. 63-66
Инфузионно-трансфузионная терапия кристаллоидными и коллоидными растворами повсеместно применяется в практике критической медицины. Многие авторы отмечают положительные свойства коллоидов, например, раствор гидроксиэтилкрахмала (ГЭК) 130/0,42 уменьшает капиллярную утечку [1]. Применение ГЭК при тяжелых травмах ассоциировалось с увеличением внутрисосудистого объема в большей степени, чем при использовании кристаллоидов [2]. В то же время Т.Р. Simon с соавт. считают, что растворы ГЭК при сравнении с кристаллоидами более эффективны для поддержания объема циркулирующей плазмы (ОЦП), среднего артериального давления, системной и тканевой оксигенации. Инфузия ГЭК приводит к специфическим нарушениям коагуляционного гемостаза, с изменением вязкости и реологических свойств крови, а также к активации фибринолиза. ГЭК ингибируют повреждающий эффект активированных нейтрофилов в зависимости от степени выраженности воспалительного ответа [3]. При этом ГЭК 130/0,42 оказывал достоверно меньший эффект на коагуляцию, чем ГЭК 200/0,5, особенно на АЧТВ и фактор von Willebrand [4]. Имеются сведения о том, что сбалансированные солевые растворы предпочтительны для объемного восполнения ОЦП, однако в то же время недостаточно доказательств их эффективности и безопасности в сравнении [5].
Но в последнее время появились данные о неблагоприятных результатах использования ГЭК, в частности, у больных с септическим шоком [6]. Имеются данные об увеличении риска смерти, острого повреждения почек и необходимости применения почечной заместительной терапии при использовании растворов ГЭК для волемической поддержки [7–9]. Использование 6% раствора ГЭК (130/0,42) в сравнении с Рингера ацетатом связано с увеличением смертности в течение 90 дней (р = 0,03) и на 35 % повышает необходимость в почечной заместительной терапии [10]. Однако нет доказательств неблагоприятного воздействия на почки и увеличение смертности (p = 0,079) при использовании тетракрахмала периоперационно [11]. Кроме того, нет достаточно данных о подобных неблагоприятных эффектах у хирургических пациентов и пациентов с гиповолемией. Исследование CRISTAL показало, что у пациентов с гиповолемией лечение коллоидами обеспечивает снижение 90-дневной летальности по сравнению с применением кристаллоидов. Коллоиды традиционно используются для увеличения внутрисосудистого объема, но сейчас требуются доказательства относительно их клинической целесообразности [12]. Поэтому Комитет по оценке степени фармакологического риска (PRAC) Европейского медицинского агентства (ЕМА), учитывая мнение Jean-Louis Vincent и Daniel De Backer, в 2013 г. рекомендовал использовать растворы ГЭК для лечения гиповолемии вследствие острой кровопотери. Выявленное преимущество коллоидов в отношении выживаемости нуждается в дальнейшем изучении. В то же время нельзя однозначно утверждать о преимуществе кристаллоидов по сравнению с коллоидами. Очевидно, необходимо продолжать исследования, свидетельствующие о положительных свойствах гиперосмолярных растворов и растворов ГЭК. Известны преимущества восполнения внесосудистого дефицита жидкости кристаллоидами и в то же время их недостаточный эффект для устранения внутрисосудистого дефицита [14]. Поэтому в состав инфузионной терапии (волемической ресусцитации) включен комбинированный, полиэлектролитный, коллоидно-гиперосмолярный раствор нового поколения Гекотон®; действующие вещества: 100 мл раствора содержат гидрокси-этилкрахмала 130/0,4 — 5000 мг, ксилитола 5000 мг, натрия лактата 1500 мг, натрия хлорида 800 мг, калия хлорида 30 мг, кальция хлорида 20 мг, магния хлорида 10 мг; вспомогательные вещества: вода для инъекций.
Цель исследования: оптимизация инфузионной терапии с включением комбинированного, полиэлектролитного, коллоидно-гиперосмолярного раствора нового поколения Гекотон®, производитель ООО «Юрия-Фарм», для коррекции гиповолемии при обезвоживании у хирургических больных.
Критерии включения: лечение гиповолемии у хирургических пациентов; мужчины и женщины в возрасте 35–60 лет; согласие больного на участие в исследовании.
Критерии исключения: повышенная чувствительность к действующим веществам; гипергидратация, гиперволемия; почечная недостаточность (креатинин > 177 мкмоль/л); гипокоагуляция, гипофибриногенемия, тромбоцитопения; отеки, гипертоническая болезнь III ст.; сердечно-сосудистая декомпенсация, хронические заболевания печени.
Материал и методы исследования
Обследовано и пролечено 37 пациентов.
Клиническое обследование пациентов включало оценку показателей системной гемодинамики: частоты сердечных сокращений (ЧСС, мин–1), среднего артериального давления (САД, мм рт.ст.), центрального венозного давления (ЦВД, мм рт.ст.). Степень обезвоживания оценивали пробой на гидрофильность тканей по П.И. Шелестюку (ПГТШ, минуты) [13]. Состояние гемостаза оценивали по следующим показателям: протромбиновому индексу (ПТИ, %), количеству тромбоцитов крови (x 109/л), фибриногену (г/л), международному нормализованному отношению (МНО, единицы), активированному частичному тромбопластиновому времени (АЧТВ, секунды). Функцию почек изучали по показателям суточного диуреза и креатинина крови (мкмоль/л). Исследовали показатели общего белка (г/л), амилазы (ед.), гемоглобина (г/л), гематокрита (л/л). Динамика показателей отражена поэтапно: 1-й этап — исходные показатели у пациентов и первое применение раствора Гекотон® в составе инфузионной терапии; 2-й этап — через 24 часа, второе использование раствора Гекотон®; 3-й этап — 48 часов, третье использование раствора Гекотон®; 4-й этап — 72 часа; 5-й этап — 96 часов от начала исследования. Статистическая обработка выполнена методом вариационной статистики с оценкой достоверности по t-критерию Стьюдента с помощью программы Statistica, версия 6.1.
Результаты исследований и обсуждение
В табл. 1 приведены показатели гемодинамики на этапах исследования. У больных при поступлении имелись проявления обезвоживания и гиповолемии: жажда, сухость слизистых и кожных покровов, снижение тургора подкожной клетчатки и суточного диуреза (743,5 ± 61,0 мл). САД регистрировали в пределах референтных значений — 91,9 ± 13,2 мм рт.ст.; тахикардия — ЧСС 91,7 ± 20,1 в минуту, ЦВД с среднем составило 0,92 ± 1,08 мм рт.ст.
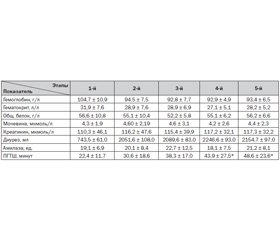
В табл. 2 приведены лабораторные показатели. Отмечено снижение гематокрита до 31,9 ± 7,6 л/л, что нехарактерно для обезвоживания и связано с постгеморрагической анемией у пациентов — гемоглобин составил 104,7 ± 10,9 г/л, поэтому использовать гематокрит для оценки степени обезвоживания в исследовании нецелесообразно. Для этого применили пробу на гидрофильность тканей по П.И. Шелестюку, при которой исходно имело место укорочение времени до 22,4 ± 11,7 минуты, что соответствовало 2-й степени обезвоживания (расчетный объем инфузии кристаллоидов по П.И. Шелестюку для устранения обезвоживания — 5,6–8,4 литра в сутки.
Перед введением гиперосмолярного раствора пациентам проводили инфузию 400 мл раствора Рингера. Далее вводили Гекотон® ежедневно в течение 3 суток в рекомендуемой производителем средней суточной дозе 400 мл со скоростью 200 мл в час, с последующей инфузией кристаллоидов в течение суток. К концу первых суток в среднем введено 2433,33 ± 238,80 мл кристаллоидов. При этом САД было в пределах референтных значений — 93,9 ± 9,9 мм рт.ст., ЧСС снизилась до 84,9 ± 12,9 в минуту, ЦВД повысилось до 3,99 ± 2,60 мм рт.ст. (p < 0,05), суточный диурез возрос и достиг в среднем 2051,6 ± 108,0 мл, что свидетельствовало об устранении проявлений гиповолемии. Время ПГТШ удлинилось до 30,6 ± 18,6 минуты, что соответствовало 1-й степени обезвоживания.
На вторые сутки введено в среднем 2014,29 ± 114,20 мл кристаллоидов. САД составило 94,6 ± 8,2 мм рт.ст., ЧСС не изменилась (84,6 ± 19,5 в минуту) по сравнению с предыдущим этапом, ЦВД возросло в среднем до 5,11 ± 2,79 мм рт.ст. (p < 0,05), суточный диурез не снизился — 2089,6 ± 83,0 мл, а время ПГТШ удлинилось в среднем до 38,3 ± 17,0 минуты (p < 0,05), что свидетельствовало об устранении проявлений обезвоживания.
На третьи сутки объем кристаллоидов сократили до 1455,0 ± 155,6 мл вследствие возможности энтерального восполнения жидкости пациентами. При этом САД составило 97,9 ± 8,5 мм рт.ст., ЧСС снизилась до 80,8 ± 10,2 в минуту (p < 0,05), ЦВД в среднем составило 4,40 ± 3,14 мм рт.ст. (p < 0,05), суточный диурез достаточен (2246,6 ± 93,0 мл), время ПГТШ удлинилось до 43,9 ± 27,5 минуты (p < 0,05).
На четвертые сутки исследуемые показатели находились в пределах референтных значений: САД — 97,8 ± 8,1 мм рт.ст., ЧСС — 75,8 ± 9,7 в минуту (p < 0,05), ЦВД — 7,16 ± 2,88 мм рт.ст. (p < 0,05), суточный диурез — 2154,7 ± 97,0 мл, а время ПГТШ — 48,6 ± 23,6 минуты (p < 0,05).
Изменения показателей концентрации креатинина и амилазы на этапах исследования недостоверны, что свидетельствовало об отсутствии нарушений функции почек и поджелудочной железы. Проведения заместительной почечной терапии не потребовалось.
В табл. 3 приведены некоторые показатели, характеризующие гемостаз на этапах исследования. На 1-м этапе не выявлено изменений лабораторных показателей гемостаза, которые находились в пределах референтных значений, кроме фибриногена, составившего 3,8 ± 1,3 г/л. На 5-м этапе количество тромбоцитов составило (253,1 ± 119,1)•109/л, МНО — 1,20 ± 0,32, ПТИ — 90,1 ± 21,4 %, фибриноген — 4,3 ± 1,6 г/л, но эти отличия не были достоверными. Также имело место недостоверное снижение показателя АЧТВ (34,8 ± 13,6 с).
Выводы
1. Использование раствора Гекотон® в дозе 400 мл в течение 3 суток в комбинации с кристаллоидами у хирургических больных со 2-й степенью дегидратации позволило корригировать гиповолемию, стабилизировать гемодинамические показатели и устранить признаки обезвоживания на вторые сутки.
2. Не выявлено изменений в исследуемых показателях гемостаза, а также нарушений функции почек, что свидетельствует о безопасности раствора Гекотон®.
3. Таким образом, приведенные данные свидетельствуют о целесообразности применения комбинированного инфузионного раствора Гекотон® для периоперационной инфузионной терапии больных хирургического профиля.
1. Simon T.P., Schuerholz T., Haugvik S.P. et al. High molecular weight hydroxyethyl starch solutions are not more effective than a low molecular weight hydroxyethyl starch solution in a porcine model of septic shock // Minerva Anestesіol. — 2013. — 79(1). — 44–52.
2. Zaar M., Lauritzen В., Secher N.H. Initial administration or hydroxyethyl starch vs lactated Ringer after liver trauma in the pig // Br. J. Anaesth. — 2009. — 102(2). — 221–6.
3. Matharu N.M., Butler L.M., Rainger G.E. et al. Mechanisms of the anti-inflammatory effects of hydroxyethyl starch demonstrated in a flow-based model of neutrophil recruitment by endothelial cells // Crit. Care Med. — 2008. — 36(5). — 1536–42.
4. Kozek-Langenecker S.A., Jungheinrich C. et al. The effects of hydroxyethyl starch 130/0.4 (6%) on blood loss and use of blood products in major surgery: a pooled analysis of randomized clinical trials // Anesth. Analg. — 2008. — 107(2). — 382–90.
5. Myburgh J.A., Mythen M.G. Resuscitation Fluids // N. Engl. J. Med. — 2013. — 369. — 1243–51.
6. Van Der Linden P., James M., Mythen M., Weiskopf R.B. Safety of modern starches used during surgery // Anesth. Analg. — 2013. — 116(1). — 35–48.
7. Gattas D.J., Dan A., Myburgh J. et al., CHEST Management Committee. Collaborators (18) Fluid resuscitation with 6% hydroxyethyl starch (130 0.4 and 130 0.42) in acutely ill patients: systematic review of effects on mortality and treatment with renal replacement therapy // Intensive Care Med. — 2013. — 39(4). — 558–68.
8. Gillies M.A., Habicher M., Jhanji S. et al. Incidence of postoperative death and acute kidney injury associated with i.v. 6% hydroxyethyl starch use: systematic review and meta-analysis // Br. J. Anaesth. — 2014. — 112(1). — 25–34.
9. Myburgh J.A., Finfer S., Bellomo R. et al. Hydroxyethyl starch or saline for fluid resuscitation in intensive care // N. Engl. J. Med. — 2012. — 367. — 1901–11.
10. Brunkhorst F.M., Engel C., Bloos F. et al. Intensive insulin therapy and pentastarch resuscitation in severe sepsis // N. Engl. J. Med. — 2008. — 358. — 125–39.
11. Van Der Linden P., James M., Mythen M., Weiskopf R.B. Safety of modern starches used during surgery // Anesth. Analg. — 2013. — 116(1). — 35–48.
12. Matharu N.M., Butler L.M., Rainger G.E. et al. Mechanisms of the anti-inflammatory effects of hydroxyethyl starch demonstrated in a flow-based model of neutrophil recruitment by endothelial cells // Crit. Care Med. — 2008. — 36(5). — 1536–42.
14. Стандарти організації професійно орієнтованих протоколів медичної допомоги хворим з невідкладною хірургічною патологією органів живота / За ред. Березницького Я.С., Фоміна П.Д. — К.: Товариство «Доктор-Медіа», 2010. — 470 с.
13. Zampien F.G., Park M., Azevedo L.C. Colloids in sepsis: evenly distributed molecules surrounded by uneven questions // Shock. — 2013. — 39 Suppl 1. — 42–9.

/64/64.jpg)
/65/65.jpg)