Международный неврологический журнал 7 (69) 2014
Вернуться к номеру
Клінічна характеристика когнітивних порушень у пацієнтів із хронічним обструктивним захворюванням легень
Авторы: Поясник І.М. — Iвано-Франківський обласний фтизіопульмонологічний центр
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
У статті подані результати дослідження когнітивних порушень у пацієнтів із хронічним обструктивним захворюванням легень. Діагноз когнітивних розладів базувався на результатах розширеного нейропсихологічного обстеження з якісною та кількісною оцінкою отриманих результатів. У пацієнтів із хронічним обструктивним захворюванням легень ІІІ–ІV стадії виявлено синдром легких і помірних когнітивних розладів порівняно з практично здоровими особами тієї ж вікової категорії.
В статье представлены результаты исследования когнитивных нарушений у пациентов с хроническим обструктивным заболеванием легких. Диагноз когнитивных расстройств базировался на результатах расширенного нейропсихологического обследования с качественной и количественной оценкой полученных результатов. У пациентов с хроническим обструктивным заболеванием легких ІІІ–ІV стадии выявлен синдром легких и умеренных когнитивных расстройств по сравнению с практически здоровыми лицами той же возрастной категории.
The article deals with the results of study of cognitive disorders in patients with chronic obstructive pulmonary diseases. Diagnosis of cognitive disorders was based on the results of the extended neuropsychological examination with qualitative and quantitative evaluation of the results. The patients with the chronic obstructive pulmonary disease of III–IV stage were found to have syndrome of mild and moderate cognitive disorders in comparison with the practically healthy persons of identical age category.
хронічне обструктивне захворювання легень, когнітивні розлади, венозна енцефалопатія.
хроническая обструктивная болезнь легких, когнитивные расстройства, венозная энцефалопатия.
chronic obstructive pulmonary disease, cognitive disorders, venous encephalopathy.
Статья опубликована на с. 31-34
Хронічне обструктивне захворювання легень (ХОЗЛ) залишається однією з найважливіших проблем охорони здоров’я як у нашій країні, так і в усьому світі. Це виснажлива хвороба, при якій утруднене дихання, кашель, задишка при фізичних навантаженнях, хрипи є повільно прогресуючими симптомами, що в кінцевому підсумку призводять до функціональних порушень, пригнічення пацієнтів, високих показників інвалідності, смертності, вельми значного економічного й соціального збитку, причому рівень його зростає. Актуальність цієї проблеми обумовлена також надзвичайно високими показниками поширеності. У світі близько 9–10 % населення хворіють на ХОЗЛ. Проблема ХОЗЛ на сьогодні стає ще більш гострою через несвоєчасне виявлення захворювання, а часто й неадекватне лікування [1–3, 7].
Супутні захворювання, що часто виникають у пацієнтів із ХОЗЛ, включають серцево-судинні захворювання, метаболічний синдром, дисфункцію скелетних м’язів, остеопороз, анемію, діабет, синдром обструктивного апное-гіпопное сну, рак легень, депресію, розлади, що можуть суттєво погіршити прогноз [6, 9]. Супутня патологія при ХОЗЛ виникає при різних ступенях тяжкості захворювання [12] і вимагає спеціального лікування [11].
Одним з основних ускладнень ХОЗЛ є легенева недостатність (ЛН). ЛН — це нездатність легень забезпечити нормальний газовий склад артеріальної крові в стані спокою або при помірному фізичному навантаженні. Основними механізмами патогенезу при цьому є обструкція дихальних шляхів, рестрикція альвеол, дифузійні розлади, порушення легеневого кровотоку, скорочення функціонуючої легеневої тканини [5]. ЛН — складова частина більш загального патологічного стану, а саме дихальної недостатності, у патогенезі якої додатково беруть участь позалегеневі фактори (порушення центральної регуляції дихання, порушення нервово-м’язової передачі імпульсу, патологія м’язів, грудної стінки, системи крові, кровообігу, пригнічення тканинного дихання) [10]. У результаті дисфункції правих відділів серця, підвищення внутрішньогрудного тиску, застою у верхній порожнистій вені, при кашлі, утрудненому вдиху виникають умови для розвитку венозної гіперемії головного мозку [16].
Центральна нервова система раніше за інші органи та тканини реагує навіть на незначну кисневу недостатність. Гіпоксія рано проявляється не лише розладом функції, а й порушенням будови різних клітин мозку (нейрони, глія) і синаптичних структур. У відповідь на кисневе голодування включаються різні компенсаторні механізми, проте при вираженій гіпоксії компенсаторна дія цих чинників відносно нетривала. У головному мозку розвиваються глибокі порушення обміну, виникають набряк, венозний застій і дисциркуляція [4]. У наш час наявні поодинокі дослідження, у яких автори вивчали порушення функцій головного мозку в міру наростання респіраторних розладів. Відсутні праці, у яких була б досліджена динаміка формування когнітивних і афективних розладів у хворих із ХОЗЛ.
Матеріали та методи дослідження
Проведено комплексне клініко-неврологічне дослідження 120 хворих на ХОЗЛ ІІ–ІV стадій. Була діагностована венозна енцефалопатія у хворих із ХОЗЛ ІІІ–ІV стадій. Діагностика клінічних проявів порушень венозного відтоку з порожнини черепа проводилась із використанням робочої класифікації М.Я. Бердичевського (1989). Усі обстежені пацієнти були розподілені на групи залежно від стадії ХОЗЛ:
— перша група — 60 пацієнтів (середній вік — 53,38 ± 5,1 року; жінок — 20, чоловіків — 40) із ХОЗЛ ІІ стадії;
— друга група — 40 пацієнтів (середній вік — 55,8 ± 5,5 року; жінок — 4, чоловіків — 36) із ХОЗЛ ІІІ стадії;
— третя група — 20 пацієнтів (середній вік — 58,65 ± 8,09 року; жінок — 1, чоловіків — 19) із ХОЗЛ ІV стадії;
— четверта група (контрольна) — 25 пацієнтів (середній вік — 54,36 ± 3,12 року; жінок — 10 , чоловіків — 15) — практично здорові особи.
Оцінку когнітивного статусу проводили скринінговим методом за допомогою шкали MMSE (Mini Mental State Examination), що містить низку субтестів, які дають змогу оцінити стан короткотривалої й тривалої пам’яті, орієнтування в просторі та часі, мовну функцію, гнозис та праксис. Максимальний бал 30 відповідає найбільш високому когнітивному рівню, 28–30 балів — немає когнітивних порушень, 24–27 балів — переддементні порушення, 20–23 бали — деменція легкого ступеня, 11–19 балів — помірна деменція, 0–10 балів — тяжкі дементні порушення [15]. Детальне нейропсихологічне обстеження провели з використанням низки додаткових тестів. Монреальська шкала оцінки когнітивних функцій (МоСА) дає змогу швидко оцінити помірні когнітивні розлади (< 26 балів). Порушення виконавчих функцій оцінювали за допомогою батареї тестів на лобну дисфункцію (FAB), що запропонував французький невролог Дюбуа. У FAB входять завдання на оцінку здатності до концептуалізації, визначення швидкості мовлення, простої та ускладненої реакції вибору, оцінка динамічного праксису, дослідження хапальних рефлексів (максимальна оцінка за цією шкалою 18 балів). Увагу та швидкість сенсомоторних реакцій оцінювали за допомогою таблиць Шульте — 30–40 с (9–10 балів) [15].
Статистична обробка одержаних даних проводилась із застосування пакета прикладних програм Statistica 12.0. Для оцінки статистичної значущості різниці показників між групами застосовували непараметричний критерій Колмогорова — Смирнова для порівняння двох незалежних змінних, проводили кореляційний аналіз із застосуванням коефіцієнта гамма. Вірогідними вважали зміни показників за умови p < 0,05.
Результати та їх обговорення
Вважали, що пацієнти не мають когнітивних порушень (КП), якщо за шкалою MMSE вони набирали 28–30 балів, за шкалою МоСА > 26 балів, при виконанні тестів FAB — 16–18 балів, заповнювали таблиці Шульте за 30–40 с. У хворих із ХОЗЛ ІІ стадії КП були відсутні: загальний бал за шкалою MMSE становив 28 (27; 28) балів (р > 0,1), за шкалою МоСА — 26 (26; 26) балів (р > 0,1); за шкалою FAB — 16 (16; 16) балів (р > 0,1). Статистично вірогідно збільшився час (р < 0,001) заповнення таблиць Шульте порівняно з групою контролю — 217 (216; 220) секунд проти 192 (185; 195) секунд відповідно) (табл. 1).
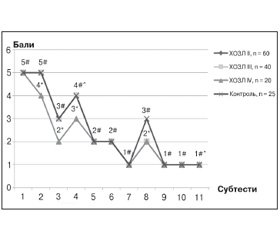
Результати даних нейропсихологічних досліджень у хворих із ХОЗЛ ІІІ стадії свідчили про наявність легких когнітивних порушень. Рівень сатурації крові в пацієнтів даної групи становив 91 (89; 93) % (р < 0,001). Загальний бал за шкалою MMSE вірогідно відрізнявся від групи контролю — 26 (25; 27) балів (р < 0,001) за рахунок субтестів «увага і лічба» (р < 0,05) та «виконання тристадійного завдання» (р < 0,001) (рис. 1). Статистично вірогідною була різниця балів і за шкалою МоСА — 24,5 (24; 25) бала (р < 0,001) за такими субтестами: «мова» (р < 0,001) та «відкладене повторення» (р < 0,001). За шкалою FAB загальний бал становив 14 (14; 15) (р < 0,001), він зменшився за рахунок субтестів «швидкість мови» (р < 0,001), «динамічний праксис» (р < 0,001), «дослідження хапальних рефлексів» (р < 0,05). Час заповнення таблиць Шульте також вірогідно відрізнявся від групи контролю — 254 с (251; 257) (р < 0,001) ( рис. 4).
У хворих із ХОЗЛ IV стадії відмічалось наростання когнітивного дефіциту. Дані нейропсихологічних досліджень свідчили про те, що в пацієнтів із ХОЗЛ IV стадії відзначалися найбільш виражені КП, які відповідали помірним когнітивним розладам. За шкалою MMSE загальний бал зменшився до 23 (23; 24) (р < 0,001) за рахунок субтестів «орієнтування в часі» (р < 0,001), «орієнтування в просторі» (р < 0,001), «запам’ятовування трьох слів» (р < 0,001), «увага і лічба» (р < 0,001), «виконання тристадійного завдання» (р < 0,001), «копіювання малюнка» (р < 0,05). Зменшився загальний бал і за шкалою МоСА — 22 (22; 23) (р < 0,001) за субтестами «зорово-конструктивні навики» (р < 0,001), «увага» (р < 0,001), «мова» (р < 0,001), «відкладене повторення» (р < 0,001), «орієнтація» (р < 0,05) (рис. 2). Загальний бал за шкалою FAB становив 12 (11–12) (р < 0,001), він зменшився за рахунок субтестів «швидкість мови» (р < 0,001), «динамічний праксис» (р < 0,001), «проста реакція» (р < 0,05), «ускладнена реакція вибору» (р < 0,05), «дослідження хапальних рефлексів» (р < 0,001) (рис. 3). Вірогідно збільшився і час заповнення таблиць Шульте — 287 с (285,5; 296,5) (р < 0,001). Сатурація кисню крові становила 83 (81; 85) % (р < 0,001). Був виявлений обернений кореляційний зв’язок середньої сили між рівнем сатурації кисню та показником за таблицями Шульте (r = –0,45; р < 0,05).
Висновки
Проведені нами дослідження засвідчили, що зниження рівня сатурації крові < 91 % може бути одним із чинників виникнення венозної енцефалопатії та відповідних когнітивних порушень у пацієнтів із ХОЗЛ. У міру прогресування ХОЗЛ, на ІІІ–ІV стадії, відмічається наростання когнітивного дефіциту, порушення активної уваги, вербальної пам’яті, страждають відкладене повторення, динамічний праксис. Це підтверджують отримані нами дані: формування помірних когнітивних розладів у хворих із ХОЗЛ ІІІ–ІV стадії та наявність кореляції між рівнем когнітивних розладів і рівнем сатурації кисню. Тому ідентифікація факторів ризику розвитку когнітивних розладів у таких хворих може відігравати істотну роль у профілактиці й лікуванні цього супутнього стану, а також дасть змогу покращити щоденний догляд за пацієнтами.
1. Фещенко Ю.И. Хроническое обструктивное заболевание легких — актуальная медико-социальная проблема // Укр. пульмонол. журнал. — 2011. — № 2. — С. 6.
2. Halbert R.J. et al. Global burden of COPD: systematic review and meta-analysis // Eur. Respir. J. — 2006. — № 28. — Р. 523–532.
3. National Institutes of Health National Heart & Lung and Blood Institute. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. — Updated 2013. — 80 р.
4. Гонгальський В.В. О возможности регуляции венозного оттока из глибоких структур головного мозга // Журнал неврологии и психиатрии им. С.С. Корсакова. — 2005. — № 5. — С. 62–63.
5. D’Mello J., Butani M. // Indian. J. Anaest. — 2002. — Vol. 46(4). — P. 269–278.
6. Depressive symptoms and chronic obstructive pulmonary disease: effect on mortality, hospital readmission, symptom burden, functional status, and quality of life // Arch. Intern. Med. — 2007. — Vol. 167. — P. 60–67.
7. Фещенко Ю.І., Яшина Л.О. Хронічне обструктивне захворювання легень і супутні депресія та розлади сну // Укр. пульмонол. журнал. — 2013. — № 2. — С. 33–40.
8. Gavrysyuk V.K. Printsipy terapii bolnykh s oslozhneniyami KHOZ (Management of patients with COPD complications) // Ukr. Pulmonol. Zhurnal. — 2011. — № 2. — Р. 10–12.
9. Barnes P.J. Systemic manifestations and comorbidities of COPD // Eur. Respir. J. — 2009. — Vol. 33. — P. 1165–1185.
10. Gavrysyuk V.K. et al. Klinicheskaya klassifikatsiya dykhatelnykh і gemo-dinamicheskikh narusheniy pri zabolevaniyakh legkikh (Clinical classifi–cation of respiratory and circulation disorders in lung diseases) // Ukr. Pulmonol. Zhurnal. — 2003. — № 1. — Р. 30–22.
11. Globalstrategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease // National Institutes of Health National Heart & Lung and Blood Institute. — Updated 2013. — 80 р.
12. Agusti A. Characterisationof COPD heterogeneity in the ECLIPSE cohort // Respir. Res. — 2010. — Vol. 11. — Р. 122.
13. Maurer J. et al. Anxiety and depression in COPD: current understanding, unanswered questions, and research needs // Chest. — 2008. — Vol. 134, Suppl. 4. — P. 43–56.
14. Фещенко Ю.І. Хронічне обструктивне захворювання легень та супутня депресія — важлива медико-соціальна проблема // Український пульмонологічний журнал. — 2013. — № 3. Додаток. — С. 56–58.
15. Міщенко Т.С., Шестопалова Л.Ф. Клінічні шкали і психодіагностичні тести в діагностиці судинних захворювань головного мозку: Метод. рекомендації. — Х.: ВІПОЛ, 2008. — 36 с.
16. Мarra C. Cognitive impairment in chronic obstructive pulmonary disease — a neuropsychological and SPECT study // J. Neurol. — 2003. — № 23. — Р. 325–332.

/32/32.jpg)
/33/33.jpg)