Журнал «Медицина неотложных состояний» 8 (63) 2014
Вернуться к номеру
Рівень глікемії як показник адекватності анестезії при аденотомії в дітей
Авторы: Пушкар М.Б., Георгіянц М.А. — Харківська медична академія післядипломної освіти МОЗ України
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
У статті проведено порівняння адекватності різних способів анестезій шляхом оцінки рівня глюкози крові при аденотомії в дітей. Було виявлено, що при аденотомії в умовах загальної анестезії, яка проводилася пропофолом та севофлюраном з використанням фентанілу, забезпечується ефективне інтраопераційне знеболювання без істотних коливань рівня глікемії. Комплексне дослідження рівня глікемії в поєднанні з вивченням реакцій больової відповіді в дітей обох груп продемонструвало, що використання ібупрофену в дозі 10 мг/кг з метою післяопераційного знеболювання сприяє адекватній післяопераційній аналгезії.
В статье проведено сравнение адекватности различных способов анестезии путем оценки уровня глюкозы крови при аденотомии у детей. Было выявлено, что при аденотомии в условиях общей анестезии, которая проводилась пропофолом и севофлюраном с использованием фентанила, обеспечивается эффективное интраоперационное обезболивание без существенных колебаний уровня гликемии. Комплексное исследование уровня гликемии в сочетании с изучением реакций болевого ответа у детей обеих групп показало, что использование ибупрофена в дозе 10 мг/кг с целью послеоперационного обезболивания приводит к адекватной послеоперационной аналгезии.
In this article, the adequacy of the different methods of anesthesia during adenotomy in children was compared by measuring blood glucose levels. It was found that during adenotomy under general anesthesia, which was conducted with propofol and sevoflurane using fentanyl, the effective intraoperative analgesia is provided without any significant fluctuations of the blood glucose levels. A comprehensive study of the level of glycemia in conjunction with the study of the pain reactions in children in both groups showed that the use of ibuprofen at a dose of 10 mg/kg for the purpose of postoperative anesthesia leads to adequate postoperative analgesia.
аденотомія, глікемія, внутрішньовенна анестезія, інгаляційна анестезія.
аденотомия, гликемия, внутривенная анестезия, ингаляционная анестезия.
adenotomy, glycemia, intravenous anesthesia, inhalation anesthesia.
Статья опубликована на с. 93-95
Введення
Гіпертрофія носоглоткової мигдалини є найбільш поширеною причиною закладеності носа в дітей. Аденотомія з проведенням тонзилектомії або без неї залишається одним із найбільш часто виконуваних хірургічних втручань в оториноларингологічній практиці. Анестезія при аденотомії покликана забезпечити достатню періопераційну аналгезію, надання якісного хірургічного доступу з метою спільного використання дихальних шляхів анестезіологом та хірургом, запобігання післяопераційній нудоті та блювоті [1].
Операційний стрес викликає в організмі дитини відповідну реакцію з боку різних систем: нервової, імунної, нейроендокринної, метаболізму [2–4]. Не варто забувати, що сам наркоз ще до приєднання операційної травми призводить до змін гомеостазу і фактично є компонентом операційного стресу [5]. Для оцінки адекватності анестезії використовують різні показники: стан центральної гемодинаміки, рівень стресових гормонів, рівень глюкози, вільних жирних кислот. Одним із проявів хірургічного стресу є зміна метаболізму глюкози як наслідок дії глюкокортикоїдів на вуглеводний обмін (гіперглікемія є наслідком глюконеогенезу та гальмування окислення глюкози у тканинах). Деякі автори вважають, що рівень плазмової концентрації глюкози може бути досить якісним індикатором рівня операційного стресу [6].
Дослідження маркерів стресу досі залишається актуальним, бо саме його результати є об’єктивним підтвердженням адекватності антиноцицептивного захисту пацієнта від операційного стресу.
Мета дослідження — порівняння рівня глюкози крові при аденотомії в дітей в умовах різних способів загальної анестезії.
Матеріали та методи
Дослідження виконано на базі Комунального закладу охорони здоров’я «Обласна дитяча клінічна лікарня» м. Харкова. До нього увійшли 55 дітей віком від 6 до 11 років, яким була проведена аденотомія. Ступінь операційно-наркозного ризику у всіх пацієнтів відповідав I за ASA.
До дослідження не входили діти молодше 5 років і старше 12 років; оперативні втручання на лор-органах за винятком аденотомії; фізичний статус ASA III–IV; наявність тяжкої хронічної патології, що супроводжується порушеннями системного метаболізму та функціонування інших органів і систем; наявність органічного або функціонального ураження центральної нервової системи.
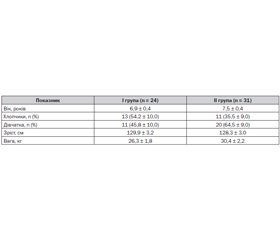
Залежно від способу проведеної анестезії пацієнти були розподілені на дві групи. У I групу (n = 24) увійшли пацієнти, оперовані в умовах внутрішньовенної анестезії на основі пропофолу. У II групу (n = 31) увійшли пацієнти, оперовані в умовах інгаляційної анестезії севофлюраном. Середній вік пацієнтів I групи становив 6,9 ± 0,4 року, II групи — 7,5 ± 0,4 року (p > 0,05). За статтю діти розподілилися у групах так: I група — 54,2 ± 10,9 % хлопчиків, 45,8 ± 10,0 % дівчаток, II група — 35,5 ± 9,0 % хлопчиків, 64,5 ± 9 % дівчаток. За кількістю хлопчиків та дівчаток групи не відрізнялися (p > 0,05). Середня тривалість оперативного втручання у I групі — 7,7 ± 0,5 хвилини, а у другій — 9,2 ± 0,6 хвилини, статистичної різниці між групами не було (p > 0,05). Пацієнти порівнюваних груп також вірогідно не відрізнялися за зростом, вагою та обсягом оперативного втручання (табл. 1).
У I групі індукцію анестезії виконували з використанням 1% розчину пропофолу (2,5–3 мг/кг), підтримання здійснювали фракційним введенням пропофолу з розрахунку (1 мг/кг), приблизно через 2,5–3 хвилини після попереднього введення.
У II групі індукцію анестезії здійснювали севофлюран-кисневою сумішшю болюсною методикою без попереднього заповнення дихального контура 8 об% севофлюрана при потоці кисню 4 л/хв. Після досягнення клініки хірургічної стадії наркозу підтримання анестезії здійснювали подачею 2–2,5 об% севофлюрана при потоці свіжого газу 2 л/хв. Використовували наркозно-дихальний апарат МК-1 («Респект-Плюс», Білорусь).
В обох групах міорелаксація забезпечувалася дитиліном (2 мг/кг). У I групі аналгезія інтраопераційно забезпечувалася фентанілом (2 мкг/кг), а у II групі аналгезія здійснювалася поєднанням фентанілу (2 мкг/кг) з анальгіном (8–10 мг/кг). Із метою профілактики нудоти та блювоти пацієнтам обох груп інтраопераційно вводили ондансетрон (0,1 мг/кг), а пацієнтам II групи — у поєднанні з дексаметазоном (0,1–0,15 мг/кг). Післяопераційне знеболювання в обох групах проводилося пероральною дачею нестероїдного протизапального препарату ібупрофен (10 мг/кг).
При проведенні оперативного втручання проводився періопераційний моніторинг, що включав: пульсоксиметрію, вимірювання частоти серцевих скорочень, середнього артеріального тиску, капнометрію, варіабельність ритму серця (монітор UM-300, Україна).
Оцінка ефективності знеболювання в ранньому післяопераційному періоді проводилась за допомогою шкали Wong and Baker FACES Pain Scale («Обличчя»), поведінкової шкали FLACC (Face, Legs, Activity, Cry, and Consolability) і шкали Oucher.
Рівень глікемії визначався глюкозооксидазним методом. Забір крові для біохімічних досліджень здійснювався на наступних етапах: 1-му — перед операцією; 2-му — травматичний момент операції; 3-му — екстубація; 4-му — через 20 годин після операції. У періопераційному періоді інфузія глюкози пацієнтам не проводилася.
Статистична обробка даних здійснювалася з використанням значень t-критерію Стьюдента. Відмінності вважалися вірогідними при р < 0,05.
Результати та їх обговорення
Передопераційні показники глікемії в обох групах не виходили за межі лабораторної норми і становили в середньому 3,6 ± 0,2 ммоль/л в I групі і 3,7 ± 0,2 ммоль/л у II групі та між групами не відрізнялись (p > 0,05) (табл. 2). На етапі травматичного моменту операції показники рівня глюкози крові в групах дещо підвищувалися — до 4,0 ± 0,1 ммоль/л та 4,1 ± 0,3 ммоль/л відповідно та між групами також не відрізнялись (p > 0,05). Після екстубації в I групі підвищення показника глікемії відбувалось у межах нормальних значень — 4,8 ± 0,1 ммоль/л, проте він був статистично вищим від рівня на етапі травматичного моменту операції (p < 0,001). У II групі показник глікемії становив 4,5 ± 0,2 ммоль/л, однак статистично значущої різниці порівняно з травматичним моментом операції не відзначалося (p > 0,05); статистичної різниці між групами також не відмічалось (p > 0,05). Звертає на себе увагу, що показники глікемії на етапі екстубаціі в обох групах були статистично вищими від передопераційних значень (p < 0,001 і p < 0,01 відповідно). Наступного ранку після операції відзначалася тенденція до зниження показників глікемії в обох групах, що не виходили за межі норми. Ми не виявили статистично значущої різниці між групами на заключному етапі дослідження (p > 0,05).
Середня інтенсивність больового синдрому через 1 годину після операції в групах становила 1,0 ± 0,3 бала і 1,5 ± 0,2 бала відповідно за шкалою «Обличчя» (картинка «трохи болить»). На цьому етапі статистично вірогідної різниці між групами за шкалою «Обличчя» не відзначалося (p > 0,05). У динаміці спостереження на наступних етапах дослідження за шкалою «Обличчя» в обох групах відзначалась тенденція до зниження інтенсивності больового синдрому (картинка «не болить»), проте статистично значущої різниці між групами не реєструвалося (p > 0,05) (табл. 3).
Звертає на себе увагу те, що в ранньому післяопераційному періоді середня інтенсивність больового синдрому за шкалою Oucher через 1 годину після операції була більш вираженою у хворих II групи — 1,8 ± 0,3 бала, у I групі — 0,5 ± 0,2 бала (p < 0,001), незважаючи на інтраопераційне поєднання фентанілу з анальгіном у пацієнтів II групи. За шкалою Oucher надалі на етапах дослідження відзначається тенденція до зниження інтенсивності больового синдрому, у той же час інтенсивність болю в групах відповідає картинці «не болить». Статистично значущої різниці між групами не відзначалося (p > 0,05).
За даними поведінкової шкали FLACC за весь час спостереження між групами не відзначалося вірогідної різниці (p > 0,05), інтерпретація балів на всіх етапах дослідження за даною шкалою говорить про те, що пацієнти в обох групах почували себе комфортно.
Таким чином, враховуючи результати цього дослідження, можна припустити, що аденотомія в пацієнтів обох груп в умовах загальної анестезії, яка проводилася пропофолом та севофлюраном із використанням фентанілу, у поєднанні з анальгіном чи без нього, забезпечує ефективну інтраопераційну аналгезію без істотних коливань рівня глікемії.
Висновки
1. Комплексне дослідження рівня глікемії в поєднанні з вивченням реакцій больової поведінки в дітей обох груп продемонструвало, що використання ібупрофену в дозі 10 мг/кг з метою післяопераційного знеболювання сприяє адекватній післяопераційній аналгезії.
2. Хоча рівень глікемії є чутливим показником операційного стресу, він не дозволяє у повному обсязі судити про адекватність антиноцицептивного захисту пацієнта, тому в подальшому необхідне вивчення нейроендокринної реакції, а саме рівня кортизолу та інсуліну в сироватці крові.
1. Strauss L. Anaesthetic management of paediatric adenotonsillectomy // S. Afr. Fam. Pract. — 2012. — Vol 54, № 3, Supplement 1. — 17-20. doi: 10.1080/20786204.2012.10874231.
2. Зильбер А.П. Клиническая физиология в анестезиологии и реаниматологии / А.П. Зильбер. — М.: Медицина, 1984. — C. 113-124.
3. Рябов Г.А. Синдромы критических состояний / Г.А. Рябов. — М.: Медицина, 1994. — С. 84-105, 175-194.
4. Reis F.М. Изменения пролактина и глюкозы в плазме, индуцированные хирургическим стрессом: единая или двойственная реакция? Мини-обзор (Перевод и обработка В. Фесенко) / F.M. Reis, A. Ribeiro-de-Oliveira Jr, L. Machado, R.M. Guerra, A.M. Reis, C.C. Coimbra // Медицина неотложных состояний. — 2008. — № 5(18). — С. 108-114.
5. Chumbley G.M., Hall G.M. Recovery after major surgery: does the anesthetic make any difference? // Br. J. Anaesth. — 1997. — 78. — 347-349. doi: 10.1093/bja/78.4.347.
6. Карелов А.Е. Особенности хирургического стресса при пуринергической анальгезии: Автореф. дис… на соискание ученой степени канд. мед. наук: 14.00.37, 14.00.16 / Карелов Алексей Евгеньевич; Санкт-Петербург. гос. педиатр. мед. академия. — СПб., 2004. — 19 с.

/94/94.jpg)
/95/95.jpg)