Журнал «Актуальная инфектология» 1 (6) 2015
Вернуться к номеру
Лямбліоз: обстеження і терапія хворих у сучасних умовах
Авторы: Бодня К.І., Мочалова Г.О., Кадельник Л.О. — Харківська медична академія післядипломної освіти;
Національний медичний університет ім. О.О. Богомольця, м. Київ
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 27-33
Першочергова проблема охорони здоров’я в країні, як і раніше, — це реформування медицини. Реформування системи первинної медико-санітарної допомоги на засадах загальної практики — сімейної медицини має забезпечити вдосконалення системи медичної допомоги, наблизити її до кожної сім’ї.
У системі боротьби з паразитарними хворобами суттєву роль відіграють амбулаторно-поліклінічні установи, у тому числі амбулаторії сімейної медицини [1, 10]. Сімейний лікар повинен здійснювати діагностику, надавати первинну допомогу і, що особливо важливо, проводити первинну профілактику паразитарних хвороб.
У рамках концепції реформи охорони здоров’я визначено, що метою і критерієм управління має бути якість медичної допомоги. Але якість визначається насамперед забезпеченням виявлення захворювань на ранній стадії. Ефективне вирішення проблем профілактики паразитарних хвороб неможливо без спеціальної підготовки лікарів загальної практики з питань клініки і діагностики паразитарних хвороб.
Останніми роками істотно переглядається соціальна значимість паразитарних хвороб. Кишкові протозоози, насамперед лямбліоз, навіть у формі носійства можуть створювати вторинні імунодефіцитні стани, посилювати епідеміологічно несприятливу ситуацію з кишкових бактеріозів, знижувати ефективність вакцинопрофілактики.
Лямбліоз поширений повсюдно. За даними ВООЗ, у світі на лямбліоз щорічно хворіє близько 500 млн осіб, у 500 тис. захворювання проявляється в маніфестній формі. В Україні рівень захворюваності населення на лямбліоз залишається на високому рівні і перевищує такий у провідних країнах Європи в десятки разів.
Останнім часом велика увага приділяється водному шляху передачі лямбліозу. Особливе значення для поширення лямбліозу має висока стійкість цист лямблій до хлору. Звичайне кип’ятіння води не діє на них згубно. Тому вода з водопроводу, що відповідає за санітарними показниками вимогам нормативних документів щодо мікробного забруднення, може служити фактором передачі лямблій.
Лямблії, відповідно до міжнародної класифікації паразитичних найпростіших, належать до підцарства Protozoa, типу Sarcomastigopha, підтипу Mastigophora, класу Zoomastigororea, загону Diplomonadida і роду Giardia (Lamblia).
Існуючі протиріччя щодо номенклатури збудника лямбліозу не подолано до цього часу. Після виділення в 1882 р. Kunstler роду Giardia паразит отримав назву Giardia lamblia, яку використовують англо-американські дослідники. У вітчизняній і європейській літературі закріпилася інша назва — Lamblia intestinalis [28].
Як і в багатьох найпростіших, життєвий цикл лямблій включає вегетативну стадію (трофозоїт) і стадію цисти.
Найбільш важлива з біологічної точки зору перша з них. Лямблії в стадії трофозоїта дуже рухливі. Особливе значення має центральна пара джгутиків. Ці органели є своєрідним насосом, відкачують для свого життєзабезпечення із проміжків мікроворсинок щіткової облямівки продукти мембранного травлення. Це свідчить про вузьку пристосованість лямблій до перебування на поверхні щіткової облямівки епітеліального шару кишечника.
Особливістю будови паразита є недостатній розвиток у трофозоїта гранульованого ендоплазматичного ретикулуму, а також відсутність у нього апарату Гольджі, що дає підставу припускати переважно ендогенне використання синтезованого білка. Це суперечить думці, що лямблії здатні виділяти в зовнішнє середовище високомолекулярні сполуки, зокрема токсини [28].
Крім апарату Гольджі, у цього мікроорганізму немає скорочувальних вакуолей і типових мітохондрій. Відсутність останніх дозволяє припускати, що енергетичний обмін лямблій здійснюється за анаеробним типом, тобто так само, як і в багатьох найпростіших кишечника.
Перетворення трофозоїтів у цисти пов’язано зі зниженням інтенсивності контактного травлення, змінами осмотичного тиску й рН у дистальних відділах кишечника. При цьому інтенсивність виділення цист знаходиться в прямій залежності від масивності їх утворення. Останні не витримують висушування і стійкі до дезінфікуючих речовин, що містять хлор.
Повний цикл інвазії завершується вивільненням з організму хазяїна цист, що в зовнішньому середовищі тривалий час залишаються життєздатними.
Клінічні прояви лямбліозу характеризуються рядом ознак, обумовлених впливом на організм людини як паразитів, так і продуктів їх метаболізму. При цьому значущість клінічних проявів і змін лабораторних показників безпосередньо корелює з інтенсивністю інвазії і станом організму хазяїна.
Частота виникнення лямбліозу може змінюватися при деяких патологічних станах шлунково-кишкового тракту, що сприяють уповільненню або, навпаки, прискоренню біохімічних процесів на мембранах щіткової кайми. У зв’язку з цим мають бути правильно оцінені клінічні дані поєднання лямбліозу з дисфункцією підшлункової залози та печінки [23]. Хворі з подібними порушеннями входять до групи ризику інфікування лямбліями.
Голодування хазяїна різко скорочує чисельність лямблій. Багата вуглеводами дієта сприяє швидкому збільшенню кількості лямблій, переважно білкова дієта пригнічує паразита. Жовч у низьких концентраціях стимулює розвиток та розмноження лямблій, концентрована жовч впливає на лямблії згубно.
Інфекція, що спричиняється Lamblia intestinalis, може перебігати безсимптомно, зі спонтанною елімінацією паразитів і завершуватися через 1–3 місяці. При маніфестному лямбліозі незалежно від характеру перебігу інфекції хворі скаржаться на здуття та урчання у животі, біль в епігастрії, у них виражені явища ентериту та стеатореї. Стеаторея виникає внаслідок порушення всмоктування ліпідів і є одним із небагатьох цілком вірогідних патологічних проявів лямбліозу. За відсутності лікування надійного самовиліковування не відзначається.
Зміни мікроворсинок можуть варіювати у хворого дуже суттєво за наявності лімфоїдної гіперплазії та бактеріальної колонізації тонкого кишечника. Після лікування лямбліозу архітектура мікроворсинок відновлюється, мальабсорбція та лімфоїдна гіперплазія набувають оборотного розвитку.
Лямбліоз, як і багато інших паразитарних хвороб, може мати субклінічний перебіг, що ускладнює діагностику й лікування. Численні публікації, що з’явилися протягом останніх 5–10 років, присвячені переважно дитячому лямбліозу [3]. За даними ВООЗ, ураження лямбліями дитячого населення планети вище від дорослого в 5–6 разів, зареєстровані випадки захворювання навіть у новонароджених [4, 20].
Лямблії мають особливу значущість у формуванні в дітей алергічних дерматитів [11, 27]. При тривалій персистенції лямблій в організмі дитини формуються стійкі зміни шкіри з інфільтрацією, пігментацією, фолікулярним кератозом. Лямблії виявляються у 69 % дітей з алергічними дерматитами. Багатьма авторами визнається можливість розвитку на тлі інфікування лямбліями бронхіальної астми [25]. Деякі дослідники реєструють при лямбліозі еозинофільні інфільтрати в легенях, деякі пацієнти відзначають біль у суглобах, у більшості хворих зазначені ознаки зникали після проведення протипаразитарної терапії.
Причина дуже широкого діапазону хвороби до цього часу не з’ясована та залежить від особливостей хазяїна й патогенності різних ізолятів і штамів Lamblia intestinalis різної вірулентності, що відрізняються стійкістю до трипсину та хемотрипсину.
Поширена в літературі минулих років думка про можливість співіснування лямблій і людини за типом симбіозу (лямбліоносійство), що припускає адаптацію організму людини до паразита, в сучасних умовах неактуальна. Сьогодні загальноприйнятою вважається думка про необхідність ерадикації лямбліозної інфекції незалежно від наявності клінічних проявів захворювання [6, 25].
За даними вітчизняних і зарубіжних дослідників, у клініці лямбліозу можна виділити 4 основних синдроми: больовий, диспептичний, астеноневротичний та алергодерматичний [23]. Лямбліоз може мати субклінічний або безсимптомний перебіг. За клінічним перебігом виділяють гостру й затяжну рецидивуючу (хронічну) форми.
Клінічна картина лямбліозу може характеризуватися клінічними ознаками ураження шкіри, травної, серцево-судинної та нервової систем. Це вимагає від клініцистів дуже критичного підходу до оцінки симптомів у хворих на лямбліоз [1, 3, 11, 17].
Оскільки лямбліоз не супроводжується розвитком патогномонічних ознак, лікар на підставі клінічних даних може встановити лише попередній діагноз.
Хоча лямбліоз відомий уже протягом тривалого часу, існують серйозні проблеми в його діагностиці. Останніми роками активно проводяться дослідження з розробки більш ефективних методів діагностики лямбліозу. З цією метою використовують виявлення специфічних антигенів у фекаліях і специфічних антитіл у сироватці крові [7, 8, 17]. Чутливість і специфічність таких методів варіює залежно від складу і якості використаних для їх конструювання антигенів лямблій або антитіл до них. Існує проблема перехресних реакцій антигенів лямблій з іншими паразитарними і соматичними антигенами, що дають хибнопозитивні результати.
Виявлення хворих або підозрілих на лямбліоз проводять медичні працівники всіх органів охорони здоров’я (лікувально-профілактичні заклади, приватні клініки, науково-дослідні інститути тощо), а також особи, які займаються приватною медичною практикою, під час профілактичних, планових, попередніх при прийомі на роботу і періодичних обстеженнях при проведенні медичного нагляду за особами, які контактували з хворим чи носієм лямбліозної інфекції, а також за епідеміологічними показаннями [13, 14, 17]. Показаннями до обстеження на лямбліоз є: діарея невстановленої етіології; хронічні захворювання шлунково-кишкового тракту; дисбіоз кишечника; гіпотрофія, відставання у фізичному розвитку; дерматити, екземи, нейродерматити; імунодефіцитні стани; обструктивні бронхіти, бронхіальна астма; алергії нез’ясованої етіології.
Лабораторну діагностику лямбліозу проводять у клініко-діагностичних лабораторіях лікувально-профілактичних закладів, паразитологічних підрозділах інших лабораторій, що атестовані і мають відповідний дозвіл для роботи зі збудниками III–IV групи патогенності у встановленому порядку.
У сучасних лабораторіях розпізнавання найпростіших, у тому числі лямблій, проводять, використовуючи нативний мазок, оброблений розчином Люголя, і метод ефір-формалинового збагачення. Перевагами першого методу є простота виконання та можливість виявлення в цистах важливих морфологічних деталей. При дослідженні фекалій методом нативного мазка, забарвленого розчином Люголя, вегетативні стадії лямблій практично не виявляються, що ускладнює диференціацію їх від інших найпростіших (бластоцисти, гриби роду Candida, Ent.сoli) [5, 8].
При застосуванні методу збагачення, що заснований на концентрації цист найпростіших у пробах калу й усуненні фекальних частинок, аналізу можуть піддаватися як свіжі фекалії, так і матеріал із консервантів. Перевагою методу є його доступність і досить висока інформативність. Він дозволяє виявляти інвазії з високою, середньою і низькою інтенсивністю, а також є ефективним при дослідженні фекалій із консервантів [8].
У консервуючій рідини Турдієва цисти найпростіших зберігають свою морфологічну структуру протягом 6 місяців. Це дозволяє досліджувати матеріал через тривалий час після отримання його від хворого і також дає можливість накопичувати фекалії протягом декількох днів.
Недоліком є те, що при потраплянні в консервант трофозоїти гинуть. Крім того, дослідження є більш трудомістким і дорогим, ніж метод нативного мазка, забарвленого розчином Люголя. Досить висока ефективність дозволяє використовувати його в практичній охороні здоров’я, хоча за рядом обставин метод поки недостатньо поширений. Залишається дискусійним і питання про кратність проведення копропротозооскопічного дослідження для верифікації лямбліозу. Одні автори вважають цілком достатнім трикратне дослідження калу, інші — до семи разів.
Дослідження дуоденального аспірату дозволяє виявляти вегетативні та цистні форми найпростіших. Як правило, використовуються дві методики: дослідження нативного мазка жовчі і жовчі з центрифугуванням.
Вегетативні форми лямблій виявляють у секреті кишки (порціях А і В), отриманому під час зондування. При цьому мікроскопія дуоденального вмісту проводиться негайно для кожної порції. Деякі фахівці вважають за краще досліджувати не кал, а дуоденальний уміст, бо в ньому лямблії знаходяться постійно, а з фекаліями виділяються з великими перервами (від декількох днів до двох тижнів).
Однак мікроскопічне дослідження дуоденального вмісту не дає особливих переваг порівняно з дослідженням фекалій і навіть поступається копропротозооскопічному в ефективності. Багато авторів указують на те, що це дослідження малоінформативне, особливо в тих випадках, коли лямблії паразитують у середніх і дистальних відділах тонкої кишки, недоступних для зондування.
Також важливо, що трофозоїти лямблій часто розміщуються не на апікальній частині ворсинок, а біля їх основи, в епітеліальних трубочках кишкових ворсинок. У зв’язку з цим доцільно проводити дослідження секрету дванадцятипалої кишки без домішок жовчі, шлункового і панкреатичного соку, що вимагає застосування вакуумного триканального зонда.
До недоліків дослідження дуоденального аспірату слід зарахувати і те, що отриману таким чином жовч необхідно негайно досліджувати мікроскопічно, оскільки вже через 30 хвилин її склад значно зміниться. Крім того, не можна забувати про інвазивність методу, що дуже важливо, коли йдеться про дітей раннього віку.
У сучасних умовах найбільш вірогідним методом виявлення лямблій є дуоденальна біопсія, при якій вивчаються мазки-відбитки розчавлених біоптатів. Основним недоліком методу є інвазивність, а також неможливість його використання у дітей.
Останніми роками широко застосовуються в діагностиці лямбліозу імунологічні методи, засновані на виявленні сироваткових антитіл.
Серологічні методи діагностики є опосередкованими, тому можуть використовуватися як додаткові. Вони ґрунтуються на виявленні в крові антитіл, специфічних до антигенів лямблій. Рівень таких антитіл залежить від особливостей імунної системи хазяїна, інтенсивності інвазії, форми перебігу захворювання та ряду інший факторів.
Антитіла до антигенів лямблій з’являються на 10–14-й день після початку інвазії і присутні у крові і секретах людини практично на всіх її стадіях. Через 1–2 місяці після повної елімінації паразита концентрація специфічних IgG у крові людини різко знижується. Серологічні дослідження при лямбліозі використовують і для епідемологічних завдань, бо специфічні антитіла виявляються при маніфестній і безсимптомній формі інфекції. Ці ж обставини заважають інтерпретації серологічної реакції в кожному конкретному випадку.
Значно вищий діагностичний потенціал мають методи виявлення лямблій у фекаліях і біотопах при використанні антитіл до цілісних трофозоїтів або моноспецифічних антитіл до антигенів лямблій із молекулярною масою 65 кД (GSA–65). Контроль ефективності лікування лямбліозу проводять через 3–4 тижні після закінчення лікування. Критерій ефективності: три негативних результати копропротозооскопічного дослідження з інтервалом 1–2 дні.
Останніми роками активно ведуться дослідження з розробки більш ефективних методів діагностики лямбліозу. Розробка науково обґрунтованих методів боротьби з лямбліозом та їх успішна реалізація неможливі без наявності простих і надійних методів його виявлення.
Проблема лікування та профілактики лямбліозу залишається актуальною, оскільки лямблії дуже поширені в зовнішньому середовищі й людській популяції.
Терапія лямбліозу має на меті досягнення перш за все клінічного ефекту: зменшення проявів інтоксикаційного й алергічного синдромів, посилення власного імунного захисту організму.
Важливе значення має дієта, зменшення вживання простих вуглеводів. На фоні запального процесу в кишечнику, особливо у дітей, розвивається синдром вторинної недостатності та целіакії від стертих до виражених форм. Результатом цього може бути утворення значної кількості проміжних сахарів у кишечнику хворого, які створюють поживне середовище для найпростіших та умовно-патогенної флори, що бурхливо проліферує й підсилює запальний процес. Розірвати це порочне коло неможливо без призначення безлактозної та аглютенової дієти як мінімум на 3–4 місяці. При цьому з раціону дитини виключається молоко, або його заміняють соєвими, низьколактозними сумішами, гідролізатами коров’ячого молока. Різко скорочують або виключають продукти з умістом глютену (хлібобулочні та макаронні вироби, всі крупи, окрім рису, гречки та кукурудзи). Замість хліба можливе вживання випічки на основі рису, гречки, кукурудзи або хліба на основі висівок. Замість продуктів із борошна, звичних для дітей, до яких належать печиво, здоба, можна використовувати в їжу кукурудзяні пластівці (попкорн), рисові кульки, рисове або кукурудзяне печиво. Рекомендується кисле питво (журавлиний морс, знежирений кефір, компот із сухофруктів). Можна вживати нежирне відварене м’ясо, овочеві гарніри, а також салати, вінегрет із вареної моркви й буряка, заправлені соняшниковою олією.
Для етіотропної терапії призначають препарати, ефективні щодо патогенних і умовно-патогенних найпростіших [9].
Перші роботи, що стосуються етіотропного лікування лямбліозу, описують застосування акрихіну як протилямбліозного засобу (1936 рік). У 50–60-ті роки минулого століття почали застосовувати похідні хіноліну (амінохінол). Амінохінол є ефективним для лікування хворих на лямбліоз, лейшманіоз шкіри, токсоплазмоз, системні захворювання сполучної тканини. У сучасних умовах ці препарати мають обмежене застосування через недостатню ефективність і серйозні побічні явища: головний біль, шум у вухах, алергічні реакції, кволість [16, 21, 29].
Проте в сучасних умовах при проведенні протипаразитарного лікування слід враховувати, що ефективність протипаразитарних лікарських засобів (як і антибіотикотерапії) з часом знижується. Це обумовлено такими факторами: різким зниженням імунного захисту; відсутністю достатнього набору простицидних препаратів із вираженою протилямбліозною дією і без побічних шкідливих ефектів; високим рівнем реінфікування (повторного зараження), особливо в дитячих колективах і сім’ї; появою стійких форм паразитів, зниженням їх чутливості до препаратів, що використовувались багато років (трихопол, фуразолідон) [22].
Ефективність фуразолідону досягає 80 %, проте він має відносно високу частоту побічних явищ: приблизно 10 % пацієнтів повідомляють про шлунково-кишкові симптоми у вигляді нудоти, блювоти, шкірної сверблячки, а в окремих випадках — гемолітичної або мегалобластної анемії й агранулоцитозу, що змушує з обережністю підходити до його застосування і регулярно контролювати стан крові. Призначають фуразолідон по 10 мг/кг маси тіла на добу, розділивши цю дозу на 4 прийоми, протягом 5–10 днів.
Останніми роками у хворих на лямбліоз найчастіше використовують три препарати, що є похідними нітроімідазолу — метронідазол, тинідазол і орнідазол [19, 24]. Зазначені лікарські засоби близькі один до одного за структурою і механізмом дії. Проте в ряді випадків у пацієнтів спостерігаються побічні явища: диспептичний і астеноневротичний синдроми, алергічні прояви.
Метронідазол тривалий час був основним препаратом для лікування лямбліозу, призначався з розрахунку 5 мг/кг маси тіла 3 рази на день протягом 7–10 днів. Зазвичай при використанні метронідазолу для підвищення ефективності лікування його призначають двома курсами з інтервалом у 5–7 днів. Ефективність метронідазолу, однак, не перевищує 70 % при частоті побічних ефектів у 15–30 % випадків, основними з яких є нудота, блювота, біль у животі, металевий присмак у роті, рідше — головний біль, запаморочення, а в окремих пацієнтів — периферичні нейропатії і навіть судомний синдром. При розгляді випадків стійкості лямблій до метронідазолу в багатьох дослідженнях було показано, що це обумовлено його токсичним, мутагенним ефектом, пов’язаним з утворенням вільних радикалів.
Ефективність орнідазолу в дозі 40 мг/кг на добу при масі тіла менше 35 кг та 1500 мг на добу — при масі тіла понад 35 кг, за даними Л.В. Бабуріна (2005), становить 91,2 %. Орнідазол показав високу ефективність при лікуванні лямбліозу у хворих на хронічні дерматози — майже у 85 % хворих була досягнута санація від збудника.
У процесі пошуку нових препаратів антипротозойної дії був застосований альбендазол [26], що, за даними В.P. Meloni і співавт. (1990), показав більш виражений ефект щодо лямблій порівняно з метронідазолом і тинідазолом. При лямбліозі препарат призначають дітям віком понад 2 роки з розрахунку 10–15 мг/кг маси тіла на добу протягом 5–7 днів. Ефективність альбендазолу, за даними Е.А. Кочергіна, становить 86 %.
За допомогою фармакоекономічного аналізу різних схем етіотропного лікування лямбліозу нами було встановлено, що найбільш економічним у поліклінічних умовах є використання Макмірору (ніфурателю).
Серед відносно нових протипаразитарних препаратів для етіотропного лікування лямбліозу ніфуратель (Макмірор, Італія) має на сьогодні найбільшу активність при найменшому числі побічних ефектів [30]. При призначенні Макмірору дорослим по 2 таблетки 2–3 рази на добу після їжі протягом 7–10 діб, дітям віком 6 років і старше — по 15 мг/кг маси тіла на прийом 2 рази на добу після їжі протягом 7–10 діб ефективність лікування становить 96,8 %.
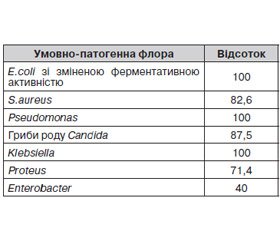
Макмірор (ніфуратель) має широкий спектр антипротозойної й антимікробної дії. Препарат ефективний щодо таких мікроорганізмів, як бактерії (Enterococcus faecalis, Enterococcus faecium, Staphylococcus aureus, Bacillus subtilis, Escherichia coli, Shigella flexneri, Shigella sonnei, Salmonella typhi, Salmonella typhimurium, Salmonella enteritidis, Klebsiella spp., Enterobacter spp., Serratia spp., Citrobacter spp., Morganella spp., Rettgerella spp., Pragia fontium, Budvicia aquatica, Rachnella aquatilis, Acinetobacter spp.), інші атипові ентеробактерії; Helicobacter pylori, у тому числі штами, стійкі до метронідазолу; гриби роду Candida; найпростіші (амеби, лямблії, трихомонади — trichomonas vaginalis). Має антихламідійну активність і активність щодо Ureaplasma urealiticum. Під час численних досліджень була продемонстрована висока активність ніфурателю і щодо Gardnerella vaginalis. Крім того, ніфуратель переважно впливає на анаеробні мікроорганізми (Bacteroides fragilis і Clostridium perfrigens).
У хімічній формулі ніфуратель має тіоефірну групу, завдяки якій істотно розширюється спектр протимікробної і протипротозойної дії препарату і не формується стійкість до нього. Побічні явища (шкірний свербіж і висипання) при застосуванні Макмірору вкрай рідкісні, препарат добре переноситься дорослими та дітьми (за нашими даними, з 6-річного віку).
На відміну від метронідазолу і фуразолідону, в елімінації яких бере участь печінка, Макмірор практично повністю елімінується нирками і не задіює дезінтоксикаційні резерви печінки. Період напіввиведення препарату чималий, що дозволяє застосовувати Макмірор 2 рази на день.
/31/31_2.jpg)
При затяжному рецидивуючому (хронічному) лямбліозі необхідно оцінювати вираженість та тривалість клінічних симптомів лямбліозу і наявність фонових та супутніх захворювань [15, 18]. Терапія кожного хворого повинна базуватися на індивідуальних особливостях організму. Починати лікування лямбліозу доцільно разом із додатковою патогенетичною терапією.
Після закінчення курсу лікування необхідне проведення контрольного паразитологічного обстеження для визначення ефективності лікування. Для того, щоб об’єктивно визначити ефект лікування і виключити реінвазію, паразитологічне обстеження потрібно проводити не пізніше ніж через 3 тижні після закінчення лікування.
З метою оптимізації лікувально-діагностичних заходів при лямбліозі на кафедрі медичної паразитології і тропічних хвороб Харківської медичної академії післядипломної освіти був проведений фармакоекономічний аналіз схем етіотропної терапії пацієнтів з інвазією Lamblia intestinalis.
Фармакоекономічну ефективність схем терапії лямбліозу порівнювали за допомогою таких методів, як: 1) аналіз «витрати — ефективність» (ВЕ) і відношення коефіцієнта збільшення вартості до збільшення ефективності (Кве); 2) аналіз «мінімізації витрат» (МВ) [2].
Клініко-економічний аналіз був проведений для оцінки економічності схем терапії окремо для амбулаторно-поліклінічних та стаціонарних умов, розрахунки проводилися також з урахуванням вікових дозувань [12].
Терапія буде найбільш ефективною з найменшою величиною показника «витрати — ефективність». Якщо значення ВЕ збігаються для двох або більше методів лікування, то для вибору найбільш оптимального необхідне проведення додаткового аналізу значень вартості та ефективності. В основу вибору може бути покладений пошук методів лікування з найменшою вартістю або найбільшою ефективністю. У тих випадках, коли для тієї або іншої нозологічної одиниці визначено її мінімальний допустимий рівень ефективності (з огляду на клінічну доцільність) та/або її максимальну допустиму вартість (виходячи з доступних фінансових ресурсів), то для обчислення ВЕ слід відкинути з розгляду ті види терапії, що не задовольняють хоча б одній із цих двох умов.
У структурі ВЕ використовується також коефіцієнт відношення приросту витрат до приросту ефективності, що є вартістю одиниці додаткової ефективності. Для порівняння більше ніж двох методів вибирається референтна схема лікування, що має найменшу ефективність. Коефіцієнти для всіх інших схем терапії розраховуються відносно референтного. Оптимальним є втручання з найменшим Кве, тобто з найменшою вартістю одиниці додаткової ефективності. Якщо в кількох втручань Кве однакові, то для негативних коефіцієнтів вибирається втручання з найбільшою ефективністю, а для позитивних необхідно проаналізувати готовність платити додаткову вартість за прирощення ефективності. Рівність Кве вказує на рівноцінну ефективність порівнюваних втручань.
При проведенні фармакоекономічного аналізу схем етіотропної терапії хворих на лямбліоз за критерій ефективності була взята протипаразитарна активність, а за референтну схему — терапія із застосуванням альбендазолу, що мала найменший показник ефективності (0,90).
При амбулаторному лікуванні хворих на лямбліоз найбільш ефективною і найменш витратною виявилась терапія з використанням як етіотропного препарату Макмірору (ніфурателю), оскільки значення ВЕ і Кве були мінімальними і у дітей, і в дорослих.
Витрати на медикаменти визначали на основі середньої вартості етіотропного препарату.
Отримані результати ВЕ при порівнянні схем етіотропного лікування хворих на лямбліоз в амбулаторно-поліклінічних умовах, як у дітей, так і в дорослих визначили найбільш економічний варіант — терапію з використанням Макмірору.
Результати проведеного аналізу мінімізації витрат при лікуванні в амбулаторно-поліклінічних умовах відповідають даним, отриманим при розрахунку показника «витрати — ефективність», і визначають як найбільш економічну схему лікування Макмірором, оскільки саме в цій групі показник ВЕ як у дітей, так і в дорослих є мінімальним.
Результати проведеного клініко-економічного аналізу показали, що при амбулаторному лікуванні хворих на лямбліоз найбільш ефективною і найменш витратною є схема лікування з використанням Макмірору, оскільки значення ВЕ, Кве і МВ виявилися мінімальними і у дітей, і у дорослих.
Таким чином, проблема діагностики та лікування лямбліозу вимагає найпильнішої уваги лікарів, хоча залишаються суперечливі й невирішені проблеми діагностики лямбліозу у дітей. Складність клінічної діагностики лямбліозу полягає в тому, що це захворювання не має патогномонічних клінічних ознак і часто є пусковим механізмом або нашаровується на інші хронічні захворювання шлунково-кишкового тракту. Лабораторне виявлення вегетативних і інцистованих форм лямблій обмежено періодичністю їх виведення з калом і змінами морфології паразитів при дослідженні через кілька годин.
При своєчасній, якісній діагностиці та лікуванні хворих на лямбліоз з урахуванням індивідуального вибору, правильного дозування препарату, підбору та дотримання методики лікування можна досягти високої клінічної та епідеміологічної ефективності, що є вагомим важелем у загальному комплексі оздоровлення населення від протозоозів.
Таким чином, лямбліоз є поширеним паразитарним захворюванням із серйозними клінічними проявами. Лямбліоз слід мати на увазі під час диференціальної діагностики багатьох захворювань, у тому числі при синдромі мальабсорбції, алергічних станах і болі в животі неясного походження. Лікування лямбліозу становить певні складнощі у зв’язку зі стійкістю лямблій, що обумовлює необхідність проведення комплексної терапії з застосуванням найбільш ефективного і найменш витратного лікування з використанням як етіотропного препарату Макмірору (ніфурателю).
1. Абулазизов А.И. Паразитозы у амбулаторных и стационарных больных детей / А.И. Абулазизов, С.Б. Абдудпатахова // Мед. паразитол. — 2007. — № 1. — С. 14–16.
2. Авксентьева М.В. Экономическая оценка эффективности лекарственной терапии (фармакоэкономический анализ) / М.В. Авксентьева, П.А. Воробьев, В.Б. Герасимов и др. — М.: Ньюдиамед, 2000. — 80 с.
3. Бандурина Т.Ю. Проблемы диагностики и лечения лямблиоза у детей / Т.Ю. Бандурина, Г.Ю. Кнорринг // Terra Medika. — 2003. — № 4. — С. 23–27.
4. Бельмер С.В. Лямблиоз у детей / С.В. Бельмер // Рос. мед. журн. — 2004. — Т. 12, № 3 [Электронный ресурс]. — Режим доступа: http://www.rmt.ru/main.htm
5. Гасанова Т.А. О некоторых особенностях лабораторной диагностики протозоозов в современных условиях / Т.А. Гасанова, С.В. Ларионов, К.А. Хачатуров и др. // Мед. паразитол. — 2007. — № 1. — С. 11–13.
6. Гасанова Т.А. Значение трихомониаза и лямблиоза в развитии воспалительных заболеваний органов малого таза / Т.А. Гасанова, Т.Н. Ткаченко, В.А. Кротова и др. // Мед. паразитол. — 2005. — № 4. — С. 22–26.
7. Дедкова Л.М. Выявление антител к антигенам трофозоитов лямблий иммуноферментным методом / Л.М. Дедкова // Мед. паразитол. — 1999. — № 3. — С. 46–49; Денисов М.Ю. Лечение атопического дерматита / М.Ю. Денисов // Современные технологии реабилитации детей с аллергодерматозами / Под ред. Л.Ф. Казначеевой. — Новосибирск, 1999. — С. 58–60.
8. Ермакова Л.А. Оценка эффективности многократного копрологического исследования для диагностики лямблиоза / Л.А. Ермакова, Н.Ю. Пшеничная, Ю.М. Амбалов, Е.А. Черникова // Мед. паразитол. — 2007. — № 4. — С. 32–33.
9. Епідеміологія, лікування та профілактика лямбліозу: Методичні рекомендації / К.І. Бодня, О.І. Повгородня, Н.С Чегодайкіна; Міністерство охорони здоров’я України, Український Центр наукової медичної інформації та патентно-ліцензійної роботи. — Київ: Б.в., 2006. — 30 с.
10. Інфекційні хвороби в загальній практиці та сімейній медицині / За ред. М.А. Андрейчина. — Тернопіль: ТДМУ, 2007. — 500 с.
11. Залипаева Т.Л. Клинические проявления лямблиозной инфекции у детей / Т.Л. Залипаева // Мед. паразитол. — 2002. — № 3. — С. 29–32.
12. Клинико-экономический анализ / П.А. Воробьев, М.В. Авксентьева, А.С. Юрьев, М.В. Сура. — М.: Ньюдиамед, 2004. — 403 с.
13. Козлов С.С. Лабораторная диагностика паразитарных болезней: методические рекомендации / С.С. Козлов. — СПб., 2006. — 44 с.
14. Корниенко Е.А. Клиника, диагностика и лечение лямблиоза у детей / Е.А. Корниенко, С.Н. Минина // Педиатрическая фармакология. — 2009. — Т. 6, № 4. — С. 2–7.
15. Кучеря Т.В. Лечение лямблиоза у детей в современных условиях: эффективность и выбор специфического препарата / Т.В. Кучеря, Т.А. Макарова, Е.А. Кочергина, Т.И. Авдюхина // Медицинская паразитология и паразитарные болезни. — 2002. — № 3. — С. 33–35.
16. Методи синтезу 2-ариламіно-4-метилхінолін-6-феніл-сульфамідів та їх антимікробна активність / Т.О. Олексієнко, І.С. Гриценко, Т.П. Осолодченко // Фармацевтичний часопис. — 2012. — № 4. — С. 17–20.
17. Осипова С.О. О необходимости расширения протозоологических и серологических исследований на кишечные простейшие / О.С Осипова, Т.В. Продеус, Х.М. Мустафаев и др. // Мед. паразитол. — 1991. — № 6. — С. 13–15.
18. Пайков В.Л. Лямблиоз у детей и подростков Санкт-Петербурга и опыт противолямблиозной терапии тибералом / В.Л. Пайков, П.В. Гончар, Т.Н. Микуева, М.И. Батырев // Клиническая фармакология и терапия. — 1998. — № 1. — С. 51–52.
19. Пекарева Н.А. Частота и особенности побочных эффектов тиберала в лечении лямблиоза у детей / Н.А. Пекарева, П.В. Лесневская, А.В. Александрова // Клиническая фармакология и терапия. — 1997. — № 3. — С. 58.
20. Погорельчук Т.Я. Кишечные паразитоценозы у детей закрытых детских учреждений и меры профилактики / Т.Я. Погорельчук, В.А. Олейник, И. Орлова, И.М. Локтева // Мед. паразитол. — 2003. — № 4. — С. 36–37.
21. Синтез біологічно активних речовин з антимікробною активністю в ряду 4-метил-2-хлорхінолін-6-алкілсульфамідів / І.С. Гриценко, Т.О. Олексієнко, В.О. Зубков, Т.О. Цапко // Вісник фармації. — 2011. — № 2(66). — С. 24–28.
22. Сучасні методи лікування основних паразитарних хвороб людини: Методичні рекомендації / Р.Г. Лукшина, К.І. Бодня, І.К. Москаленко, Л.В. Холтобіна, В.А. Коробова, В.Б. Мироненко, К.І. Колесник, Т.М. Павліковська, С.М. Ніколаєнко, М.А. Квітко, Р.Г. Павленко; Міністерство охорони здоров’я України, Український Центр наукової медичної інформації та патентно-ліцензійної роботи. — Київ: б.в., 2004. — 39 с.
23. Тумольская Н.И. Роль лямблий в патологии человека / Н.И. Тумольская // Врач. — 2000. — № 8. — С. 23–25.
24. Campell H. The effects of the antiprotozoal drugs metronidazole and furazolidone on trofozoites of Giardia lamblia / H. Campell, Smi Campanati Lorain, Monteiro–Leal Luis Henrique // Parasitol. Res. — 2002. — Vol. 88, № 1. — C. 80–85.
25. Di Prisco M. Association between giardiasis and allergy / M. Di Prisco, J. Hagel, R. Lynch et al. // Arm. Allergy Asthma Immunoe. — 1998. — Vol. 81, № 3. — P. 261–265.
26. Dutta A.K. A randomised multicentre study to compare the safety and efficacy of albendazole and metronidazole in the treatment of giardiasis in children / A.K. Dutta, M.A. Phadke, A.C. Bagade et al. // Indian J. Pediatr. — 1994. — Vol. 61. — P. 689–693.
27. Granot E. Immunologic response to infection with Giardia Lamblia in children, effect of different clinical settings / E. Granot, D. Spira, D. Fraser, R. Deckeibaum // J. Trop. Pediatr. — 1998. — Vol. 44, № 4. — P. 241.
28. Soltys B.J. Giardia lamblia: cell biology and microscopy of one of the most primitive eukaryotes / B.J. Soltys, R.S. Gupta // Journal of Eukaryotic Microbiology. — 2001. — Vol. 41. — P. 625–632.
29. Synthesis and Invitro Antimicrobial Screening of some new Substituted benzilidine-3-(4,5-diphenyl-1H-imidazol-2-yl)-6-methyl-quinoline / M. Shaikh, S.N. Kinkar1, S.R. Chavan // Archives of Applied Science Research. — 2011. — Vol. 3, № 1. — P. 401–406.
30. Zaot Jo. A systematic review on the treatment of giardiasis / Zaot Jo, T.G. Mank, W.J. Assendelft // Trop. Med. Int. Health. — 1997. — Vol. 2, № 1. — P. 63–82.

/31/31.jpg)