Международный неврологический журнал 5 (75) 2015
Вернуться к номеру
Мексиприм в лечении больных с дисциркуляторной энцефалопатией, обусловленной атеросклерозом и артериальной гипертензией
Авторы: Мищенко Т.С., Дмитриева Е.В. - ГУ «Институт неврологии, психиатрии и наркологии Национальной академии медицинских наук Украины», г. Харьков
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
В статье рассматриваются вопросы лечения хронических нарушений мозгового кровообращения, развившихся вследствие атеросклероза и/или артериальной гипертензии. Подчеркнуто, что при назначении лекарственных препаратов таким пациентам необходим патогенетически обусловленный подход, что возможно при применении средств, обладающих вазоактивными, психостимулирующими и ноотропными свойствами. Приведены данные исследования эффективности и безопасности применения препарата Мексиприм. Показано, что терапия препаратом Мексиприм в течение 4 недель способствовала регрессированию субъективных и объективных симптомов дисциркуляторной энцефалопатии, развившейся на фоне атеросклероза и/или артериальной гипертензии. Препарат оказывал положительное влияние на психоэмоциональное состояние больных по шкалам депрессии и астенизации. В комплексном лечении Мексиприм приводил к достоверному улучшению двигательных и когнитивных функций.
У статті розглядаються питання лікування хронічних порушень мозкового кровообігу, що розвинулися внаслідок атеросклерозу та/або артеріальної гіпертензії. Підкреслено, що при призначенні лікарських препаратів таким пацієнтам необхідний патогенетично обумовлений підхід, що можливо при застосуванні засобів, які мають вазоактивнi, психостимулюючi і ноотропні властивості. Наведено дані дослідження ефективності та безпеки застосування препарату Мексиприм. Показано, що терапія препаратом Мексиприм протягом 4 тижнів сприяла регресуванню суб’єктивних і об’єктивних симптомів дисциркуляторної енцефалопатії, що розвинулася на тлі атеросклерозу та/або артеріальної гіпертензії. Препарат мав позитивний вплив на психоемоційний стан хворих за шкалами депресії і астенізації. У комплексному лікуванні Мексиприм призводив до істотного покращення рухових і когнітивних функцій.
This article discusses the issues of treatment for chronic disorders of cerebral circulation, which developed due to atherosclerosis and/or hypertension. It was stressed that in the appointment of drugs for these patients, the pathogenetic approach is necessary, which is possible when using agents with vasoactive, psychostimulant and nootropic properties. The data of the study on the efficacy and safety of Mexiprim are provided. It is shown that therapy with Mexiprim for 4 weeks promoted regression of subjective and objective symptoms of dyscirculatory encephalopathy developed against the background of atherosclerosis and/or hypertension. The drug has a positive effect on the psychoemotional state of patients by scales of depression and asthenia. In the comprehensive treatment, Mexiprim contributed to significant improvement in motor and cognitive functions.
мозговое кровообращение, атеросклероз, артериальная гипертензия, Мексиприм.
мозковий кровообіг, атеросклероз, артеріальна гіпертензія, Мексиприм.
cerebral circulation, atherosclerosis, hypertension, Mexiprim.
Статья опубликована на с. 91-98
В структуре сердечно-сосудистых заболеваний, которые являются пандемией современной медицины, очень важное место занимает цереброваскулярная патология. Сосудистые заболевания головного мозга являются одной из ведущих причин смертности и инвалидизации населения земного шара. Так, смертность от сосудистых заболеваний головного мозга в экономически развитых странах мира занимает в структуре общей смертности 3-е место [1, 2].
Как отмечают эксперты Всемирной организации здравоохранения, в будущем количество цереброваскулярных заболеваний (ЦВЗ) возрастет, что связано с постарением населения планеты и увеличением распространенности в популяции как развитых, так и развивающихся стран таких факторов риска, как артериальная гипертензия (АГ), сахарный диабет (СД), гиперхолестеринемия, курение, ожирение, гиподинамия и др.
В структуре ЦВЗ мозговой инсульт, как наиболее тяжелая форма этой патологии, занимает лишь около 4 %. Львиная доля (96 %) в структуре ЦВЗ в Украине принадлежит хроническим нарушениям мозгового кровообращения — дисциркуляторным энцефалопатиям (ДЭ) [1, 3]. Именно за счет роста ДЭ наблюдается увеличение распространенности ЦВЗ. Следует отметить, что почти половина всех случаев ДЭ регистрируется у людей трудоспособного возраста. Развитие ДЭ обусловливают возрастающая распространенность и выявляемость среди населения АГ, СД, заболеваний сердца, ранний атеросклероз, курение, злоупотребление алкоголем, стрессовые ситуации. Также значительное влияние на рост ДЭ оказывает гипердиагностика этой патологии [4, 5].
Впервые термин ДЭ был предложен в 60-х годах прошлого столетия Е.В. Шмидтом и Г.А. Максудовым и вошел в классификацию сосудистых заболеваний головного и спинного мозга, принятую в 1984 г. Согласно существующим представлениям ДЭ характеризуется как результат медленно прогрессирующей недостаточности кровоснабжения, приводящей к развитию множественных мелкоочаговых некрозов мозговой ткани и обусловливающей нарастающее ухудшение функций головного мозга.
Следует отметить, что термина ДЭ нет в Международной классификации болезней 10-го пересмотра (МКБ-10).
В МКБ-10 для хронических форм ЦВЗ выделены «церебральный атеросклероз», «гипертензивная энцефалопатия», ряд редких сосудистых заболеваний, другие уточненные поражения сосудов мозга, включая «хроническую ишемию мозга», и «неуточненная цереброваскулярная болезнь».
За рубежом хронические формы ЦВЗ сводят в основном к сосудистой деменции («мультиинфарктная деменция» по V. Hachinski), тогда как в нашей стране наиболее близкой к традиционному термину «ДЭ» является «хроническая ишемия мозга», включающая ряд клинических синдромов, являющихся причиной нетрудоспособности и социальной дезадаптации. Наряду с сосудистой энцефалопатией, этот термин применим и к состояниям, обусловленным повторными инсультами с развитием стойких неврологических нарушений.
Клиническая картина ДЭ имеет прогрессирующее развитие, и на основании выраженности симптоматики ее разделяют на три стадии.
Характерной особенностью ДЭ является сочетание неврологических симптомов и синдромов, эмоциональных расстройств и когнитивных нарушений [6].
Для установления диагноза ДЭ необходимо наличие таких критериев: 1) клинические признаки поражения головного мозга: неврологические, когнитивные, эмоционально-аффективные, подтвержденные психодиагностическими, психопатологическими методами; 2) сердечно-сосудистое заболевание (атеросклероз, АГ и др.), выявляемое по анамнезу и с помощью инструментальных методов; 3) причинно-следственная связь между 1-м и 2-м критерием; 4) структурные изменения головного мозга по данным нейровизуализации (компьютерная томография (КТ), магнитно-резонансная томография (МРТ) головного мозга); 5) клинические и параклинические признаки прогрессирования цереброваскулярной недостаточности.
Необходимые методы обследования для установления диагноза ДЭ: 1) клинико-неврологическое с обязательной аускультацией каротидных артерий; 2) психодиагностические обследования (краткая шкала оценки психического статуса, или Mini-Mental State Examination — MMSE, тест «запоминания 10 слов», таблицы Шульте и др.); 3) КТ или МРТ головного мозга; 4) ультразвуковая допплерография (УЗДГ) экстра- и интракраниальных сосудов головного мозга; 5) офтальмоскопия; 6) электрокардиография (ЭКГ); 7) мониторирование артериального давления (АД) и ЭКГ (по показаниям); 8) биохимическое исследование крови; 9) электроэнцефалография (по показаниям).
АГ и атеросклероз являются основными причинами ДЭ. Установлено, что в процессе развития и прогрессирования АГ и атеросклероза на всех структурно-функциональных уровнях сосудистой системы головного мозга формируется сложный и многообразный комплекс первичных деструктивных (острых, повторных), вторичных репаративных изменений и адаптивных процессов — ДЭ головного мозга. Из-за гипертонического стеноза или облитерации или атеросклеротического поражения мелких внутримозговых артерий происходит нарушение кровотока в бассейне этих сосудов и развитие наиболее типичных малых глубинных (лакунарных) инфарктов головного мозга (симптомных и асимптомных). При неблагоприятном течении АГ повторные острые эпизоды нарушения мозгового кровообращения приводят к лакунарному состоянию мозга. Помимо повторных острых нарушений, которые часто возникают в зонах терминального кровообращения, развиваются явления хронической ишемии. Маркером последней является разрежение перивентрикулярного или субкортикального белого вещества — лейкоареоз, который патоморфологически представляет собой зону демиелинизации, глиоз и расширение периваскулярных пространств. В некоторых случаях неблагоприятного течения АГ возможно подострое развитие диффузного поражения белого вещества головного мозга с клиникой быстро прогрессирующей деменции и других проявлений разобщения, что обозначается в литературе термином «болезнь Бинсвангера».
Таким образом, в основе патоморфогенеза ДЭ лежит поражение перфорантных церебральных артерий, приводящее к патологии белого вещества мозга (демиелинизация, поражение клеток олигодендроглии, апоптоз, лейкоареоз, атрофия коры). Характерные для ДЭ изменения (фибриноидный некроз, облитерирующий гиалиноз и склероз сосудистых стенок, милиарные аневризмы, очаги периваскулярного энцефалолизиса, малые глубинные инфаркты и др.) развиваются как в белом веществе полушарий, так и в определенных подкорковых структурах и стволе головного мозга. Наряду с множественными мелкоочаговыми изменениями в белом веществе полушарий мозга, при ДЭ обнаруживаются его диффузные изменения (персистирующий отек, деструкция миелиновых волокон, спонгиоз и др.) [7–10].
Ведущим патоморфологическим моментом хронической ишемии головного мозга является гипоксия, приводящая к ограничению аэробного образования энергии вследствие нарушения энергосинтезирующей функции дыхательной цепи митохондрий. В результате происходит накопление активных форм кислорода, истощение запасов эндогенных антиоксидантов и активация перекисного окисления липидов (ПОЛ) клеточных мембран, что в конечном итоге приводит к гибели клеток мозга [11–14].
В условиях ишемии запускается каскад процессов: ишемия — снижение продукции энергетического метаболизма — увеличение продукции активных форм кислорода — повышение уровня продуктов ПОЛ — повреждение ДНК — апоптоз — нарушение функций центральной нервной системы [15, 16].
Своевременное и комплексное блокирование этого каскада с помощью препаратов с выраженным и доказанным антиоксидантным и антигипоксантным действием уменьшает нейрональные потери и составляет цель нейропротекции [17–22].
В начале 1980-х годов был синтезирован этилметилгидроксипиридина сукцинат (ЭМГПС), способный проникать через гематоэнцефалический барьер. Среди препаратов ЭМГПС на фармацевтическом рынке Украины на сегодняшний день заслуживает внимания препарат Мексиприм (представлен на рынке Украины фирмой «Стада Арцнаймиттель АГ», Германия), фармакологические эффекты которого можно разделить на основные и дополнительные.
Синергизм основных эффектов определяет тройной механизм действия препарата Мексиприм при гипоксических состояниях: 1) активация основных ферментов антиоксидантных систем: супероксиддисмутазы, глутатионпероксидазы, глутатионредуктазы, каталазы — обусловливает повышение активности физиологической антиоксидантной системы в целом; 2) непосредственное связывание молекулой препарата Мексиприм свободных радикалов обеспечивает мембраностабилизирующий эффект и улучшение функционирования мембраносвязанных ферментов (кальцийнезависимая фосфодиэстераза, аденилатциклаза, ацетилхолинэстераза), ионных каналов и рецепторных комплексов, в том числе ГАМК-бензодиазепинового, ацетилхолинового, усиливается их способность связываться с лигандами, повышается активность нейромедиаторов и активация синаптических процессов; 3) активация окислительных процессов в цикле Кребса (увеличение активности сукцинатдегидрогеназы и поступление сукцината), обусловливающих увеличение продукции аденозинтрифосфата и снижение уровня лактата.
Входящий в состав препарата Мексиприм сукцинат в условиях гипоксии, поступая во внутриклеточное пространство, способен окисляться дыхательной цепью. Активация сукцинатоксидазного пути окисления в условиях гипоксии приводит к повышению резистентности клеток мозга и дефициту кислорода.
Комбинация основных фармакологических эффектов обусловливает эффективность препарата Мексиприм в уменьшении эксайтотоксичности и, как результат, обеспечении нейропротекции.
К дополнительным фармакологическим эффектам можно отнести следующие: повышение содержания в головном мозге дофамина, улучшение транспорта нейромедиаторов и синаптической передачи, клинически данные эффекты определяют анксиолитическое действие препарата Мексиприм, повышение работоспособности и когнитивных функций, увеличение резистентности организма к действию различных экстремальных факторов (стресс, физические нагрузки, снижение сна, различные интоксикации, в том числе при алкоголизме и наркоманиях).
Терапия когнитивных нарушений и неврологических расстройств, обусловленных атеросклерозом и АГ, у больных с ДЭ требуют патогенетически обусловленного подхода, что возможно при применении препаратов, обладающих вазоактивными, психостимулирующими и ноотропными свойствами.
Учитывая вышесказанное, целью нашего исследования явилась оценка эффективности и безопасности применения препарата Мексиприм у пациентов с ДЭ, развившейся на фоне АГ и/или атеросклероза.
Объект и методы исследования
Нами проведено открытое несравнительное исследование эффективности, безопасности и переносимости препарата Мексиприм у пациентов с ДЭ II ст., развившейся на фоне АГ и/или атеросклероза. В исследование были включены 20 пациентов (из них 12 женщин и 8 мужчин) в возрасте от 48 до 73 лет, находившиеся на лечении в отделении сосудистой патологии головного мозга ГУ «Институт неврологии, психиатрии и наркологии НАМН Украины».
Показатели нейропсихологических тестов, клинико-неврологического обследования, дополнительных методов обследования, КТ и МРТ головного мозга и УЗДГ экстра- и интракраниальных сосудов отражали наличие у наблюдаемых пациентов ДЭ II ст.
В задачи исследование входило:
1) оценить переносимость препарата, выявить возможные побочные явления, в том числе проанализировать влияние терапии препаратом Мексиприм на общее состояние больных с ДЭ (артериальное давление, частоту сердечных сокращений) и основные показатели гомеостаза;
2) влияние препарата на основные субъективные проявления ДЭ;
3) динамику объективных неврологических симптомов ДЭ в результате лечения препаратом Мексиприм;
4) общую двигательную активность пациентов с ДЭ в ходе лечения препаратом Мексиприм;
5) влияние препарата Мексиприм на психоэмоциональное состояние пациентов по шкалам депрессии и астенизации;
6) изучить влияние препарата на когнитивные функции по результатам психометрических тестов.
Все пациенты получали исследуемый препарат Мексиприм в дозе 100 мг в/м 2 раза в сутки в течение 14 дней, затем — 100 мг/сутки в течение 14 дней.
Все пациенты также получали базовую терапию, которая была максимально унифицирована и включала прием диуретиков, гипотензивных, кардиальных, противодиабетических, антиагрегантных, гиполипидемических препаратов по показаниям. Препараты и дозы назначались индивидуально, с учетом показателей АД, липидограммы, наличия сопутствующих заболеваний.
Пациентам, включенным в исследование, не назначали: другие ноотропные препараты; нейротрофические и вазоактивные средства; другие препараты, влияющие на мозговой метаболизм и мозговое кровообращение; сосудорасширяющие средства; препараты, угнетающие центральную нервную систему; производные бензодиазепина; антидепрессанты.
Для решения поставленных целей и задач исследования в работе применяли следующие методы обследования:
1. Для оценки основных субъективных клинических проявлений заболевания использовали 5-балльную рейтинговую шкалу со стандартизированными критериями оценки выраженности каждого симптома: 0 — симптом отсутствует, 1 — легкие проявления, 2 — умеренная выраженность, 3 — выраженные проявления, 4 — грубые проявления.
2. Для оценки основных объективных клинических проявлений заболевания использовали 5-балльную рейтинговую шкалу со стандартизированными критериями оценки выраженности каждого симптома: 0 — симптом отсутствует, 1 — легкие проявления, 2 — умеренная выраженность, 3 — выраженные проявления, 4 — грубые проявления.
3. Оценка двигательной активности проводилась по шкале Тинетти (или Performance-Oriented Mobility Assessment, POMA) [23], которая позволяет определить статическое равновесие и походку больных при выполнении ими конкретных двигательных заданий. Степень двигательных нарушений оценивалась по двум субшкалам: общей устойчивости и походки. Для оценки двигательных функций пациента просят сесть и подняться со стула, пройти по прямой линии, встать на носки и поднять руки вверх (показать, как он достает предметы с верхней полки), присесть и поднять предмет с пола. Оценивается устойчивость в толчковых пробах, выполнение поворота. С учетом шкалы Тинетти устанавливается степень общей устойчивости пациентов и нарушение походки, варьирующие от 0 до 24 и 16 баллов соответственно. В совокупности сумма баллов позволяет судить об уровне общей двигательной активности пациента: от 0 до 20 — значительно выраженная степень нарушений; от 21 до 33 — умеренная; от 34 до 38 — легкая степень нарушений; 39–40 баллов — норма.
4. Для оценки влияния препарата на психоэмоциональное состояние больных использовали шкалу самооценки уровня депрессии Zung и субъективную шкалу оценки астении.
5. Для определения влияния препарата на когнитивные функции использовали MMSE, пробы Шульте, методику «заучивания 10 слов» (по А.Р. Лурия).
Статистическая обработка результатов исследования проводилась с помощью современных методов математического анализа с использованием пакета статистических программ Statistica 6 и Excel 2007 — рассчитывали средние показатели и ошибки средних. В качестве критерия достоверности отклонения показателей использовали параметрический критерий Стьюдента и непараметрический критерий U (Вилкоксона — Манна — Уитни).
Нежелательные явления оценивали при каждом визите, фиксировали все нежелательные явления, происходившие с пациентами после приема первой дозы исследуемого препарата и до окончания лечения.
Результаты и их обсуждение
Влияние препарата Мексиприм на основные субъективные и объективные клинические проявления ДЭ
Под влиянием терапии препаратом Мексиприм отмечалось существенное ослабление выраженности объективной и субъективной симптоматики ДЭ, как количественное, так и по динамике распределения больных внутри группы в зависимости от степени ослабления субъективных и объективных показателей заболевания.
Терапия препаратом Мексиприм способствовала существенному уменьшению количественной выраженности и выявляемости практически всего перечня характерной для ДЭ объективной и субъективной симптоматики. У большинства пациентов степень выраженности жалоб снизилась от 4 до 1–2 баллов, а у значительного числа больных отмечена полная редукция предъявляемых ими жалоб. Динамика субъективной симптоматики представлена в табл. 1.
Оценка динамики субъективных и объективных симптомов заболевания (по данным шкалы динамики: ухудшение, без динамики, незначительное улучшение, заметное улучшение, исчезновение симптомов) показала, что в той или иной степени положительное действие препарата Мексиприм отмечено у 18 (90 %) пациентов, отсутствие эффекта («без динамики») — у 2 (10 %). Ни у одного из включенных в исследование больных осложнений не было.
Влияние препарата Мексиприм на психоэмоциональное состояние больных по данным шкалы самооценки уровня депрессии Zung и cубъективной шкалы оценки астении
По данным шкалы самооценки уровня депрессии Zung (табл. 2), у 16 (80 %) пациентов сумма баллов к окончанию лечения возросла до 20–49, что соответствует градации «нормальное состояние», тогда как до начала лечения данные только 6 (30 %) пациентов соответствовали этому показателю. По завершении исследования таких явлений, как умеренная и тяжелая депрессия, не зарегистрировано. При этом до начала исследования умеренная депрессия была отмечена у 2 (10 %) больных.
Данные субъективной шкалы оценки астении в ходе терапии препаратом Мексиприм представлены в табл. 3.
До начала лечения пациенты предъявляли жалобы, характерные для астении. Больные жаловались на быструю утомляемость, снижение памяти на текущие события, внимания. Из других симптомов также отмечались повышенная раздражительность и физическая усталость, снижение настроения, диссомнические нарушения.
При оценке уровня астенических расстройств по шкале МFI-20 (табл. 3) у больных наблюдался повышенный уровень общей (15,6 ± 3,3 балла) и физической (14,9 ± 3,7 балла) астении, а также снижение активности (13,8 ± 2,7 балла). Показатели уровня мотивации и психической астении были в пределах нормы: 10,7 ± 1,1 балла и 11,1 ± 1,9 балла соответственно.
Результаты тестирования после лечения выглядят следующим образом. Показатели астении снизились до уровня нормы, составив в среднем по группе: для общей астении — 11,2 ± 1,9 балла; для физической астении — 10,7 ± 2,1 балла; показатель снижения активности также стал меньше — 10,5 ± 2,3 балла.
Влияние препарата Мексиприм на когнитивные функции по данным методики «заучивания 10 слов» (по А.Р. Лурия), шкалы ММSE, а также методики «поиск чисел по таблицам Шульте»
Представленные данные нейропсихологического тестирования по шкале ММSЕ (табл. 4) свидетельствуют, что до начала лечения у обследуемых пациентов имелись когнитивные нарушения, степень которых соответствовала критериям умеренных когнитивных расстройств, что по шкале ММSЕ составляло 24–25 баллов. В структуре нарушений познавательных функций доминировали умеренные расстройства вербальной памяти (4,2 ± 1,3 балла), счетных операций (3,2 ± 0,7 балла) и функций гнозиса (4,6 ± 1,2 балла).
Результат анализа динамики познавательных нарушений в ходе лечения свидетельствует об отчетливом и равновыраженном улучшении всех оцениваемых параметров. Так, на фоне приема препарата Мексиприм несколько улучшались показатели вербальной памяти (4,2 ± 1,3 до лечения и 4,8 ± 0,7 — после) и отмечены достоверные улучшения показателей счетных операций (3,2 ± 0,7 и 4,6 ± 0,4 соответственно), гностических функций (4,6 ± 1,2 и 6,1 ± 1,6), общего показателя когнитивной продуктивности (24,5 ± 0,6 и 27,1 ± 1,9).
К окончанию лечения произошли существенные и количественно равновыраженные позитивные изменения параметров когнитивной продуктивности у обследованных больных (табл. 5). В целом эти изменения состоят в значительном уменьшении количества пациентов с умеренными когнитивными расстройствами и столь же значительном увеличении числа пациентов, у которых либо полностью восстановилась когнитивная продуктивность, либо выраженность когнитивных расстройств снизилась до уровня «легкие когнитивные нарушения».
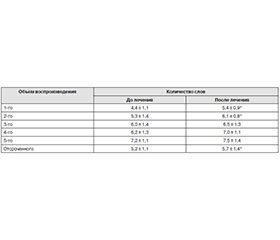
Показатели вербальной памяти по методике «запоминания 10 слов» у обследованных больных представлены в табл. 6.
Как видно, мнестические расстройства отмечали у всех пациентов. Объем непосредственного воспроизведения вербального материала у больных, принимавших препарат Мексиприм, составил 4,4 ± 1,1 слова.
Продуктивность произвольного запоминания вербального материала была снижена по сравнению с нормой. Фиксировался типичный платообразный тип кривой заучивания, характерный для больных с сосудистой патологией головного мозга. Объемы отсроченного воспроизведения были также достоверно уменьшены по сравнению с нормой у всех обследованных пациентов, что свидетельствует о наличии у них расстройств долговременной памяти.
В ходе терапии препаратом Мексиприм отмечены отчетливые позитивные изменения функций вербальной памяти. Достоверно улучшались объемы непосредственного запоминания (до лечения — 4,4 ± 1,1; после лечения — 5,4 ± 0,9), объемы второго воспроизведения (до — 5,3 ± 1,4; после — 6,1 ± 0,8), объемы отсроченного воспроизведения (до — 5,2 ± 1,1; после — 5,7 ± 1,4).
Представленные данные свидетельствуют, что к окончанию лечения у обследованных пациентов значительно улучшились количественные показатели теста, характеризующие состояние памяти и внимания. Это выразилось в запоминании большинства слов уже со второго или третьего предъявления (повторений), истощаемость к концу исследования была достоверно меньше.
По данным методики «поиск чисел по таблицам Шульте» до начала лечения у обследованных больных оперативная память была в пределах 42,1 ± 3,2 с.
После окончания курсового лечения препаратом Мексиприм результаты тестирования по таблицам Шульте показали достоверное (р < 0,01) уменьшение времени отыскивания чисел (от 42,1 ± 3,2 с до 31,7 ± 3,8 с).
Влияние препарата Мексиприм на двигательные функции по данным шкалы Тинетти
Результаты выполненного исследования свидетельствуют о положительном влиянии препарата Мексиприм и на двигательные функции больных с ДЭ гипертонического и атеросклеротического генеза. После лечения выявлено достоверное улучшение устойчивости и походки по шкале Тинетти, о чем свидетельствуют данные табл. 7.
Выводы
Терапия препаратом Мексиприм в течение 4 недель способствовала регрессированию субъективных и объективных симптомов ДЭ, развившейся на фоне атеросклероза и/или АГ. Препарат оказывает положительное влияние на психоэмоциональное состояние больных с ДЭ по шкалам депрессии и астенизации (улучшает настроение, повышает физическую и психическую активность, работоспособность и др.).
В комплексном лечении ДЭ Мексиприм приводит к достоверному улучшению двигательных и когнитивных функций. По результатам проведенного исследования выявлено улучшение внимания, кратковременной памяти, а также регуляторных функций на фоне лечения препаратом Мексиприм. Учитывая, что мнестические нарушения при ДЭ носят динамический характер и связаны с недостаточностью внимания и нарушением регуляции, отмеченное улучшение памяти на фоне лечения препаратом Мексиприм связано с влиянием именно на эти патогенетические звенья.
Обнаружено также достоверное улучшение устойчивости и походки, о чем свидетельствуют показатели шкалы Тинетти.
Препарат хорошо переносится пациентами и не вызывает побочных эффектов при длительном приеме.
Мексиприм может быть рекомендован к использованию в клинической практике для лечения больных с ДЭ, развившейся на фоне атеросклероза и/или АГ.
1. Волошин П.В., Міщенко Т.С., Лекомцева Є.В. Аналіз поширеності та захворюваності на нервові хвороби в Україні // Международный неврологический журнал. — 2006. — № 3(7). — С. 9-13.
2. WHO. World Health Report 2008. — Geneva: World Health Organization, 2008.
3. Мищенко Т.С. Эпидемиология цереброваскулярных заболеваний в Украине // Практична ангіоневрологія. — К., 2009. — № 1/1. — С. 5.
4. Мищенко Т.С., Мищенко В.Н. Современная диагностика и лечение неврологических заболеваний. Справочник врача. — К., 2010. — 470 с.
5. Евтушенко С.К. Дисциркуляторная энцефалопатия как анахронизм отечественной неврологии // Международный неврологический журнал. — 2010. — № 6(36). — С. 181-187.
6. Мищенко Т.С. Вопросы и ответы в неврологии. Справочник врача. — К.: Доктор-Медиа, 2012. — 432 с.
7. Максудов Г.А. Дисциркуляторная энцефалопатия (сосудистые заболевания нервной системы). — М., 1975. — С. 501-512.
8. Шмидт Е.В., Лунев Д.К., Верещагин Н.В. Дисциркуляторная энцефалопатия. Сосудистые заболевания головного и спинного мозга. — М., 1976. — С. 227-244.
9. Верещагин Н.В., Моргунов В.А., Гулевская Т.С. Патология головного мозга при атеросклерозе и артериальной гипертензии. — М., 1997. — 288 с.
10. Дамулин И.В., Захаров В.В. Дисциркуляторная энцефалопатия: Методические рекомендации. — М., 2000. —
20 с.
11. Батышева T.T., Артемова И.Ю. и др. Хроническая ишемия мозга: механизмы развития и современное комплексное лечение // Справочник практического врача — Т. 3. — М., 2004. — С. 18-23.
12. Болдырев А.А. Окислительный стресс и мозг // Соросовский образовательный журнал. — 2001. — № 7. — С. 21-27.
13. Федорова Т.Н. Окислительный стресс и защита головного мозга от ишемических повреждений: Дис... д-ра биол. наук. — М., 2004.
14. Challenging age-old ideas і about stroke // Lancet Neurol. — 2012. — Vol. 11(12). — 1013.
15. Маркин С.П. Современный подход к диагностике и лечению хронической ишемии мозга // Русский медицинский журнал. Неврология и психиатрия. — 2010. — № 8.— С. 445.
16. Гомазков O.A. Старение мозга и нейротрофическая терапия. — М.: ИКАР, 2011. — 178 с.
17. Бачинская Н.Ю. Нейропсихологические и нейрофизиологические аспекты синдрома умеренных когнитивных нарушений // Український вісник психоневрології. — 2007. — Т. 15, вип. 1(50), дод. — С. 18.
18. Мищенко Т.С. Новые мишени терапевтического воздействия у пациентов с хронической ишемией головного мозга // Международный неврологический журнал. — 2011. — № 2(40). — С. 7-17.
19. Бурчинский С.Г. Возможности и перспективы ноотропных средств при дисциркуляторной энцефалопатии // Журн. практичного лікаря. — 2005. — № 2. — С. 51-55.
20. Гусев Е.И. Ишемия головного мозга. — М.: Медицина, 2007. — 328 с.
21. Черний В.И. Ишемия головного мозга в медицине критических состояний. Нейропротекция (патофизиология, терминология, характеристика препаратов): Метод. рек. / В.И. Черний, А.Н. Колесников, Г.А. Городник. — К., 2007. — 72 с.
22. Adibhatla R.M. Citicoline: Neuroprotective mechanisms in cerebral ischemia // J. Neurochem. — 2002. — 80. — 12-13.
23. Tinetti M.E. // New Engl. J. Med. — 2003. — Vol. 348(1). — P. 42-49.

/95.jpg)
/96.jpg)
/97.jpg)