Международный неврологический журнал 2 (72) 2015
Вернуться к номеру
Досвід застосування препарату Медітан у пацієнтів із вторинним синдромом неспокійних ніг
Авторы: Мардзвік В.М. - Хмельницька міська лікарня; Мардзвік М.В. - Хмельницький обласний госпіталь інвалідів ВВВ
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
Стаття присвячена особливостям діагностики й різноманіттю клінічних проявів первинного та вторинного синдрому неспокійних ніг. Наведено основні рейтингові шкали для оцінки клінічного перебігу вказаної патології. Доведено ефективність застосування препарату Медітан у дозі 1200 мг у лікуванні вторинного синдрому неспокійних ніг на основі отриманих даних власного спостереження за 63 пацієнтами із діабетичною полінейропатією.
Статья посвящена особенностям диагностики и многообразию клинических проявлений первичного и вторичного синдрома беспокойных ног. Приведены основные рейтинговые шкалы для оценки клинического течения указанной патологии. Доказана эффективность применения препарата Медитан в дозе 1200 мг в лечении вторичного синдрома беспокойных ног на основе полученных данных собственного наблюдения за 63 пациентами с диабетической полинейропатией.
The article considers the features of diagnosis and variety of clinical manifestations of primary and secondary restless legs syndrome. Basic ratings scales to evaluate the clinical course of this pathology are presented. Efficiency of using Meditan at a dose of 1200 mg for the treatment of secondary restless legs syndrome, based on the findings of our own observation of 63 patients with diabetic polyneuropathy, has been proved.
синдром неспокійних ніг, цукровий діабет 2-го типу, діабетична полінейропатія, Медітан.
синдром беспокойных ног, сахарный диабет 2-го типа, диабетическая полинейропатия, Медитан.
restless legs syndrome, diabetes mellitus type 2, diabetic polyneuropathy, Meditan.
Статья опубликована на с. 51-55
Синдром неспокійних ніг (СНН) — стан, що характеризується неприємними відчуттями в нижніх кінцівках, що з’являються у спокої (частіше у вечірній і нічний час) та змушують хворого здійснювати рухи, що полегшують їх, і часто стають причиною порушення сну. Слід зазначити, що вперше СНН був описаний Томасом Віллісом у 1672 р. Вагомий внесок у вивчення синдрому зробив шведський невролог K.A. Ekbom, який у 1945 році проаналізував 53 випадки СНН, описав основні клінічні прояви і напрями терапії, завдяки чому СНН назвали синдромом Екбома [1, 10].
Відповідно до сучасних даних поширеність СНН серед дорослого населення становить 2–5 % [6, 17].
СНН зустрічається в усіх вікових групах, однак в осіб середнього та похилого віку його поширеність сягає 10–35 %. Проте не менше ніж в 1/3 випадків СНН має прояви і в осіб молодого віку [2, 20]. У жінок СНН зустрічається в 1,5 раза частіше, ніж у чоловіків. На думку деяких дослідників, ця диспропорція існує за рахунок того, що жінки частіше звертаються по медичну допомогу з приводу СНН [5]. Слід зауважити, що близько 15 % випадків хронічної інсомнії пов’язано з СНН [11].
Більше ніж у половині випадків СНН виникає за відсутності будь-якого неврологічного або соматичного захворювання. Виділяють первинний (ідіопатичний) і вторинний СНН. К.А. Еkbom уперше описав сімейний компонент первинного СНН. Клінічні спостереження свідчать про те, що принаймні 60 % осіб з ідіопатичним СНН мають обтяжений сімейний анамнез. Описано можливість автосомно-домінантного типу наслідування з майже повною пенетрантністю, але варіабельною експресивністю патологічного гена. Передбачають як полігенну, так і моногенну природу захворювання. У деяких сім’ях виявлений зв’язок СНН із локусами на 9, 12, 14-й хромосомах. Можливо, у значній частині випадків захворювання має мультифакторну природу та виникає в результаті складної взаємодії генетичних і зовнішніх факторів [3, 5, 11].
Пацієнти з первинним СНН мають тенденцію до дебюту в більш ранньому віці (до 45 років), симптоми зазвичай зберігаються протягом усього життя, проте їх інтенсивність може значно змінюватись, тимчасово посилюючись під час вагітності, стресу, після інтенсивних фізичних навантажень. У більшості випадків із часом має місце тенденція до повільного наростання симптомів, можуть спостерігатися періоди стаціонарного перебігу або ремісії, що продовжуються до кількох років [3].
Зазвичай вторинний СНН виникає після 50 років, на тлі деяких соматичних або неврологічних захворювань, при цьому клінічні прояви розвиваються відносно швидко, не мають ремісії та характеризуються тяжким перебігом. Вторинний СНН спостерігається при великій кількості захворювань і станів, однак основними етіологічними факторами залишаються залізодефіцитна анемія, вагітність, ниркова недостатність і полінейропатії [15, 12]. Недостатність заліза є одним із найбільш важливих факторів у розвитку цього синдрому.
Необхідно пам’ятати, що серед лабораторних показників найбільш інформативним є рівень феритину, а не вміст сироваткового заліза [3, 16].
Дані епідеміологічних досліджень свідчать про те, що симптоми СНН розвиваються у близько 20–25 % вагітних, частіше в III триместрі, і зникають незабаром після пологів. Основні причини поєднання СНН із вагітністю вірогідно не відомі. Існують гіпотези, згідно з якими розвиток цього синдрому пов’язаний не лише з дефіцитом заліза, фолієвої кислоти, а також із гормональними змінами у вигляді збільшення рівнів пролактину, прогестерону та естрогену [6, 13]. Серйозною клінічною проблемою СНН є у хворих з уремією, що спостерігається в 15–70 % пацієнтів [21]. Патогенез цього синдрому при термінальній стадії ниркової недостатності остаточно не з’ясовано, однак значна роль при цій патології також відводиться дефіциту заліза в організмі. Частими причинами вторинного СНН є полінейропатії, як набуті (алкогольна, діабетична, амілоїдна, порфірійна), так і спадкові. При полінейропатіях СНН зустрічається при переважному ураженні аксонів із залученням у процес тонких сенсорних волокон. За даними різних авторів, поширеність СНН при полінейропатіях знаходиться в межах від 5 до 54 % [12]. Слід відмітити, що випадки СНН також було описано при гіпотиреозі, тиреотоксикозі, хронічних обструктивних захворюваннях легенів, ревматоїдному артриті, хворобі Шегрена, порфірії, тяжкій серцевій недостатності, розсіяному склерозі, ураженнях спинного мозку й інших захворюваннях [14, 21]. У деяких випадках СНН спостерігався в пацієнтів із хворобою Паркінсона, проте серед дослідників немає єдиної думки про частоту, із якою трапляється СНН саме при цій хворобі. Іноді прояви СНН можуть спостерігатись у період стресу у здорових осіб або після інтенсивного фізичного навантаження, при надлишковому вживанні напоїв із високим вмістом кофеїну, алкоголю. Викликати або підсилити СНН можуть різні лікарські препарати, перш за все нейролептики, трициклічні антидепресанти, інгібітори зворотного захвату серотоніну, препарати літію, ніфедипін та інші антагоністи кальцію [10].
Діагноз СНН ґрунтується на чотирьох ключових ознаках, що вказані у критеріях (Diagnostic Criteria for RLS, 2012):
1. Неприємні відчуття в ногах, що змушують до рухової активності.
2. Прагнення здійснювати рухи або неприємні відчуття виникають або посилюються в спокої.
3. Прагнення здійснювати рухи або неприємні відчуття полегшуються або повністю зникають при рухах.
4. Прагнення здійснювати рухи або неприємні відчуття більш виражені у вечірній і нічний час.
У переважній більшості випадків ретельного аналізу скарг і клінічної картини цілком достатньо для встановлення діагнозу СНН [8]. Важливо проводити диференціальну діагностику з нічними крампі, акатизією, судинною патологією нижніх кінцівок і полінейропатією. Найчастіше диференціальна діагностика СНН проводиться саме з полінейропатією. Це пов’язано з деякими труднощами, оскільки на тлі невропатії, особливо діабетичної, уремічної, може спостерігатися розвиток вторинного СНН. Клінічна картина полінейропатії зазвичай представлена сенсорними порушеннями та симптомами вегетативних розладів. Сенсорні розлади проявляються болем і парестезіями, що часто посилюються у вечірній і нічний час і порушують сон. Досить часто в таких пацієнтів зустрічається СНН, що розглядається як вторинний щодо невропатії. З іншого боку, у деяких пацієнтів із первинним СНН при дослідженні виявляють приховану аксонопатію, що підтверджує роль периферичного відділу нервової системи в патогенезі цього синдрому [9, 15].
Відомо, що вітчизняна фармакологічна фірма «Фармак» є виробником препарату Медітан, діюча речовина якого — габапентин. Форма випуску препарату — капсули із дозуванням 100, 300 та 400 мг діючої речовини. Препарат належить до групи антиконвульсантів. Слід зазначити, що габапентин є амінокислотою, що за хімічною структурою подібна до гальмівних медіаторів гамма-аміномасляної кислоти (ГАМК). Проте він не взаємодіє з рецепторами ГАМК, не трансформується в процесі метаболічних реакцій ні в ГАМК, ні в агоністи ГАМК, не інгібує захват або розщеплення ГАМК, також габапентин не зв’язується з білками плазми крові. Препарат проникає через гематоенцефалічний бар’єр, його концентрація у спинномозковій рідині становить близько 20 % відповідної рівнозначної концентрації плазми крові. Габапентин практично не метаболізується в організмі людини, не викликає індукції або гальмування ферментів печінки, він має широкий спектр застосування та рекомендований для лікування СНН вторинного генезу, особливо у хворих із полінейропатією та наявним больовим синдромом.
Мета дослідження — оцінка ефективності препарату Медітан у пацієнтів із вторинним синдромом неспокійних ніг.
Матеріали та методи
Під нашим спостереженням знаходились 63 пацієнти. Умовно всіх хворих було розподілено на основну та контрольну групи. До основної групи увійшли 43 пацієнти, із них було 46,5 % (20) чоловіків, 53,5 % (23) — жінок. Середній вік становив у чоловіків 67,0 ± 3,5 року, у жінок — 65,0 ± 3,2 року.
До контрольної групи увійшли 20 пацієнтів — 10 чоловіків і 10 жінок. Пацієнти обох груп страждали від цукрового діабету 2-го типу. Середня тривалість перебігу хвороби була в межах 8,7 ± 2,1 року. Слід зазначити, що в 90,6 % (39) хворих основної та у 85,0 % (17) хворих контрольної групи цукровий діабет 2-го типу був у стадії субкомпенсації. На основі загальноприйнятих критеріїв у хворих основної та контрольної групи було діагностовано тяжке ускладнення перебігу цукрового діабету 2-го типу у вигляді діабетичної полінейропатії. В основній групі в 74,5 % (32) пацієнтів було виявлено симетричну сенсорну, а у 25,5 % (11) пацієнтів — сенсомоторну форму діабетичної полінейропатії. У контрольній групі сенсорну форму було діагностовано у 80 % (16) випадків, а сенсомоторну — у 20 % (4) випадків відповідно.
У хворих обох груп на основі критеріїв відповідно до консенсусу IRLSSG (Diagnostic Criteria for RLS 2012) було діагностовано вторинний СНН.
Із метою встановлення ступеня тяжкості клінічних проявів та оцінки ефективності лікування СНН використовували сучасні рейтингові шкали:
— Міжнародну шкалу СНН (The International Restless Legs Syndrome scale — IRLS) — 10-компонентна шкала з бальним діапазоном від 0 (найкраще) до 40 (найгірше), за допомогою якої оцінювали інтенсивність та частоту первинних проявів хвороби, асоційовані розлади сну і її вплив на настрій і повсякденне функціонування та класифікували за ступенем тяжкості — легкий (1–10 балів), помірний (11–20 балів), тяжкий (21–30 балів) або дуже тяжкий (31–40 балів);
— шкалу загального враження від клінічного поліпшення (The Clinician Global Impression Improvement scale) — рейтингова шкала, де оцінювали тяжкість захворювання і поліпшення порівняно з вихідним станом хворого в балах від 1 (виражене поліпшення) до 7 (виражене погіршення), а також терапевтичний і побічні ефекти лікування; клінічно значущими критеріями відповіді на лікування були оцінка пацієнта як «істотне поліпшення» (much improved) і «дуже виражене поліпшення» (very much improved).
Пацієнти контрольної групи отримували терапію, рекомендовану при цукровому діабеті 2-го типу та діабетичній полінейропатії (корекція рівня глюкози крові метаболічна, антиоксидантна терапія, вітаміни групи В), у свою чергу, пацієнтам основної групи до загального лікування було призначено препарат Медітан у дозі 1200 мг на добу за один прийом у вечірній час. Стаціонарний курс лікування в середньому становив 16,5 ± 1,5 доби.
Результати та їх обговорення
Пацієнти основної та контрольної групи із наявним вторинним СНН скаржились на відчуття «ворушіння» під шкірою, проходження електричного струму та відчуття дискомфорту, що примушувало їх ворушити ногами. Описані відчуття були локалізовані переважно в глибині гомілок, меншою мірою — у стопах і стегнах та зазвичай виникали з обох сторін. Чим довше пацієнти знаходились у стані спокою, у положенні сидячи та особливо лежачи, тим швидше в них було відмічено виникнення неприємних відчуттів і бажання до здійснення рухів. Щоб полегшити свій стан, хворі були вимушені витягувати або згинати кінцівки, струшувати, розтирати чи масажувати їх, повертатися в ліжко, вставати й ходити по кімнаті, переминатися з ноги на ногу. Пацієнти відмічали, що під час ходьби неприємні відчуття зменшувались, однак вони знову з’являлися після того, як рухи припинялися. Зазвичай прояви СНН виникали увечері, у середньому через 15–30 хвилин після того, як хворий лягав у ліжко. Якщо пацієнт не зміг заснути, неприємні відчуття починали турбувати його приблизно до 2–3-ї години ночі, після чого швидко зменшувалися й поступово зникали.
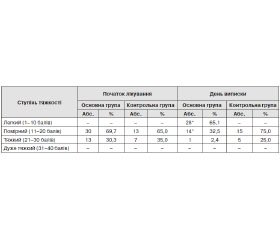
Слід зауважити, що в процесі обстеження в пацієнтів основної групи у 69,7 % (30) випадків було встановлено помірний ступінь, а в 30,3 % (13) випадків — тяжкий ступінь клінічних проявів СНН. У свою чергу, у контрольній групі помірний ступінь клінічних проявів було діагностовано в 65,0 % (13) пацієнтів, у 35,0 % (7) — тяжкий ступінь відповідно.
Клінічно значущими критеріями відповіді на лікування ми визначали зниження тяжкості СНН із дуже тяжкого або тяжкого до середнього або легкого ступеня та зменшення сумарної кількості балів на ≥ 50 % порівняно з початковим (відповідно до міжнародної шкали СНН).
У табл. 1 наведено динаміку зміни ступеня тяжкості клінічних проявів у пацієнтів обох груп із вторинним СНН відповідно до шкали IRLS на день надходження й на момент виписування зі стаціонару. Таким чином, відповідно до даних табл. 1 за період стаціонарного лікування в 93,3 % (28) хворих ступінь прояву СНН із помірного став легким, а у 92,3 % (11) — із тяжкого став помірним. У той час як у контрольній групі за період стаціонарного лікування вірогідно позитивну динаміку на фоні стандартної терапії було виявлено лише у 2 пацієнтів.
Було встановлено вірогідне зниження сумарної кількості балів на ≥ 50 % порівняно з початковим, а саме середній бал при помірних проявах знизився з 18,3 ± 1,5 до 7,2 ± 1,2 (р < 0,05), при тяжких проявах — із 27,4 ± 2,1 до 12,1 ± 1,3 (р < 0,05) відповідно.
За рейтинговою шкалою загального враження від клінічного поліпшення (CGII scale) серед пацієнтів основної групи із позитивною динамікою терапевтичну ефективність було визначено як «істотне поліпшення» в 32 (82,1 %) випадках та «дуже виражене поліпшення» в 7 (17,9 %) випадках відповідно. Слід зазначити, що в 3 пацієнтів ефективність було визначено як «помірне поліпшення».
Отже, на нашу думку, використання препарату Медітан у середній рекомендованій терапевтичній дозі в 1200 мг є достатньо ефективним у лікуванні вторинного синдрому неспокійних ніг пацієнтів із діабетичною полінейропатією на фоні цукрового діабету 2-го типу та суттєво покращує якість їх життя.
Висновки
1. Вторинний СНН на фоні діабетичної полінейропатії — доволі поширене неврологічне захворювання, діагностика якого не вимагає складних і трудомістких досліджень і базується на клінічному аналізі симптомів, що виявляються в пацієнта.
2. Препарат Медітан продемонстрував високу ефективність у лікуванні вторинного СНН на фоні діабетичної полінейропатії та може бути рекомендованим для широкого застосування.
3. Вторинний СНН є контрольованим захворюванням, а отже, рання діагностика й раціонально підібрана терапія можуть значно поліпшити якість життя більшості пацієнтів.
1. Аверьянов Ю.Н., Подчуфарова Е.В. Синдром беспокойных ног // Неврологический журнал. — 1997. — № 3. — С. 12-16.
2. Левин О.С. Синдром беспокойных ног // Диагностика и лечение экстрапирамидных расстройств / Под ред. В.Н. Штока. — М., 2000. — С. 124-138.
3. Левин О.С. Синдром беспокойных ног // Экстрапирамидные расстройства. Руководство по диагностике и лечению / Под ред. В.Н. Штока, И.А. Ивановой-Смоленской, О.С. Левина. — М.: Медпресс-информ, 2002. — С. 425-434.
4. Обухова А.В., Артемьев Д.В. // Синдром беспокойных ног // Cons. Med. — 2010. — № 96 (12). — С. 72-7.
5. Allen R.P., Walters A.S., Monplaisir J. et al. Restless legs syndrome // Slep. Med. — 2003. — V. 4. — P. 101-119.
6. Allen R.P. Contraversies and challenges in defining etiology and pathophysiology of restless legs syndrome // Am. J. Med. — 2007. — V. 120. — S. 13-21.
7. Becker P.M., Jamieson A.O., Brown W.D. Dopaminergic agents in restless legs syndrome and periodic limb movements of sleep: response and complications of extended treatment in 49 cases // Sleep. — 1993. — V. 16. — P. 713-716.
8. Brindani F., Vitetta F., Gemignani F. Restless legs syndrome: differential diagnosis and management with pramipexole // Clin. Interv Aging. — 2009. — № 4. — Р. 305-13.
9. Chokroverty S. Differential Diagnosis of restless legs syndrome // Restless Legs Syndrome / Ed. by W.A. Hening, R.P. Allen, S. Chokroverty et al. — Elsevier, 2009. — Р. 111-118.
10. Ekbom K.A. Restless legs // Acta Med. Scand. — 1945. — V. 158. — P. 5-123.
11. Earley C.J. Restless legs syndrome // N. Engl. J. Med. — 2003. — V. 348. — P. 2103-2109.
12. Gemignani F., Brindani F., Negrotti A. Restless legs syndrome and polyneuropathy // Mov. Disord. — 2006. — V. 21 (8). — P. 1254-1257.
13. Hening W., Walters A.S., Allen R.P. et al. Impact, diagnosis and treatment of restless legs syndrome (RLS) in a primary care population: the REST (RLS epidemiology, symptoms, and treatment) primary care study // Sleep Med. — 2004. — V. 5 (3). — P. 237-246.
14. Natarajan R. Review of periodic limb movement and restless legs syndrome // J. Postgrad. Med. — 2010. — V. 56 (2). — P. 157-162.
15. O’Keeffe S.T. Secondary causes of restless legs syndrome in older people // Age and Ageing Advance Access published. — 2005 May. — № 10. — Р. 2005.
16. Patrick L. Restless Legs Syndrome: Pathophysiology and the Role of Iron and Folate // Alternative Medicine Review. — 2007. — V. 12, № 2.
17. Paulus W., Trenkwalder C. Pathophysiology of dopaminergic therapy — related augmentationin rextlesslegs syndrome // Lancet Neurology. — 2006. — V. 5. — P. 878-886.
18. Phillips B., Young T., Finn L. et al. Epidemiology of restless legs symptoms in adults // Arch. Int. Med. — 2000. — V. 160. — P. 2137-2141.
19. Saletu M., Anderer P., Saletu-Zyhlarz G. et al. Restless legs syndrome (RLS) and periodic limb movement disorder (PLMD) acute placebo-controlled sleep laboratory studies with clonazepam // Eur. Neuropsychopharmacol. — 2001. — V. 11. — P. 153-161.
20. Ulfberg J., Nystrom B., Carter N. et al. Prevalence of restless legs syndrome among men aged 18 to 64 years: an association with somatic disease and neuropsychiatric symptoms // Mov. Disord. — 2001. — V. 16. — P. 1159-1163.
21. Winkelmann J., Prager M., Lieb R. et al. Anxietas tibiarum. Depression and anxiety disorders in patients with restless legs syndrome // J. Neurol. — 2005. — V. 252 (1). — Р. 67-71.
Вперше опубліковано в журналі
«Практикуючий лікар», 2014, № 1

/53/53.jpg)