Статья опубликована на с. 169-176
Рассеянный склероз (РС) — хроническое демие-линизирующее заболевание головного и спинного мозга, отличающееся разнообразием неврологических симптомов, развивающееся преимущественно у лиц молодого возраста [1–3].
В основе данного заболевания лежит развитие процессов демиелинизации, аутоиммунного воспаления [4].
Сочетанное развитие воспалительных и нейродегенеративных процессов в головном и спинном мозге приводит к атрофии структур центральной нервной системы (ЦНС) [5–7].
Основными этапами патогенеза РС являются: 1) развитие воспалительных патологических реакций, сопровождающихся активацией иммунокомпетентных клеток, действием провоспалительных медиаторов; 2) деструкция миелина; 3) аксональная дегенерация, атрофия [1, 8].
Совокупность вышеуказанных реакций вызывает нарушение проведения нервных импульсов по проводящим путям ЦНС и обусловливает развитие разнообразных неврологических проявлений РС, таких как пирамидные, мозжечковые, чувствительные нарушения, симптомы поражения ствола головного мозга, развитие ретробульбарного неврита, а также когнитивных и эмоционально-аффективных нарушений, сексуальной дисфункции [1, 9].
Малоизученной остается роль неспецифических систем в этиологии РС. Известно, что неспецифические системы, функционально объединенные в единый интегративно действующий механизм, регулируют функциональное состояние головного мозга, уровень сна и бодрствования, участвуют в модуляции передачи сенсорной информации, влияют на двигательные и вегетативные функции организма [10].
Сохранность неспецифических механизмов головного мозга не только контролирует адаптивные реакции организма, но и во многом определяет компенсаторные возможности больных при различных заболеваниях ЦНС [11, 12].
В последнее время возрос интерес к изучению проблемы ночного сна и его нарушений при различных заболеваниях ЦНС [11, 13, 14].
Статистические исследования показали, что более 50 % больных рассеянным склерозом предъявляют жалобы на различные нарушения ночного сна [15].
Показано, что расстройства сна являются декомпенсирующим фактором, усиливают астенизацию у больных РС на фоне других неврологических синдромов, увеличивают вероятность частых экзацербаций, влияющих на тяжесть течения РС [12, 15].
Результаты современных исследований указывают на определенную роль нарушения циркадной регуляции секреции мелатонина в развитии инсомнии у лиц, страдающих РС. Это подтверждалось снижением показателей эффективности сна, а также достоверным снижением суточных концентраций мелатонина сульфата в моче [10].
Поэтому объективное исследование структуры ночного сна поможет глубже изучить роль неспецифических систем мозга в патогенезе РС, что поможет в дальнейшем разработать новые подходы к лечению этих больных.
Цель: изучить особенности функционирования неспецифических систем головного мозга у больных РС на основе клинических, биохимических и полисомнографических исследований.
Методы
Исследование проведено на 25 больных рассеянным склерозом в возрасте от 22 до 50 лет. Мы обследовали больных с крайними вариантами течения РС — 18 больных рассеянным склерозом с ремиттирующим течением (РРС), 7 больных с первично-прогредиентным течением (ППРС). У всех пациентов, участвующих в исследовании, диагноз подтвержден в соответствии с критериями McDonald, 2005.
Обследование больных с ремиттирующим течением РС проводилось в стадии ремиссии, с учетом возможного развития бессонницы — одного из системных побочных эффектов глюкокортикостероидов, применяемых для купирования экзацербаций.
Клиническое исследование проводилось с использованием специально разработанных оценочных шкал Kurtzke: шкала неврологического дефицита (FS, от англ. functional system) и расширенная шкала инвалидизации (Expanded Disability Status Scale, EDSS).
В целях выделения клинических вариантов нарушений сна у больных РС с различными типами течения мы использовали специальные шкалы-опросники, где подробным образом выявляли характер расстройств сна в течение месяца.
Биохимические исследования проводились с помощью оценки уровня мелатонина сульфата. Определялся уровень экскреции 6-сульфатоксимелатонина в утренней порции мочи с помощью реактивов для иммуноферментного анализа фирмы IBL International (Germany). Детекция оптической плотности осуществлялась с помощью микропланшетного анализатора GBG Stat Fax 2100 (USA).
Для полиграфических исследований ночного сна применяли компьютерный комплекс «Нейрон-Спектр+». Больным РС запись полиграммы проводилась до назначения базовой терапии. Полиграмма ночного сна включала электроэнцефалограмму (монополярные отведения С3А1, С4А2, О1А1, О2А2 по системе «10–20»), электроокулограмму, электромиограмму и электрокардиограмму. Оценка структуры ночного сна осуществлялась по Международной классификации стадий и фаз сна. При анализе структуры ночного сна и построении гипнограммы использовали эпохи длительностью 30 с. Расчет показателей ночного сна проводился с помощью программного обеспечения «Нейрон-Спектр-ПСГ». Достоверность различий между группами наблюдений оценивалась с использованием непараметрического критерия Манна — Уитни.
Результаты
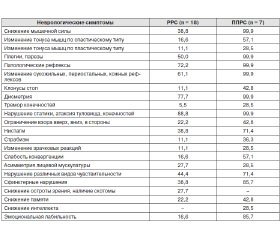
Особенность клинических проявлений у больных с РС — грубый, динамический характер неврологических нарушений. Как показали результаты клинических исследований, у всех больных РС наблюдались определенные субъективные проявления (табл. 1).
В клинической картине общими наиболее частыми были жалобы на общую слабость, утомляемость, мышечную слабость, нарушение акта ходьбы, неловкость и скованность движений. В меньшей степени были выражены такие симптомы, как нарушение речи, двоение в глазах (5,5 %) у больных РРС. У всех больных клиническая симптоматика была значительнее выражена при первично-прогредиентном типе течения.
Все обследованные нами больные жаловались на наличие пароксизмально возникающих мышечных спазмов, судороги конечностей, болезненность при движении глазных яблок, двоение в глазах, онемение конечностей, парестезии.
Парестезии характеризовались ощущением жжения, покалывания в конечностях, преимущественно в ночное время суток.
Наряду с описанными жалобами довольно часто больных беспокоили головокружения, в основном системные, центрального характера. В этих случаях у больных возникало ощущение вращения окружающих предметов, движение по кругу или взад-вперед. Головокружения совпадали с шаткостью при ходьбе. Следует отметить, что жалобы на ухудшение зрения, наличие темного пятна в поле зрения встречались только у больных с ремиттирующим типом течения РС. Все обследованные больные отмечали жалобы на нарушение речи. У всех больных наблюдались симптомы сфинктерных нарушений. Среди них наиболее часто встречались жалобы на задержку мочеиспускания, недержание мочи. Также отмечались императивные позывы на мочеиспускание, чувство неполного опорожнения мочевого пузыря, недержание кала, запоры.
Одно из ведущих мест в клинической картине нарушений сна у больных РС занимали расстройства засыпания. Основные его причины — чувство напряжения, боли, мышечные спазмы конечностей, сфинктерные нарушения, переживаемые во время дневного бодрствования чрезмерные положительные, отрицательные эмоции, мысли о своем самочувствии, возникающие перед сном и т.д. В группе РРС больные жаловались на невозможность уснуть в течение 30 минут с частотой: меньше чем 1 раз в неделю — 28,3 % больных, 3 раза и более в неделю — 18,8 % больных. У 52,8 % больных такие жалобы не возникали ни разу за последний месяц от момента обследования. В группе ППРС невозможность –уснуть в течение 30 минут с частотой 3 раза и более в неделю отмечали все больные.
Достаточно часто, чтобы уснуть, больные принимали снотворные препараты, прописанные врачом или самостоятельно. Так, в группе РРС препараты использовали 75,4 % больных с частотой приема: меньше чем 1 раз в неделю — 9,4 % больных, 1 или 2 раза в неделю — 28,3 % больных, 3 раза и более в неделю — 37,7 % больных. Не использовали снотворные препараты ни разу за последний месяц 24,5 % обследованных.
В группе ППРС снотворные препараты принимали все больные с частотой 3 раза и более в неделю.
Таким образом, жалобы на невозможность уснуть в течение 30 минут были более выражены у больных с ППРС, что провоцировало более частое использование снотворных препаратов в этой группе.
Процесс засыпания у больных РС протекал c определенными различиями. Больные РРС характеризовали его в одних случаях как «постепенное» (56,6 % больных), в других — как «незаметное проваливание в сон» (43,3 % больных). При ППРС все больные отмечали «незаметное проваливаниев сон».
У всех больных РС отмечалось сокращение общей длительности сна, что было связано с ночными, а также ранними утренними пробуждениями. В группе РРС 75,5 % больных просыпались посреди ночи (1–2 пробуждения за ночь) или рано утром с частотой 3 раза и более в неделю; 9,4 % больных — с частотой 1 или 2 раза в неделю; 15 % больных не отмечали ночных и ранних утренних пробуждений ни разу за последний месяц. В группе ППРС в отличие от группы РРС все больные просыпались посреди ночи (3–4 пробуждения за ночь) или рано утром с частотой 3 раза и более в неделю.
Причины пробуждения были разнообразны и вызывали проблемы со сном у больных РС с различной частотой. Посторонний звук (кашель, громкий храп, шум) создавал проблемы со сном в группе РРС меньше чем 1 раз в неделю (28,3 % больных), в группе ППРС — у всех больных с частотой более 3 раз в неделю. Субъективные ощущения изменения окружающей температуры (было слишком холодно или жарко) беспокоили больных в группе РРС меньше чем 1 раз в неделю (37,7 % больных), в группе ППРС — 3 раза или более в неделю (60 % больных).
Больные также предъявляли жалобы на чувство нехватки воздуха, которое провоцировало пробуждение. Среди группы РРС такие жалобы встречались у 18,8 % больных с частотой меньше чем 1 раз в неделю и не были выявлены у больных ППРС.
Также у больных РС отмечались возникающие во время сна боли в конечностях, мышечные спазмы, нарушения мочеиспускания (никтурия, императивные позывы). Такие жалобы также являлись причиной проблем со сном в целом, возникающих у больных РС с определенной для каждой группы частотой: в группе РРС — меньше чем 1 раз в неделю (28,3 % больных), 1 или 2 раза в неделю (9,4 % больных), 3 раза и более в неделю (37,7 % больных.); в группе ППРС — 3 раза и более в неделю у всех больных.
Со слов родственников, в группе РРС отмечались вздрагивания во время сна с частотой менее чем 1 раз в неделю (28,3 % больных), 3 раза и более в неделю (47,1 %), в группе ППРС — 3 раза и более в неделю у всех больных.
Помимо описанных нарушений сна, у больных РС отмечалось ухудшение качества ночного сна. Качество сна в группе РРС было оценено как «хорошее» — 56,6 % больных, «плохое» — 24,5 %, «очень плохое» — 18,8 % больных.
В группе ППРС 54,5 % больных оценили качество сна как «плохое» и 45,5 % — как «очень плохое».
При субъективной оценке характера ночного сна в группе РРС 37,7 % больных отмечали спокойный сон, 62,2 % — прерывистый сон. В группе ППРС все больные говорили о поверхностном сне.
Довольно часто больные РС наблюдали замедленный переход от сна к бодрствованию и трудность с включением в активную деятельность. Более чем у половины больных РРС — бодрость в вечернее время суток (62,2 % больных), чувство бодрости утром среди них отмечали лишь 37,7 % больных. Подавляющее число больных в середине дня испытывали общую слабость (66 % больных), сонливость (75,4 %), разбитость (47,1 %). В группе ППРС все больные отмечали чувство бодрости в утреннее время суток, выраженную общую слабость, разбитость в вечернее время суток, а также дневную сонливость.
В свою очередь, у большинства обследованных наблюдались изменения дневной активности, трудоспособности. Так, большинство больных в группе РРС жаловались на незначительное снижение внимания (43,3 %). Отмечали рассеянность, потерю интереса к поддержанию активной деятельности, заторможенность 37,7 % больных; высокий, но не максимальный уровень активности в течение дня — 18,8 % больных.
В группе ППРС такие жалобы отмечались больше чем у половины больных (54,5 % больных), у остальных — незначительное снижение внимания.
Таким образом, у обеих групп выявлены различные клинические варианты нарушений сна в виде затрудненного засыпания, сокращения общей длительности ночного сна, ухудшения качества, уменьшения глубины сна. Наряду с этим отмечались расстройства дневного бодрствования, что проявлялось периодической сонливостью в середине дня, приводившей к снижению работоспособности в этот период времени. Субъективные жалобы на те или иные нарушения сна были представлены в виде симптомокомплекса. Например, в одних случаях больные отмечали как удлинение засыпания, так и уменьшение продолжительности сна, в других — к этим расстройствам добавлялись нарушения качества сна, его глубины. Для обоих типов течения РС была характерна различная степень выраженности клинической симптоматики, которая преобладала у больных с ППРС.
При анализе анамнестических данных больных в динамике было выявлено, что состояние всех больных ухудшалось, в неврологическом статусе выявлена симптоматика, свидетельствующая об органическом поражении головного мозга (табл. 2).
/173/173.jpg)
Как следует из табл. 2, плегии, парезы, снижение мышечной силы, изменение мышечного тонуса встречались в обеих группах, однако в случае первично-прогредиентного течения РС гораздо чаще. У больных с ППРС превалировали изменения мышечного тонуса по спастическому типу. Также в обеих группах отмечалось повышение сухожильных и периостальных рефлексов, исчезновение либо снижение брюшных рефлексов, клонусы стоп. Патологические рефлексы (симптом Штрюмпеля, Бабинского, Оппенгейма, Россолимо), преимущественно с нижних конечностей, наблюдались у обеих групп. Однако при РРС стопные патологические знаки встречались реже. Наряду с этими неврологическими проявлениями у некоторых больных наблюдалась экстрапирамидная симптоматика. Она проявлялась в виде тремора пальцев рук, век, симптома Нойка, изменения мышечного тонуса по пластическому типу. У всех больных отмечались нарушения статики, дисметрия, атаксия туловища и конечностей, наблюдалась стволовая симптоматика. Однако при ремиттирующем типе течения реже встречались ограничение взора вверх, в стороны, слабость конвергенции, слабость реакции зрачков на свет, нистагм, страбизм. Практически в равной степени была представлена асимметрия лицевой мускулатуры. У всех больных были выявлены чувствительные расстройства. Причем отмечались преимущественно нарушения простых видов чувствительности: болевой, тактильной, в основном по гемитипу. Также наблюдались описанные выше тазовые расстройства, реже выявляемые при ремиттирующем типе РС. У больных с ремиттирующим типом РС чаще выявлялось снижение остроты зрения, наличие скотом. Однако не были выявлены признаки снижения интеллекта, наблюдаемые у больных с первично-прогредиентным РС в 28,5 % случаев. У больных обеих групп отмечались расстройства памяти, что проявлялось в ухудшении запоминания фамилий, текущих событий. Также у 85,7 % с первично-прогредиентным типом течения была выявлена эмоциональная лабильность, тогда как среди больных с ремиттирующим типом течения — у 16,6 % больных.
Таким образом, у больных обеих групп выявлена общая объективная неврологическая симптоматика, отличающаяся полиморфизмом своих проявлений, но более выраженная при ППРС, что обусловлено отсутствием стойких, длительных ремиссий, давностью заболевания, появлением новых симптомов в динамике развития заболевания, а также стойкой инвалидизацией больных.
Результаты исследования уровня экскреции мелатонина сульфата в утренней моче показали, что в группе больных РС уровень мелатонина сульфата достоверно (р ≤ 0,05) ниже (28,2 ± 5,8) в сравнении с группой здоровых (49,7 ± 2,6). Было также выявлено, что у больных РРС количество мелатонина сульфата снижено (45,1 ± ± 7,6), но достоверно не отличается от данных по группе здоровых. В группе ППРС уровень мелатонина сульфата (11,32 ± 4,00) достоверно ниже по сравнению как со здоровыми, так и больными РРС. Резкое уменьшение уровня мелатонина сульфата в утренней моче у больных ППРС может свидетельствовать об изменении как ритма, так и количественной секреции гормона, что, в свою очередь, может приводить к развитию десинхроноза и его негативным последствиям у этих больных.
Анализ особенностей структуры ночного сна у больных РС позволил выявить общую направленность изменений при разных типах течения заболевания, а именно — сокращение продолжительности сна; увеличение времени бодрствования в период сна за счет частых пробуждений; сокращение длительности фазы медленноволнового сна (ФМС), сокращение числа завершенных циклов сна и низкий индекс эффективности сна.
Качественный анализ особенностей структуры ночного сна у больных РРС и ППРС показал, что для больных РРС были характерны удлинение первого цикла сна, частые и длительные пробуждения, частые переходы на поверхностные стадии сна, снижение представленности как глубокого медленноволнового сна, так и фазы быстрого сна (ФБС). У больных ППРС ночной сон характеризовался максимальной представленностью дельта-сна и ФБС в первом цикле сна и грубой «деформацией» последующих циклов с усилением процессов фрагментации сна.
Количественный сравнительный анализ структуры ночного сна в группах РРС и ППРС позволил выявить, что достоверно (р ≤ 0,05) различается только время засыпания, причем в группе ППРС процесс засыпания короче (табл. 3).
Обращает внимание наличие большого диапазона разброса параметров структуры ночного сна в обеих группах, что не позволило получить достоверных отличий. Однако нам удалось проследить определенные тенденции, позволяющие показать разницу в организации ночного сна при РРС и ППРС.
Как видно из табл. 3, в группе ППРС длительность латентных периодов всех стадий ФМС и ФБС существенно ниже, чем в группе РРС, что свидетельствует о повышенной потребности больных ППРС как в глубоком медленноволновом сне, так и в быстром сне, в то время как у больных РРС механизмы запуска этих стадий и фаз нарушаются. У больных ППРС отмечено также укорочение длительности ФМС в целом, в первую очередь ее наиболее синхронизированной стадии С4, снижена длительность ФБС, все стадии и фазы ночного сна представлены короткими сегментами, что может снижать восстановительную функцию ночного сна и адаптивные возможности у этих больных. Общая продолжительность сна при ППРС короче, несмотря на то, что длительность бодрствования и количество ночных пробуждений в этой группе несколько меньше. В обеих группах наблюдения выявлена высокая вариабельность сердечного ритма.
Выводы
Таким образом, проведенное исследование позволило выявить недостаточность адаптивно-компенсаторных возможностей у больных РС, обусловленную как специфическими патогенетическими особенностями заболевания, так и нарушением функционирования неспецифических (синхронизирующих и десинхронизирующих) механизмов регуляции интегративной деятельности мозга. По данным клинического исследования было выявлено, что при первично-прогредиентном течении РС механизмы компенсации поврежденных функций мозга нарушены более значимо, что явилось одной из причин отсутствия длительных стойких ремиссий и быстрого формирования грубого неврологического дефицита у этих больных. У всех обследованных больных РС выявлено нарушение процессов организации и поддержания стадий и фаз ночного сна, обусловленное нарушением баланса между синхронизирующими и десинхронизирующими механизмами мозга. Отмечено снижение уровня мелатонина сульфата в утренней моче больных РС, со значимым преимуществом при первично-прогредиентном течении заболевания, что приводило к сбою в функционировании прежде всего синхронизирующих мозговых систем, контролирующих стабильность течения сна и определяющих адаптивно-восстановительные функции сна. Полученные результаты необходимо учитывать при оценке сохранности функционирования неспецифических систем мозга у больных РС, при прогнозировании типа течения РС, а также при подборе и проведении лечебно-профилактических мероприятий.

/171/171.jpg)
/173/173.jpg)
/174/174.jpg)