Статья опубликована на с. 85-89
Актуальность темы
Мигрень — распространенное заболевание, проявляющееся в виде приступов интенсивной головной боли, которое часто сопровождается сенсорными, вегетативными и неврологическими симптомами. По разным данным, 12–15 % населения земного шара страдают мигренью, у 10 % из которых приступы мигрени возникают еженедельно (примерно 100 млн человек) [5]. В популяции среди женщин мигренью болеют 18 %, среди мужчин — 6 % и среди детей — 4 %. Среди пациентов, страдающих мигренью, более 85 % женщин и 82 % мужчин отмечают, что заболевание снижает качество их жизни. По данным Всемирной организации здравоохранения, мигрень увеличивает риск развития инсульта в 16 раз [4]. Не будучи фатальным заболеванием, мигрень приносит огромные убытки экономике в связи с пропусками на работе и учебе во время приступов [2].
Несмотря на более чем длительную историю изучения мигрени, не существует единого мнения относительно этиологии и патогенеза этого заболевания. Существующие методы патогенетического и симптоматического лечения мигрени не позволяют добиться стойкого уменьшения числа приступов, а порой и вовсе не оказывают никакого терапевтического эффекта. Превентивная терапия повторных мигренозных атак не всегда оказывает ожидаемый терапевтический эффект [1, 2].
Все вышеуказанное говорит о чрезвычайной актуальности и важности поиска дополнительных методов диагностики и лечения мигрени.
Транскраниальная магнитная стимуляция (ТМС) является относительно новым методом в медицине, с помощью которого мы можем влиять на нервную систему человека [3]. Основа действия метода ТМС — стимуляция нервной ткани с использованием переменного магнитного поля, способная подавлять или активировать различные участки коры головного мозга и базирующаяся на открытии Фарадеем (1831 г.) закона о том, что «переменное магнитное поле индуцирует электрический ток в расположенном рядом проводнике, причем сила тока прямо пропорциональна частоте изменения магнитного поля» [11].
Начиная с середины 80-х годов прошлого века, после изобретения первого коммерческого магнитного стимулятора [7], прошло несколько этапов становления этого метода. В настоящее время транскраниальная магнитная стимуляция — важный диагностический и терапевтический метод, который применяется при большом разнообразии патологических состояний. В доступной литературе отмечается, что купирование мигренозного приступа возможно с помощью транскраниальной магнитной стимуляции [8, 9], при этом есть только единичные публикации о применении ТМС в качестве средства превентивной терапии при мигрени [6], а также мы не нашли данных о влиянии применения ТМС на выраженность депрессивного расстройства при мигрени.
Цель исследования: изучить терапевтический эффект повторяющейся транскраниальной магнитной стимуляции при мигрени на примере группы пациентов с неэффективным медикаментозным лечением.
Материалы и методы
Проведены обследование и лечение методом повторяющейся ТМС (пТМС) 10 пациентов с неэффективным медикаментозным лечением, мужчин было 2, женщин — 8. Средний возраст составил 38,8 ± 10,2 года.
Исследование проходило на базе лечебно-диагностического центра «ВИТА-МЕД І» в г. Одессе. Всем пациентам проводилась МРТ головного мозга с целью исключения патологических образований, способных вызывать головную боль.
Все пациенты предъявляли жалобы на головную боль, которая классифицирована как мигрень без ауры (простая мигрень), согласно Международной классификации головных болей второго пересмотра (МКГБ ІІ).
Для оценки тяжести мигрени нами использована шкала нарушения повседневной активности при мигрени — MIDAS (Migraine Disability Assessment). Интенсивность головной боли при мигрени оценивалась с помощью визуальной аналоговой шкалы боли (ВАШ). Для оценки выраженности депрессивных включений была использована шкала Гамильтона.
Магнитная стимуляция проводилась на аппарате «Нейро-МС/Д» производства компании «Нейрософт». Наш стимулятор оснащен индуктором типа «бабочка», максимальная индуктивность составляет 1,6 Тл, максимальная частота магнитных стимулов в режиме повторяющейся стимуляции — 20 Гц.
Все пациенты получали пТМС по протоколу: 5 Гц с интенсивностью 120 % от моторного порога (моторный порог — наименьшая интенсивность, при которой вызывается простейший моторный ответ), длительностью 10 минут на дорсолатеральную префронтальную кору (ДЛПФК). Длительность трейна — 10 секунд, межтрейновый интервал — 10 секунд. Данный протокол выбран неслучайно. Он основывается на экспериментальных данных, доказывающих, что стимуляция ДЛПФК способна изменять метаболизм серотонина и, как следствие, уменьшать боль при мигрени [8]. Все пациенты проходили магнитную стимуляцию через равные промежутки времени, всего 10 сеансов в одинаковое время суток. Использованный нами протокол не противоречит существующему руководству по безопасному применению ТМС в медицине [10].
Результаты
Причиной обращения пациентов за помощью была длительная неэффективность лекарственной терапии, в связи с чем прием препаратов был прекращен. Данные пациенты самостоятельно отказались от медикаментозного лечения, при котором использовались НПВС (ацетилсалициловая кислота, ибупрофен, метамизол натрия), триптаны, СИОЗС и комбинированные препараты, и не использовали никаких препаратов на протяжении более 3 месяцев до применения ТМС. Отказ от препаратов, со слов пациентов, был вызван низкой эффективностью либо полным отсутствием эффективности принимаемых препаратов.
Известно, что критериями эффективности лечения мигрени являются уменьшение частоты приступов и увеличение межприступного времени. В какой-то степени эти понятия взаимозависимы — если увеличить время межприступной ремиссии, то частота приступов в месяц уменьшится. Однако говорить о времени между приступами можно лишь условно, если известно, что приступы возникают не через равные промежутки времени, могут провоцироваться психоэмоциональными переживаниями, приемом некоторых лекарственных средств или продуктов питания и т.д. Поэтому мы брали среднее количество приступов в месяц до лечения и сравнивали с количеством приступов в месяц на протяжении 3 месяцев после курса ТМС. Мы получили следующие результаты (табл. 1).
В среднем у пациентов было 4,4 приступа в месяц до лечения ТМС, после курса пТМС средняя частота приступов в месяц изменилась и составила 3, что отображено на рис. 1. У 2 пациентов частота приступов не изменилась.
По шкале MIDAS у 3 пациентов до начала лечения верифицирована IIІ степень (18, 18 и 16 баллов), что соответствует сильной боли, выраженному ограничению повседневной активности. У остальных 7 пациентов до лечения верифицирована IV степень, что соответствует сильной боли, значительному снижению повседневной активности. Результаты представлены в табл. 2.
Основная идея шкалы MIDAS заключается в оценке влияния мигрени на повседневную активность, в определении выраженности дезадаптации. Мы получили результаты по шкале MIDAS и вывели среднее значение для всех пациентов до и после курса ТМС, что представлено на рис. 2.
Полученные результаты отражают улучшение повседневной активности, уменьшение количества дней, во время которых снижались работоспособность и активность. После курса пТМС изменилась выраженность дезадаптации у наших пациентов. Так, количество дней, в которые снижались работоспособность, бытовая активность, уменьшилось у всех пациентов, что представлено в табл. 2. При этом у 5 пациентов (на 2 больше, чем до курса пТМС) верифицирована IIІ степень (18, 12, 19, 12 и 15 баллов соответственно), что соответствует сильной боли, выраженному ограничению повседневной активности. У остальных 5 пациентов после курса ТМС верифицирована IV степень, что соответствует сильной боли, значительному снижению повседневной активности.
Оценка интенсивности головной боли в баллах по ВАШ показала, что интенсивность головной боли уменьшилась у 5 пациентов, у 4 из них боль уменьшилась на 1 балл, у 1 — на 2 балла (табл. 3).
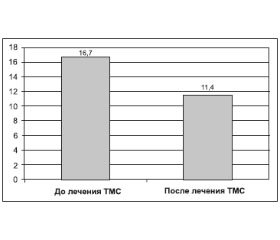
Известно, что мигрень часто сочетается с депрессивным расстройством. Между этими двумя патологическими состояниями присутствует прямая связь: мигрень служит хорошей почвой для появления депрессивного расстройства, которое, в свою очередь, усугубляет проявления мигрени. Как сказано выше, мы использовали шкалу Гамильтона. Эта шкала отражает состояние пациента в течение последней недели. Мы опрашивали наших пациентов перед началом курса пТМС и через 1 неделю после его окончания. Полученные результаты свидетельствуют об улучшении настроения, снижении выраженности подавленности и других проявлений депрессивного расстройства (рис. 3).
/88.jpg)
Таким образом, выраженность депрессивных проявлений по шкале Гамильтона уменьшилась на 31,7 %, при этом оценка по шкале MIDAS, свидетельствующая о снижении повседневной активности, улучшилась на 23,7 %, частота приступов в месяц уменьшилась на 31,8 %, а интенсивность головной боли во время приступа снизилась только на 6,9 %. Учитывая то, что уменьшилась частота приступов, закономерно ожидать увеличение активности и трудоспособности. При этом частота приступов уменьшилась не у всех пациентов, а оценка по шкале MIDAS — у всех. Мы считаем, что такой эффект связан также с изменением выраженности депрессивных проявлений, которая, безусловно, влияет на активность. К тому же в 2 случаях пациенты, не указывающие динамику по частоте приступов и интенсивности головной боли, тем не менее, отмечали улучшение общего состояния.
Побочные эффекты. Согласно литературным данным, за время применения ТМС в качестве метода диагностики и лечения заболеваний нервной системы описаны различные побочные явления [10]. Самыми частыми являются усиление головной боли, головокружение, зуд в месте стимуляции, а самым опасным — индуцированный магнитной стимуляцией судорожный приступ. Мы не наблюдали никаких побочных эффектов ТМС у наших 10 пациентов.
Выводы
Транскраниальная магнитная стимуляция, основанная на протоколе повторяющихся стимулов, — безопасный и эффективный метод, позволяющий уменьшить частоту приступов мигрени на 31,8 %, добиться улучшения настроения и уменьшения выраженности депрессивных включений на 31,7 %, снижения дезадаптации — на 23,7 %, уменьшения интенсивности головной боли — на 6,9 %.
Несмотря на обнадеживающие результаты, применение ТМС в качестве средства превентивной терапии при мигрени требует дальнейшего изучения.
Список литературы
1. Артеменко А.Р. Лечение хронической мигрени / Артеменко А.Р., Куренков А.Л., Никитин С.С. // Журнал неврологии и психиатрии. — 2011. — № 5. — С. 85-89.
2. Дубенко О.Е. Профилактическое лечение мигрени / Дубенко О.Е., Сотников Д.Д. // Международный неврологический журнал. Головная боль (тематический номер). — 2009. — С. 24-29.
3. Евтушенко С.К. Применение метода транскраниальной магнитной стимуляции в клинической неврологии / Евтушенко С.К., Казарян Н.Э., Симонян В.А. // Международный неврологический журнал. — 2007. — № 5. — С. 119-126.
4. Мищенко Т.С. Мигрень: эпидемиология, диагностика, лечение, профилактика / Мищенко Т.С. // Здоровье Украины. — 2010. — № 2. — С. 7-9.
5. Морозова О.Г. Мигрень: современные представления о классификации, диагностике, терапии и профилактике (Часть I) / Морозова О.Г. // Медицина неотложных состояний. — 2012. — № 4. — С. 32-41.
6. Almaraz A.C. The effect of prophylactic medications on TMS for migraine aura / Almaraz A.C., Dilli E., Dodick D.W. // Headache. — 2010. — № 10. — 1630-3.
7. Barker A.T. Noninvasive magnetic stimulation of the human motor cortex / Barker A.T., Jalinous R., Freeston I.L. // Lancet. — 1985. — 1. — 1106-1107.
8. Clarke B.M. Transcranial magnetic stimulation for migraine: clinical effects / Clarke B.M., Upton A.R.M., Kamath M.V. et al. // Headache Pain. — Oct 2006. — № 7(5). — 341-346.
9. Lipton R.B. Single-pulse transcranial magnetic stimulation for acute treatment of migraine with aura: a randomised, double-blind, parallel-group, sham-controlled trial / Lipton R.B., Dodick D.W., Silberstein S.D. // Lancet Neurol. — 2010. — № 9. — 373-380.
10. Rossi S. Safety, ethical considerations, and application guidelines for the use of transcranial magnetic stimulation in clinical practice and research / Rossi S., Hallett M., Rossini P.M. // Clin. Neurophysiol. — 2009. — № 120. — 2008-2039.
11. Wassermann E.M. Therapeutic application of repetitive transcranial magnetic stimulation: a review / Wassermann E.M., Lisanby S.H. // Clin. Neurophysiol. — 2011. — № 112. — 1367-1377.
/86.jpg)
/88.jpg)

/87.jpg)
/87_2.jpg)