Резюме
Проведено дослідження вмісту микротубуласоційованого тау-протеїну у сироватці крові 42 пацієнтів з різними нейродегенеративними захворюваннями (середній вік досліджуваних хворих — 58,31 ± 13,49 року), в тому числі осіб з хворобою Альцгеймера (n = 8, середній вік — 69,76 ± 9,5 року), первинно-генералізованою фармакорезистентною епілепсією (n = 23, середній вік — 40,95 ± 7,30 року) і з хворобою Паркінсона, тремтільна форма (n = 11, середній вік — 51,38 ± 12,61 року), а також контрольна група (n = 30, середній вік — 42,11 ± 5,67 року). У даній роботі для визначення тау-протеїну було застосовано імунофлюоресцентний метод з використанням первинних і вторинних моноклональних антитіл (SIGMA, США). Показано, що вміст тау-протеїну рівномірно збільшений практично в усіх хворих з нейродегенеративною патологією незалежно від типу перебігу з тенденцією до більш високих даних у пацієнтів з хворобою Альцгеймера. Ідентифікація тау-протеїну може служити неспецифічним маркером аксонального пошкодження, що супроводжує різні типи перебігу нейродегенерації.
Проведено исследование содержания микротубулассоциированного тау-протеина в сыворотке крови 42 пациентов с различными нейродегенеративными заболеваниями (средний возраст обследованных больных — 58,31 ± 13,49 года), в том числе лиц с болезнью Альцгеймера (n = 8, средний возраст — 69,76 ± 9,50 года), первично-генерализованной фармакорезистентной эпилепсией (n = 23; средний возраст — 40,95 ± 7,30 года) и болезнью Паркинсона, дрожательная форма (n = 11; средний возраст — 51,38 ± 12,61 года), а также контрольная группа (n = 30, средний возраст — 42,11 ± 5,67 года). В данной работе для определения тау-протеина был применен иммунофлуоресцентный метод с использованием первичных и вторичных моноклональных антител (SIGMA, США). Показано, что содержание тау-белка равномерно повышено практически у всех больных с нейродегенеративной патологией независимо от ее типа течения с тенденцией к более высоким показателям у пациентов с болезнью Альцгеймера. Идентификация тау-протеина может служить неспецифическим маркером аксонального повреждения, которое сопровождает различные типы течения нейродегенерации.
This investigation was carried out to study the content of microtubule-associated tau protein in sera of 42 patients with different neurodegenerative disorders (mean age of patients was 58.31 ± 13.49 years), among them there were eight patients with Alzheimer’s disease (mean age 69.76 ± 9.50 years), primary-generalized pharmacoresistant epilepsy (n = 23, mean age 40.95 ± 7.3 years) and Parkinson’s disease, tremor form (n = 11, mean age 51.38 ± 12.61 years), healthy controls (n = 30, mean age 42.11 ± 5.67 years). In this work for tau protein evaluation, immunofluorescence method was used with the primary and secondary monoclonal antibodies (SIGMA, USA). It was shown that tau protein content is evenly increased in almost all patients with neurodegenerative pathology, regardless of its course, with a tendency to higher values in patients with Alzheimer’s disease. Identification of tau protein may serve as a non-specific marker of axonal damage that accompanies various types of neurodegeneration.
Введение
Сложной проблемой клинической патоневрологии является ранняя диагностика аксонального повреждения головного мозга (АПГМ) с последующей верификацией этиопатогенетических данных. Определение в крови антител или других биомаркеров повреждения нейронных мембран позволяет решить проблему своевременной и адекватной диагностики АПГМ и дает нам возможность продолжить поиск новых терапевтических путей данного патологического состояния. АПГМ является отличительной клинико-патологической чертой черепно-мозговой травмы (ЧМТ) и связано с диффузным повреждением структуры головного мозга, при котором формируются микроскопические мелкоочаговые кровоизлияния, выявляемые преимущественно в мозолистом теле, полуовальном центре и верхних отделах ствола мозга [1, 12]. Также вследствие разрыва аксона и выхода аксоплазмы в спинномозговую жидкость в первые часы и сутки после ЧМТ [8] или, например, после повреждения головного мозга инфекционно-воспалительного генеза [13, 15] наблюдается значительная дезорганизация ней-рофиламентного скелета аксонов с последующим нарушением аксоплазматического тока. Одним из патологических клинических условий, ассоциированным с аксональным повреждением, также является нейродегенеративный процесс [5, 7].
В многочисленных экспериментальных работах зарубежных авторов показано, что тепловой белок, необходимый для создания микротрубочек цитоскелета аксона, был идентифицирован [9] и обозначен как тау (τ)-протеин (Tau protein) [14], который регулирует образование аксональных микротубул и служит для проведения информации из одной части аксона в другую. В неполимеразных условиях тау-протеин представляет собой от 6S димера до 36S кольцевых структур, вовлеченных как нейротрансмиттеры в процесс формирования тубулина. Уникальная возможность тау-протеина восстанавливать нормальные свойства микротубульной агрегации in vitro делает его одним из важнейших регуляторов формирования и создания микротубул (микротрубочек цитоскелета). При болезни Альцгеймера (БА) и других таупатиях избыточно фосфорилирующийся тау-белок образует нейрофибриллярные клубки, тем самым прекращая стабилизировать микротрубочки и нарушая работу аксона и нейрона [7, 9, 12]. Тау-протеин — это новый класс аксональных микротубулассоциированных фосфобелков (Microtubule-associated phosphorproteins), функция которых, прежде всего, — формирование аксона и поддержание его структурной микротубульной организации: тепловой белок тау формирует, регулирует и поддерживает цитоскелет. Тау-протеин изначально вовлечен во многие нейротоксические дегенеративные механизмы: нити гиперфосфорилированного тау-белка объединяются между собой и образуют нейрофибриллярные тяжи внутри нервных клеток, что приводит к выраженной дезинтеграции микротубул аксонов и деструкции транспортной системы нейрона [5, 7, 9, 12]. Последние исследования показали, что тау-белок был также идентифицирован как диагностический биомаркер раннего аксонального повреждения не только у пациентов с ЧМТ [8, 15], но также и у пациентов с фармакорезистентной эпилепсией [3, 11], рассеянным склерозом [6, 10, 13] и инсультом [2].
Однако, несмотря на достаточное количество работ, клинико-патогенетическая роль тау-белка в механизмах диффузного аксонального повреждения при нейродегенеративном процессе не до конца изучена. Определение особенностей содержания тау-белка у больных с нейродегенерацией позволит повысить качество диагностики и лечения данных пациентов. В этом исследовании изучали содержание теплового тау-белка в сыворотке крови у лиц с различными нейродегенеративными заболеваниями.
Материалы и методы
Для постановки диагноза болезни Альцгеймера были использованы критерии NINCDS-ADRDA (the National Institute of Neurological and Communicative Disorders and Strokes and the Alzheimer Disease Related Disorders Association, 1984). По данным анамнеза, физикального осмотра, инструментального обследования (магнитно-резонансная и компьютерная томография) и нейропсихологическим данным, у пациентов была диагностирована деменция той или иной степени выраженности: нарушение корковых функций (афазия, агнозия), снижение мотиваций, возбудимость и нарушение социального поведения, также по данным нейровизуализации у всех пациентов с БА выявлена церебральная атрофия. В данном исследовании выделен 2-й подтип БА с ранним началом (до 65 лет, согласно Международной классификации болезней 10-го пересмотра) в зависимости от возраста начала заболевания и особенностей клинической картины [1]. Диагноз болезни Паркинсона был выставлен в соответствии с критериями Huges (1992) [1]. Систематизация клинических проявлений эпилепсии осуществлялась на основе Международной классификации эпилепсии, принятой на конгрессе Международной лигой по борьбе с эпилепсией в октябре 1989 г. в Нью-Дейли (США) [3]. С целью изучения функциональной активности нейронов и выявления эпилептической патологической активности нами проводилась регистрация биопотенциалов головного мозга методом электроэнцефалографии с помощью 19-канального электроэнцефалографического комплекса (DX-NT32.V19, Украина).
Для определения содержания тау-белка в сыворотке крови человека был использован иммуно-флуоресцентный метод, основанный на конкурентном связывании моноклональных антител, которые специфичны к двум разным эпитопам IgG и IgM тау-белка (модифицированный метод Zemlan F., 2003) [15]. Иммунофлуоресцентный метод — метод флуоресцентного окрашивания, при котором исследуемый тау-протеин помечается антителами, конъюгированными FITC (Flurescein Isothiocyanate), с последующей их визуализацией. Образцы инкубировали с первичными моноклональными антителами в присутствии вторичных антител, меченных флуоресцентом, отмывка фиксированных и несвязанных комплексов проводилась концентратом фосфатно-солевого буферного раствора с твином. В данном исследовании были использованы мышиные антитела IgG (γ-chain specific) FITC-конъюгированные (Affinity isolated antigen specific antibodies) и моноклональные анти-τ (Tau) антитела Clone TAU-5, Mouse Ascites Fluid (SIGMA, США). Результаты флуоресцентного свечения оценивали с применением микроскопа Olympus BX41 (Япония) при увеличении × 100, × 600: коэффициент поглощения, Zeisus-135, расчет оптической плотности в условных единицах проводился с применением десятичного логарифма (D = Log10Ftau/F0). Статистическая обработка результатов исследования проходила с использованием пакета статистических программ Statgraph, оценка связи между рядами наблюдений — с помощью корреляционного анализа с вычислением линейного коэффициента Стьюдента (t-критерий) [4].
Результаты и обсуждение
В основу работы положены результаты обследования 42 пациентов с нейродегенеративными заболеваниями [1], которые находились на обследовании и лечении в ГУ «Институт неврологии, психиатрии и наркологии НАМНУ», в возрасте от 49 до 78 лет (средний возраст всех обследованных больных — 58,31 ± 13,49 года). В том числе пациенты с болезнью Альцгеймера (n = 8, средний возраст — 69,76 ± 9,50 года), первично-генерализованной фармакорезистентной эпилепсией (n = 23, средний возраст — 40,95 ± 7,30 года) и болезнью Паркинсона, дрожательная форма (n = 11, средний возраст — 51,38 ± 12,61 года). Контрольная группа состояла из 30 практически здоровых лиц: женщины (n = 22; 73,33 %) и мужчины (n = 8; 26,67 %) в возрасте от 35 до 45 лет (средний возраст — 42,11 ± 5,67 года) с благоприятной наследственностью и отсутствием неврологической, психиатрической и соматической патологии.
Первую клиническую группу составили пациенты с болезнью Альцгеймера, из них 5 женщин (62,5 %) и 3 мужчин (37,5 %). Промежуток времени от появления первых симптомов до развития деменции составлял в среднем 6,33 года. Вторую клиническую группу составили больные с первично-генерализованной фармакорезистентной эпилепсией, из них 14 мужчин (60,86 %) и 9 женщин (39,14 %). У больных этой клинической группы наблюдались абсансы, тонико-клонические и миоклонические припадки, а также полиморфные приступы, которые представляли собой варианты сочетания тонико-клонических приступов с абсансами. Преобладали полиморфные припадки, которые имели место у 12 больных (52,17 % больных 2-й группы) и были частыми у 7 больных (30,43 %) и средней частоты — у 5 больных (21,73 %), в основном за счет тонико-клонических припадков. Также эпилептические припадки наблюдались у 2 пациентов с болезнью Альцгеймера. Третья клиническая группа была сформирована из пациентов с болезнью Паркинсона, дрожательная форма (из них 5 женщин, 45,5 %; 6 мужчин, 54,5 %), у которых паркинсонизм мог быть одним из основных или дополнительных проявлений других нейродегенеративных заболеваний с поражением экстрапирамидной системы.
Результаты исследования и статистической обработки полученных данных изучения содержания тау-протеина у обследованных лиц представлены в табл. 1, из которой видно, что содержание тау равномерно повышено у практически у всех больных с нейродегенеративной патологией по сравнению со здоровым контролем. Полученные данные совпадают с данными ряда зарубежных авторов [5, 8, 15].
/39_2.jpg)
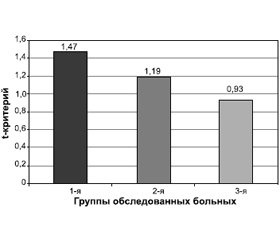
Наше исследование показало, что концентрация тау в сыворотке крови достоверно повышена: у больных с болезнью Альцгеймера по сравнению со здоровым контролем — на 0,82 усл. ед. оптической плотности (ОD), у больных с первично-генерализованной эпилепсией — на 0,7 усл. ед. ОD, у больных с болезнью Паркинсона — на 0,66 усл. ед. ОD (p < 0,05). Анализ степеней отклонения от контрольных значений (t-критерий) уровня тау-протеина выявил, что наблюдаемая разница между показателями была достаточно выражена (t = 1,47, 1,19 и 0,93 соответственно для 1-й, 2-й и 3-й групп). Таким образом, у всех больных с нейродегенеративной патологией независимо от типа ее течения отмечается достоверное и равномерное повышение уровня тау-протеина в сыворотке крови с тенденцией к более высоким показателям у пациентов с болезнью Альцгеймера (рис. 1).
/39.jpg)
Неврологическая симптоматика выявлена у большинства обследованных больных всех клинических групп, наиболее часто наблюдались асимметрия носогубных складок — у 7 больных 1-й группы (87,5 %), у 14 больных 2-й группы (60,86 %) и у 9 больных — 3-й (81,81 %); нарушение координации и статики — у 5 больных 2-й группы (21,73 %) и 4 больных — 3-й (36,36 %); повышение сухожильных и надкостничных рефлексов — у 6 больных 1-й группы (75 %), у 11 больных 2-й группы (47,83 %) и у 3 больных — 3-й (27,3 %); нистагм — у 2 больных 1-й группы (25 %), у 9 больных 2-й группы (39,13 %) и у 4 больных — 3-й; нарушение чувствительности — у 1 больного 2-й группы (4,34 %); глазодвигательные нарушения — у 3 больных 1-й группы (37,5 %), у 12 больных 2-й группы (52,18 %) и у 1 больного — 3-й (9,09 %); патологические стопные рефлексы — у 6 больных 1-й группы, у 4 больных 2-й группы (17,39 %) и у 5 больных — 3-й (45,4 %); девиация языка — у 2 больных 1-й группы (8,69 %).
Вопрос о содержании микротубулассоциированных белков пирамидных нейронов в сыворотке крови является принципиально важным с точки зрения патогенеза АПГМ. У больных с нейродегенеративной патологией высокий уровень тау в крови может отражать степень выраженности и/или распространенности дегенеративного процесса в центральной нервной системе, которые вызваны повреждением нейрофиламентного скелета клетки, и сопровождается повышением концентрации тау в крови и спинномозговой жидкости. Учитывая, что болезнь Альцгеймера является хроническим прогрессирующим заболеванием, важным фактором у пациентов 1-й группы становится длительность нейродегенеративного заболевания. У пациентов 1-й группы отмечается тенденция к увеличению количества тау в сыворотке крови с увеличением возраста больных, однако недостаточность клинического материала не позволила статистически подтвердить данное научное утверждение в каждой из подгрупп (р > 0,05).
Таким образом, данные результаты проведенного научного исследования делают целесообразным, интересным и нужным дальнейшее изучение содержания тау-протеина в сыворотке крови и спинномозговой жидкости больных с различной нейродегенеративной патологией и изучение состояния маркеров аксонального повреждения головного мозга при других неврологических и психиатрических заболеваниях с определением их прогностической роли в патогенезе и исходе этих заболеваний.
В данной научной работе изложен современный взгляд на проблему диагностики аксонального повреждения головного мозга у больных с различными нейродегенеративными заболеваниями, где особое внимание уделено роли тау-протеина как нового серологического биомаркера аксонального повреждения [5–8]. Показано, что у данной категории пациентов имеет место повышение уровня тау в сыворотке крови (p < 0,05) по сравнению с контролем. Идентификация тау-протеина в сыворотке крови может служить маркером диффузного аксонального повреждения, которое сопровождает различные типы течения нейродегенерации. Данное исследование свидетельствует о необходимости продолжения рассматриваемой проблемы.
Выводы
Полученные в исследовании данные показывают, что уровень тау-протеина равномерно повышен практически у всех больных с нейродегенеративной патологией независимо от ее типа течения, и более выражены данные изменения у пациентов с болезнью Альцгеймера. Тау-протеин служит неспецифическим маркером аксонального повреждения, сопровождающим различные типы течения нейродегенеративного процесса. Необходимо дальнейшее изучение содержания тау у пациентов с нейродегенеративными заболеваниями для разработки дифференциально-диагностических и прогностических критериев течения и поиска новых путей лечения этой категории пациентов.
Конфликт интересов. Автор заявляет об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Дополнительная информация
В ходе исследования были сделаны электронные микрофотографии патологического тау-протеина сыворотки крови у больных 1-й группы, демонстрирующие иммунофлуоресцентное окрашивание микротубулассоци-ированного тау-протеина у больной с болезнью Альцгеймера (71 год, время от появления первых симптомов до развития выраженной деменции — в среднем 6 лет) в реакции с моноклональными антителами (Sigma, USA). Фото показывает зеленые размытые флуоресцирующие нити тау-протеина (green fluorescent tau protein, GFtP), меченные антимышиными IgG (γ-chain specific) FITC-конъюгированными моноклональными антителами.
Всем заинтересованным читателям автор готова предоставить данные фотографии, для чего просьба связаться с автором по электронной почте.
Список литературы
1. Болезни нервной системы: В 2 т. / Под ред. Н.Н. Яхно, Д.Р. Штульмана. — М.: Медицина, 2001. — 480 с.
2. Ворлоу Ч.П., Деннис М.С., Гейн Ж.В. Инсульт. Практическое руководство для ведения больных: Пер. с англ. — СПб.: СП «Политехника», 1998. — 629 с.
3. Зенков Л.Р. Клиническая эпилептология (с элементами нейрофизиологии). — М.: Медицинское информационное агентство, 2002. — 416 с.
4. Иванов Ю.И., Погорелюк О.Н. Обработка результатов медико-биологических исследований на микрокалькуляторах. — М.: Медицина, 1990. — 218 с.
5. Avila J., Lucas J., Perez M., Hernandez P. Role of Tau Protein in both physiological and pathological conditions // Physiol. Rev. — 2004. — Vol. 84. — P. 361-384.
6. Bartosik-Psuiek H., Stelmasiak Z. The CSF levels of total-tau and phosphor-tau in patients with relapsing-remitting multiple sclerosis // J. Neural. Transm. — 2006. — 113. — P. 339-345.
7. Blennow K., Zetterberg H. // Alzheimer Disease Lancet. — 2006. — 368. — P. 387-403.
8. Bulut M., Koksal O., Dogan S. et al. Tau protein as a serum marker of brain damage in mild traumatic brain injury: Preliminary results // Advances in Therapy. — 2006. — № 23(1). — Р. 12-22.
9. Delacourte A. Tauopathies: recent insights into old diseases // Folia Neuropathol. — 2005. — № 43. — Р. 244-257.
10. Kapaki E., Paraskevaz G., Michalopoulou M., Kilidireas K. Increased cerebrospinal luid tau protein in multiple sclerosis // Eur. Neurol. — 2000. — № 43(4). — P. 228-232.
11. Lekomtseva Y., Gorbach T., Gubina-Vakulik G. High serum tau protein in patients with therapy-resistant intractable epilepsy under a baseline // J. of Neurology. — 2009. — Vol. 256(Suppl. 2). — P. S77.
12. Roder H.M., Hutton M.L. Microtubule-associated protein tau as a therapeutic target in neurodegenerative disease // Expert Opin. Ther. Targets. — 2007. — № 11(4). — Р. 435-442.
13. Terzi M., Birinci A., Cetinkaya E., Onar M.K. Cerebrospinal fluid total tau protein levels in patients with multiple sclerosis // Acta Neurol. Scand. — 2007. — 115(5). — Р. 325-30.
14. Uchihara T., Duyckaerts C., Seilhean D. et al. Exclusive induction of tau2 epitope in microglia/macrophages in inflammatory lesions-tautwopathy distinct from degenerative tauopathies // Acta Neuropathol. — 2005. — 109. — P. 159-164.
15. Zemlan P.F. US Patent 6589746. Method of detecting axonally-derived protein tau in patients with traumatic CNS injury // Traumatic CNS injury. — 2003.
/39.jpg)

/39_2.jpg)