Черепно-мозкова травма (ЧМТ) і гострі порушення мозкового кровообігу (ГПМК) є одними з найпоширеніших причин смерті й інвалідизації населення. Згідно з епідеміологічними дослідженнями, інсульт посідає чільне місце в структурі смертності й інвалідизації населення, становлячи собою значну медичну й соціально-економічну проблему [3–5, 9]. Також значною проблемою є травматичні ушкодження черепа й головного мозку, які становлять 30–40 % усіх травм. ЧМТ є головною причиною летальності й інвалідизації серед осіб працездатного віку. Щороку у світі понад 10 млн осіб одержують ЧМТ, 250–300 тис. з яких закінчуються летально (відповідно до даних ВООЗ). Частота ЧМТ в Україні становить у середньому 4–4,2 випадку на 1000 населення, що щорічно призводить до летального кінця в 10–11 тис. осіб [22, 24]. Високий рівень смертності пацієнтів і недостатньо ефективні результати лікування ЧМТ і ГПМК свідчать про необхідність подальшого вивчення різних аспектів лікування з використанням принципів доказової медицини.
Найважливішим фактором, що безпосередньо впливає на прогноз при ГПМК і ЧМТ, є гіпоксія нейронів [30]. У патогенезі мозкової ішемії, як показали результати багатьох досліджень, важливу роль відіграє набряк головного мозку, що призводить до вторинного пошкодження нейронів. Це, у свою чергу, диктує необхідність включення до комплексної терапії ішемічного інсульту і ЧМТ протинабрякових препаратів уже на ранніх етапах захворювання. Набряк тканин, що розвинувся в зоні ушкодження, призводить до подальших ішемічних і гіпоксичних порушень і зрештою — до некрозу й апоптозу клітинних структур [10]. У зв’язку зі значним впливом внутрішньочерепного тиску (ВЧТ) на прогноз при ураженні головного мозку велика кількість протоколів ведення хворих з ГПМК і ЧМТ акцентують увагу саме на цьому клінічному показнику [33].
Іншим клінічним і прогностичним критерієм, що використовується як при ЧМТ, так і при ГПМК, є шкала коми Глазго (ШКГ), яка об’єктивно відображає рівень свідомості пацієнта. ШКГ, розроблена 1974 року, є найпоширенішим клінічним критерієм для оцінки ураження мозку. У численних дослідженнях було показано, що при пошкодженні головного мозку показник ШКГ вірогідно корелював з рівнем смертності та шкалою результатів Глазго [28, 31].
Специфічним маркером тяжкості неврологічної симптоматики в гострому періоді ГПМК є шкала NIHSS (National Institutes of Health Stroke Scale). Показник шкали NIHSS ≤ 6 балів є предиктором сприятливого результату, тоді як показник ≥ 11 з високою імовірністю визначає негативний прогноз захворювання (тяжку інвалідизацію та смерть) [25, 27]. Слід зазначити, що шкала NIHSS вважається більш точним предиктором негативного неврологічного результату при ГПМК, ніж ШКГ [31].
Як уже зазначалося, у клінічній практиці набряковий синдром є одним із провідних патологічних синдромів, характерних для різних захворювань та ушкоджень головного мозку. У переважній більшості випадків він не тільки є симптомом, але й значно обтяжує перебіг патологічного процесу. Набряковий синдром призводить до так званого синдрому невідновленого кровотоку і, як наслідок, обтяжує перебіг захворювання або пошкодження; з іншого боку, тривалий період невідновленого кровотоку сприяє виникненню тяжкого реперфузійного пошкодження органів і тканин і дуже часто є причиною посилення або рецидиву патологічного процесу. Тому своєчасне лікування набрякового синдрому і запобігання йому при критичних станах і локальних ушкодженнях є важливим завданням і має включатися до комплексу інтенсивної терапії гострого захворювання або ушкодження [10].
У зв’язку з цим стає актуальним питання вибору адекватних, безпечних та ефективних протинабрякових лікарських засобів. Одним з таких препаратів є L-лізину есцинат, розчин для ін’єкцій, виробництва ПАТ «Галичфарм» Корпорації «Артеріум». Цей препарат застосовується в складі комплексної терапії при посттравматичних, інтра- і післяопераційних набряках будь-якої локалізації: тяжких набряках головного і спинного мозку, у тому числі з внутрішньочерепними крововиливами, підвищенням внутрішньочерепного тиску і явищами набряку-набухання; лікворно-венозних порушеннях при хронічних порушеннях мозкового кровообігу і вегетосудинній дистонії; набряках м’яких тканин із залученням опорно-рухового апарату, що супроводжуються локальними розладами кровопостачання і больовим синдромом; набряково-больових синдромах з боку хребта, кінцівок; тяжких порушеннях венозного кровообігу нижніх кінцівок при гострому тромбофлебіті, що супроводжуються набряково-запальним синдромом.
L-лізину есцинат виявляє виражену і швидку протинабрякову дію, усуває або істотно зменшує набряк-набухання головного і спинного мозку, а також мозкових оболонок, усуває стиснення і дислокацію структур мозку, знижує внутрішньочерепну гіпертензію. Препарат поліпшує еластичність вен, підвищує тонус венозних судин, нормалізує реологічні властивості крові, поліпшує мікроциркуляцію, дозозалежно знижує судинно-тканинну проникність і проникність плазмолімфатичного бар’єра, зменшує активність лізосомальних ферментів і перешкоджає виникненню ексудативної реакції на простагландини, у зв’язку з чим препарат має також протизапальну і знеболювальну дію. Венотонізуючий ефект має суттєве значення для поліпшення венозного кровообігу і запобігання венозному рефлюксу. L-лізину есцинат має також імунокоригуючий ефект, усуває стресову гіперглікемію в пацієнтів з пошкодженням мозку і нормалізує рівень глюкози в крові, запобігаючи розвитку або усуваючи явища ацидозу мозкової тканини й посилення церебрального пошкодження [19].
/222.jpg)
Мета даної роботи — систематизувати дані клінічних досліджень ефективності й безпеки лікарського засобу (ЛЗ) L-лізину есцинат (вплив на показники летальності, ВЧТ, ШКГ і NIHSS).
Матеріали та методи
Стратегія пошуку
Було проведено літературний пошук за ключовими словами: «L-лізину есцинат», «ЧМТ», «ГПМК», «черепно-мозкова травма», «інсульт» у різних комбінаціях для ідентифікації контрольованих клінічних досліджень. Пошук проводили в таких електронних джерелах: Embase, Medline, PubMed, US Food and Drug Administration, NICE, The European Medicines Agency і каталоги Національної наукової медичної бібліотеки. Крім того, виробник ЛЗ L-лізину есцинат (ПАТ «Галичфарм» Корпорації «Артеріум») надав звіти про результати клінічних випробувань препарату при ЧМТ і ГПМК.
Критерії пошуку
Критерії відбору публікацій включали застосування ЛЗ L-лізину есцинат у пацієнтів з ГПМК і ЧМТ, мови публікації — українська, російська або англійська, дизайн дослідження — проспективне клінічне дослідження серед пацієнтів усіх вікових груп з наявністю контрольної групи.
Критеріями виключення були:
— дослідження з відсутністю контрольної групи;
— застосування ЛЗ у дозах, що перевищують рекомендовані в інструкції з медичного застосування;
— використання клінічно незначущих критеріїв ефективності.
Відбір літературних джерел
Проведено аналіз за назвами й резюме для виключення статей, які однозначно не належать до предмета огляду. Публікації, що залишилися, вивчалися повністю для відбору необхідних досліджень (табл. 1). Включення досліджень в аналіз узгоджено з усіма авторами метааналізу.
Публікації, відібрані при початковому пошуку, аналізувалися незалежно двома членами авторської групи. Усі розбіжності вирішувалися консенсусом.
Результати та обговорення
Під час пошуку у відкритих базах даних було ідентифіковано 21 літературне джерело. Виробник ЛЗ L-лізину есцинат додатково надав 4 звіти про проведені клінічні дослідження (КД), результати яких публікувалися не в повному обсязі; таким чином було опрацьовано 25 літературних джерел. Надалі, після виключення літературних джерел, що не задовольняють критеріям включення, а також після видалення дублюючих літературних джерел в метааналіз були включені результати 12 досліджень (рис. 1). Загальна кількість пацієнтів, які оцінюються, становила 1728. Згідно з аналізованими джерелами, L-лізину есцинат, розчин для ін’єкцій, додатково до базисної терапії приймали 727 пацієнтів. До аналізу були включені пацієнти всіх вікових груп з діагнозом ЧМТ і ГПМК з оцінкою таких параметрів: зміна ВЧТ; зміна за шкалою NIHSS; шкалою коми Глазго; шкалою результатів Глазго; летальність.
Аналіз зміни оцінок ВЧТ
У даний аналіз зміни ВЧТ було включено 82 пацієнти, які отримували додатково до базисної терапії L-лізину есцинат, і 60 пацієнтів, які проходили курс базисної терапії. Інформацію було отримано з 3 літературних джерел [6, 13, 14].
Відносна оцінка зміни ВЧТ обчислювалася за такою формулою:
Узагальнена оцінка відносної зміни аналізованих параметрів за публікаціями, у яких були присутні дані параметри, подана у вигляді арифметичного середнього зваженого, що обчислюється за формулою:
де wi — ваговий коефіцієнт (кількість пацієнтів) для xi, яке є середнім арифметичним для даної кількості пацієнтів.
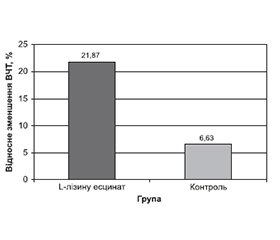
Відповідно до розрахунків ВЧТ унаслідок застосування L-лізину есцинату зменшився загалом на 21,87%. У пацієнтів, які отримували лише базисну терапію, ВЧТ знизився на 6,63 %.
Тому можна констатувати, що зменшення ВЧТ у пацієнтів, які приймали L-лізину есцинат, було більш вираженим, ніж у пацієнтів, які приймали лише базисну терапію.
Аналіз зміни оцінок стану пацієнтів за шкалою коми Глазго за період до 12 діб
В аналіз зміни оцінок стану пацієнтів за шкалою коми Глазго було включено 535 пацієнтів, які приймали додатково до базисної терапії L-лізину есцинат, і 459 пацієнтів, які проходили курс базисної терапії. При аналізі було взято оцінки, отримані за період до 12 діб. Наявні в деяких публікаціях значення оцінок ШКГ на 30-ту й 14-ту добу не аналізувалися. Інформація була отримана із 9 джерел [6, 7, 11–16, 23].
Відносна оцінка зміни стану пацієнтів за шкалою коми Глазго обчислювалася за формулою (1).
Узагальнена оцінка відносної зміни аналізованих параметрів за даними джерел, у яких ці параметри були присутні, надана у вигляді арифметичного середнього зваженого, що обчислюється за формулою (2). Графічно результати аналізу подані на рис. 3.
Згідно з виконаними розрахунками оцінки за шкалою коми Глазго стану пацієнтів, які додатково отримували L-лізину есцинат, підвищилися на 66,89 %.
У пацієнтів, які приймали лише базисну терапію, оцінки стану за шкалою коми Глазго підвищилися на 40,61 %.
Це дозволяє дійти висновку, що підвищення оцінок стану за шкалою коми Глазго в пацієнтів, які приймали L-лізину есцинат, було більш вираженим, ніж у пацієнтів, які приймали тільки базисну терапію.
Оцінка ефективності за зміною оцінок стану пацієнтів за шкалою результатів Глазго з 10-го по 30-й день
У даний аналіз зміни оцінок стану пацієнтів за шкалою результатів Глазго було включено 70 пацієнтів, які отримували додатково до базисної терапії L-лізину есцинат, і 50 пацієнтів, які отримували лише базисну терапію. Інформація була отримана з двох літературних джерел [13, 14].
Відносна оцінка зміни оцінок стану пацієнтів за шкалою результатів Глазго з 10-го по 30-й день обчислювалася за формулою (1).
Узагальнена оцінка відносної зміни аналізованих параметрів за публікаціями, у яких ці параметри були наявні, наведена у вигляді арифметичного середнього зваженого, що обчислюється за формулою (2). Графічно результати розрахунків подані на рис. 4.
Згідно з виконаними розрахунками, оцінка за шкалою результатів Глазго в пацієнтів, які додатково отримували L-лізину есцинат, підвищилася на 20,14 %.
У пацієнтів, які отримували лише базисну терапію, оцінка за шкалою результатів Глазго зросла на 13,79 %.
Це дозволяє дійти висновку, що підвищення оцінок за шкалою результатів Глазго в пацієнтів, які отримували L-лізину есцинат на додаток до базисної терапії, було більш вираженим, ніж у пацієнтів, які приймали тільки базисну терапію.
Оцінка ефективності за зміною оцінок за шкалою NIHSS
У даний аналіз зміни оцінок за шкалою NIHSS було включено 70 пацієнтів, які отримували додатково до базисної терапії L-лізину есцинат, і 70 пацієнтів, які отримували лише базисну терапію. Інформація була отримана із 3 джерел [8, 16, 19]. Період спостереження за динамікою за шкалою NIHSS — до 21 доби.
Відносна оцінка зміни за шкалою NIHSS обчислювалася за формулою (1).
Узагальнена оцінка відносної зміни аналізованих параметрів за джерелами (публікаціями або звітами), у яких були наявні дані параметри, подана у вигляді арифметичного середнього зваженого, що обчислюється за формулою (2). Графічно результати розрахунків подані на рис. 5.
Згідно з виконаними розрахунками, оцінки за шкалою NIHSS у пацієнтів, які додатково до базисної терапії отримували L-лізину есцинат, знизилися на 47,10%.
У пацієнтів, які отримували лише базисну терапію, оцінки за шкалою NIHSS знизилися на 30,15 %.
Це дозволяє дійти висновку, що зниження оцінок за шкалою NIHSS у пацієнтів, які отримували L-лізину есцинат на додаток до базисної терапії, було більш вираженим, ніж у пацієнтів, які приймали лише базисну терапію.
Аналіз зміни категоріальних оцінок за шкалою NIHSS
У двох джерелах [1, 11] було наведено динаміку оцінок неврологічного статусу пацієнтів за шкалою NIHSS у категоріальній інтерпретації. Загальновідомо, що для інтерпретації дані, отримані за шкалою NIHSS, перетворюють на категоріальні за такою категоріальною шкалою:
— 0–2 бали — нормальний стан;
— 3–8 балів — порушення легкого ступеня;
— 9–12 балів — порушення середнього ступеня;
— 13–15 балів — порушення тяжкого ступеня;
— понад 15 балів — дуже тяжкий стан;
— 34 бали — коматозний стан.
У статті В.В. Ніконова (2009) «Сучасні підходи до ведення пацієнтів з гострою церебральною недостатністю на догоспітальному та госпітальному етапах» [11] категорії були подані так: нормальний стан, легкі порушення, середні порушення, тяжкі порушення і вкрай тяжкі порушення, а в статті В.Є. Авакова (2015) «Застосування L-лізину есцинату у пацієнтів з черепно-мозковою травмою та гострим ішемічним інсультом» [1] — 0–8 балів, 9–12 балів і понад 12 балів; дані з джерела [5] також були адаптовані до цієї шкали, яка була інтерпретована таким чином:
— 0–8 балів — нормальний стан і порушення легкого ступеня;
— 9–12 балів — порушення середнього ступеня;
— > 12 балів — порушення тяжкого ступеня і дуже тяжкий стан.
Крім того, у джерелі [16] дані були подані на 1-шу добу, 7-му добу і день виписки, а в джерелі [1] — на 1-шу, 15-ту і 30-ту добу. Тому для аналізу було взято такі дані: вихідний стан на 1-шу добу і дані завершального візиту на день виписки або 30-ту добу. Усі пацієнти, які на додаток до базисної терапії приймали L-лізину есцинат, були об’єднані в одну групу, а пацієнти, які отримували тільки базисну терапію, — в іншу групу. Результати аналізу методами описової статистики наведено в табл. 2.
В аналіз було включено 119 пацієнтів, які отримували додатково до базисної терапії L-лізину есцинат, і 71 пацієнт, який отримував лише базисну терапію.
Графічно динаміка оцінок в об’єднаних групах наведена на рис. 6 і 7.
Для порівняння груп у вихідному стані й на 30-ту добу (або день виписки) був застосований критерій хі-квадрат Пірсона. Для оцінки значущості динаміки в групах був застосований критерій маргінальних частот (розширений критерій Мак-Немара для випадку, коли кількість категорій понад 2) [29, 26]. Розрахунки виконувались за допомогою програми SPSS 13.0.
Результати порівняльного аналізу об’єднаних груп методами описової статистики у вихідному стані наведено у табл. 3, а на момент завершення лікування (30-та доба або виписка) — у табл. 4.
Як видно з результатів аналізу (табл. 3), на 1-шу добу відмінності між групами за категоріальними оцінками за NIHSS були статистично незначними (р = 0,994).
На 30-ту добу або на момент виписки групи статистично значуще відрізнялися (р < 0,001) на користь групи пацієнтів, які додатково до базисної терапії отримували L-лізину есцинат, що свідчить про значний вплив даного препарату на відновлення неврологічного статусу пацієнтів. Графічно різницю між групами на заключному візиті (30-та доба чи виписка) наведено на рис. 8.
Оцінка летальності
В аналіз летальності було включено 518 пацієнтів, які отримували додатково до базисної терапії L-лізину есцинат, і 360 пацієнтів, які отримували лише базисну терапію. Оцінка летальності проводилася на підставі наявних в аналізованих джерелах даних про кількість померлих пацієнтів. Інформація була отримана із 8 джерел [1, 12–14, 16, 18, 20, 23]. Період спостереження для оцінки летальності — до 14 діб.
Оцінка статистичної значущості відмінностей летальності в об’єднаних групах (група L-лізину есцинат+ базисна терапія та група базисної терапії) була виконана за допомогою критерію хі-квадрат Пірсона. Результати аналізу подані в табл. 5 і на рис. 9.
На підставі отриманих результатів можна констатувати, що летальність у групі пацієнтів, які додатково до базисної терапії отримували L-лізину есцинат, була меншою на 10,75 %, ніж у групі пацієнтів, які отримували тільки базисну терапію. Відмінність між групами була статистично значущою (р < 0,001). Отже, можна стверджувати, що застосування на додаток до базисної терапії L-лізину есцинату дозволяє значно знизити летальність пацієнтів при гострій церебральній недостатності.
/11p.jpg)
Додатково на підставі наявних даних було виконано аналіз шансів імовірності виникнення летального результату або шансів імовірності виживання залежно від застосування L-лізину есцинату як доповнення до базисної терапії або застосування тільки базисної терапії. Для цього було обчислено співвідношення шансів за методикою, викладеною в літературі [2, 17, 21]. Згідно з отриманими результатами (табл. 5), застосування додатково до базисної терапії препарату L-лізину есцинат значно знижувало шанси виникнення летальних випадків (співвідношення шансів (СШ) = 0,45; 95% довірчий інтервал (ДІ) 0,31–0,65). При визначенні зворотного співвідношення шансів було встановлено, що застосування додатково до базисної терапії препарату L-лізину есцинат збільшувало виживання пацієнтів (СШ = 2,22; 95% ДІ 1,54–3,21) порівняно з тими хворими, які отримували лише базисну терапію.
Графічно як пряме співвідношення шансів (шанси ймовірності летального випадку), так і зворотне співвідношення шансів (шанси ймовірності виживання) подані на рис. 10.
Узагальнення оцінок переносимості
При оцінці 12 досліджень, у яких брали участь 727 пацієнтів, які отримували ЛЗ L-лізину есцинат, розчин для ін’єкцій, не було виявлено непередбачених побічних реакцій/побічних явищ, пов’язаних із застосуванням препарату L-лізину есцинат, які вимагали відміни препарату.
За даними постреєстраційного нагляду, за період з 18.11.2004 до 25.12.2008 при застосуванні L-лізину есцинату, розчину для ін’єкцій, частота побічних реакцій становила 0,005 %, а за період з 26.12.2008 по 25.07.2013— 0,0093 %. Реальна частота побічних реакцій при застосуванні ЛЗ L-лізину есцинат класифікується ВООЗ як рідкісний показник.
Висновки
1. При оцінці динаміки ВЧТ у 142 пацієнтів було показано, що в результаті застосування в складі комплексної терапії L-лізину есцинату, розчину для ін’єкцій, ВЧТ зменшився в середньому на 21,87 %, тоді як при застосуванні лише базисної терапії цей показник зменшився тільки на 6,63 %.
2. Оцінка стану пацієнтів за шкалою коми Глазго у 994 пацієнтів показала, що в тих, хто отримував додатково L-лізину есцинат, показники ШКГ збільшилися на 66,89 %, у той час як у групі пацієнтів, які приймали тільки базисну терапію, збільшення становило 40,61 %.
3. Оцінка за шкалою результатів Глазго у 120 пацієнтів показала, що у хворих, які додатково до базисної терапії отримували L-лізину есцинат, показники збільшилися на 20,14 %, тоді як у пацієнтів, які отримували лише базисну терапію, збільшення становило 13,79 %.
4. Динаміка оцінок за шкалою NIHSS у 140 пацієнтів у період до 21 доби спостереження показала, що в пацієнтів, які додатково отримували до базисної терапії L-лізину есцинат, значення NIHSS зменшилися на 47,10 %, у той час як у пацієнтів, які одержували лише базисну терапію, зменшення становило 30,15 %.
5. Дані, отримані за участю 190 пацієнтів, показали, що на 30-ту добу або на момент виписки категоризовані оцінки за шкалою NIHSS у групах статистично значуще відрізнялися (р < 0,001) на користь групи пацієнтів, які отримували додатково до базисної терапії L-лізину есцинат, що свідчить про значний вплив даного препарату на відновлення неврологічного статусу.
6. При оцінці загальної летальності пацієнтів у період до 14 діб за участю 878 пацієнтів одержано дані, що показують, що летальність у групі пацієнтів, які отримували додатково до базисної терапії L-лізину есцинат, була меншою на 10,75 %, ніж у групі пацієнтів, які отримували лише базисну терапію. Відмінність між групами була статистично вірогідною (р < 0,001).
7. Застосування додатково до базисної терапії ЛЗ L-лізину есцинат значно зменшувало імовірність виникнення летальних випадків (СШ = 0,45; 95% ДІ 0,31–0,65) і збільшувало шанси пацієнтів вижити (СШ= 2,22; 95% ДІ 1,54–3,21).
8. Реальна частота побічних реакцій при застосуванні ЛЗ L-лізину есцинат класифікується ВООЗ як рідкісний показник.
/1p.jpg)
/2p.jpg)
/9p.jpg)
/11p.jpg)
/13p.jpg)

/222.jpg)
/3p.jpg)
/4p.jpg)
/5p.jpg)
/6p.jpg)
/8p.jpg)
/7p.jpg)
/10p.jpg)
/12p.jpg)